Te zadania pojawiły się na maturze (aminokwasy, peptydy, białka)
2025:
2024:
2023:
2022:
Zadanie 8.3, Zadanie 29, Zadanie 30, Zadanie 31, Zadanie 32, Zadanie 33
2021:
Zadanie 33.1, Zadanie 33.2, Zadanie 34, Zadanie 35, Zadanie 36
2020:
Zadanie 30, Zadanie 31, Zadanie 32, Zadanie 39, Zadanie 40
2019:
2017:
2016:
2015:
Ustalanie procentowej zawartości wagowej fenyloalaniny w mieszaninie aminokwasów powstałej w wyniku hydrolizy tripeptydu
Przeprowadzono hydrolizę trójpeptydu znajdującego się w 80 g jego wodnego roztworu o stężeniu równym 9,1%. Podczas tego doświadczenia przebiegła reakcja chemiczna według schematu:
Phe-Ala-Lys + 2H2O → Phe + Ala + Lys
Po zakończeniu procesu hydrolizy pozostałą wodę odparowano i uzyskano 7,4 g stałej masy zawierającej nierozłożony oligopeptyd oraz trzy powstałe aminokwasy.
Oblicz, jaki procent wagowy stałej mieszaniny (uzyskanej po odparowaniu wody) stanowiła fenyloalanina? Wynik podaj z dokładnością do dwóch cyfr znaczących. Masy molowe wymienionych aminokwasów wynoszą: MPhe = 165 g/mol, MAla = 89 g/mol oraz MLys = 146 g/mol. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Ocena poprawności zdań dotyczących cząsteczki narysowanego tetrapeptydu
Wzór cząsteczki peptydu o sekwencji aminokwasów Asp-Ser-Ser-Gly można przedstawić rysunkiem:
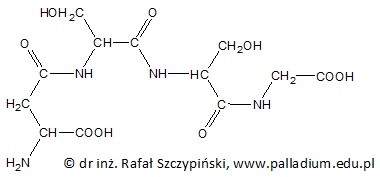
Oceń poprawność poniższych zdań dotyczących tetrapeptydu, którego wzór grupowy przedstawiony został w informacji wprowadzającej. Wpisz literę „P” (prawda) lub literę „F” (fałsz). 1. Możemy wyróżnić cztery atomy węgla stanowiące centra stereogeniczne opisanej cząsteczki tetrapeptydu. 2. W sprzyjających warunkach C-koniec cząsteczki tetrapeptydu może utworzyć z N-końcem wiązanie peptydowe. 3. Pomiędzy cząsteczkami tetrapeptydu tworzą się wiązania wodorowe. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Rysowanie wzoru stereochemicznego określonego stereoizomeru (izomeria optyczna)
Wzór cząsteczki peptydu o sekwencji aminokwasów Asp-Ser-Ser-Gly można przedstawić rysunkiem:

W cząsteczce narysowanego związku chemicznego reszta jednego z aminokwasów połączona jest wiązaniem peptydowym z resztą innego aminokwasu w sposób odmienny niż ten, jaki obserwuje się w łańcuchach peptydowych białek pochodzenia naturalnego.
Uzupełnij poniższy szablon tak, aby przedstawiał cząsteczkę niebiogennego aminokwasu, o którego reszcie mowa jest w powyższym tekście. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone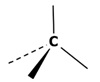
Określanie odczynu wodnego roztworu estru wraz z uzasadnieniem równaniem reakcji chemicznej
Przeprowadzono reakcję estryfikacji glicyny za pomocą etanolu stosując jego niewielki nadmiar. Po wyodrębnieniu organicznego produktu opisanej przemiany chemicznej umieszczono go w kolbie zawierającej wodę destylowaną.
Określ odczyn uzyskanego w ten sposób wodnego roztworu estru. Odpowiedź uzasadnij równaniem chemicznym procesu zapisanym w formie jonowej skróconej. Odczyn roztworu: Równanie chemiczne: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Rysowanie projekcji Fischera D-penicylaminy oraz wzoru stereochemicznego jej enancjomeru i określanie stopnia utlenienia centrum stereogenicznego cząsteczki (izomeria optyczna)
Penicylamina to zwyczajowa nazwa kwasu 2-amino-3-merkapto-3-metylobutanowego. Dzięki obecności grupy –SH (merkaptanowej), cząsteczki tego związku chemicznego mają zdolność do tworzenia trwałych kompleksów z dwu- oraz trójdodatnimi jonami tzw. metali ciężkich. Kompleksy takie stosunkowo łatwo usuwane są z organizmu. Fakt ten stanowił podstawę pierwotnego zastosowania D-penicylaminy, jakim była detoksykacja organizmu po zatruciu metalami ciężkimi.
Na podstawie: D. Steinhilber i inni, Chemia medyczna. Cele leków, substancje czynne, biologia chemiczna, Wrocław 2012.
Narysuj projekcję Fischera D-penicylaminy oraz wzór przestrzenny (stereochemiczny) jej enancjomeru, a następnie określ wartość stopnia utlenienia atomu węgla stanowiącego centrum stereogeniczne cząsteczki D-penicylaminy © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określanie wzoru półstrukturalnego produktu kondensacji dwóch cząsteczek aminokwasu
W odpowiednich warunkach, dwie cząsteczki α-aminokwasu mogą ulegać kondensacji z utworzeniem cyklicznego związku organicznego o masie cząsteczkowej mniejszej o 36 u od sumy mas cząsteczkowych aminokwasów biorących udział w opisanej reakcji chemicznej. Częściowa hydroliza uzyskanego produktu prowadzi do powstania łańcuchowego dipeptydu.
Narysuj wzór półstrukturalny opisanego produktu kondensacji dwóch cząsteczek izoleucyny. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zapis równania reakcji przebiegającej podczas miareczkowania roztworu aminokwasu
Po wprowadzeniu aminokwasu do wody destylowanej i rozpuszczeniu go ustala się równowaga dynamiczna między jego postacią kationową, anionową oraz jonem obojnaczym. W układzie takim dwie pierwsze wymienione struktury niemal nie istnieją.
Miareczkowano wodny roztwór waliny za pomocą roztworu wodorotlenku sodu.
Napisz w formie jonowej skróconej równanie przebiegającej reakcji chemicznej. Zastosuj półstrukturalne (grupowe) wzory odpowiednich form aminokwasu. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Rysowanie wzoru grupowego cząsteczki karbocysteiny ze wskazaniem liczby atomów węgla o określonym modelu hybrydyzacji
Substancją czynną wchodzącą w skład leków stosowanych w objawowym leczeniu chorób układu oddechowego przebiegających z nadmiernym wytwarzaniem gęstej i lepkiej wydzieliny oskrzelowej jest karbocysteina. Cząsteczka tego kwasowego aminokwasu, zbudowana jest z reszty cząsteczki cysteiny oraz reszty cząsteczki kwasu etanowego połączonych za pośrednictwem atomu siarki. Inną pochodną cysteiny o zbliżonym do karbocysteiny działaniu leczniczym jest związek chemiczny o nazwie N-acetylocysteina, w cząsteczkach której rozróżnia się wiązanie amidowe. Wodne roztwory N-acetylocysteiny mają od-czyn kwasowy.
Na podstawie: D. Steinhilber i inni, Chemia medyczna. Cele leków, substancje czynne, biologia chemiczna, Wrocław 2012.
Narysuj wzór półstrukturalny (grupowy) cząsteczki karbocysteiny, a następnie określ liczbę atomów węgla w jej cząsteczce, których orbitalom walencyjnym można przypisać hybrydyzację typu sp3. Wzór cząsteczki karbocysteiny: Liczba atomów węgla o hybrydyzacji sp3: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Rysowanie wzorów grupowych cząsteczek oraz jonów powstałych w wyniku hydrolizy kwasowej oraz zasadowej N-acetylocysteiny
Substancją czynną wchodzącą w skład leków stosowanych w objawowym leczeniu chorób układu oddechowego przebiegających z nadmiernym wytwarzaniem gęstej i lepkiej wydzieliny oskrzelowej jest karbocysteina. Cząsteczka tego kwasowego aminokwasu, zbudowana jest z reszty cząsteczki cysteiny oraz reszty cząsteczki kwasu etanowego połączonych za pośrednictwem atomu siarki. Inną pochodną cysteiny o zbliżonym do karbocysteiny działaniu leczniczym jest związek chemiczny o nazwie N-acetylocysteina, w cząsteczkach której rozróżnia się wiązanie amidowe. Wodne roztwory N-acetylocysteiny mają od-czyn kwasowy.
Na podstawie: D. Steinhilber i inni, Chemia medyczna. Cele leków, substancje czynne, biologia chemiczna, Wrocław 2012.
Narysuj wzory półstrukturalne cząsteczek oraz jonów organicznych produktów powstałych w wyniku hydrolizy kwasowej oraz hydrolizy zasadowej N-acetylocysteiny. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone