22.10.2025 | 0 komentarze
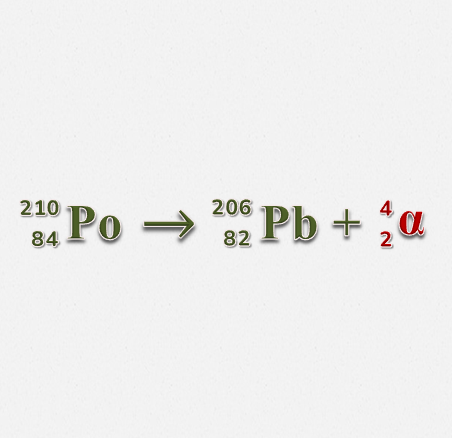
Naturalnymi rozpadami promieniotwórczymi nazywamy procesy przebiegające w obrębie jąder atomowych. Ulega im wiele tzw. radioizotopów, czyli takich atomów, które są promieniotwórcze. Jedną z przemian jądrowych, której znajomość obowiązuje Cię na maturze z chemii jest rozpad α (alfa). Podczas takiego procesu emitowane jest jądro nuklidu helu zawierające 2 protony oraz 2 neutrony. W równaniach reakcji jądrowych drobinę taką można zapisać symbolami:
![]()
Jak zatem wygląda równanie rozpadu promieniotwórczego, prowadzącego do powstania cząstki α? Przede wszystkim należy pamiętać, że jest to równanie REAKCJI JĄDROWEJ, a nie reakcji chemicznej (o czym za chwilę). Za przykład może posłużyć rozpad promieniotwórczego izotopu polonu-210:
![]()
Tutaj u części z Was zapewne rodzi się pytanie: no dobrze – skoro cząstka alfa jest drobiną zawierającą protony oraz neutrony, to w takim razie co z jej elektronami? Odpowiedź jest prosta: cząstka α to dwudodatni kation izotopu helu-4, zatem elektronów nie ma tam w ogóle! Drobinę taką można zatem zapisać również wzorem: 4He2+.
W tym momencie pojawia się kolejne pytanie: czy zapisane wyżej równanie rozpadu promieniotwórczego polonu-210 jest poprawne, skoro po prawej jego stronie pojawia się kation? Tutaj odpowiedź jest bardziej złożona – musimy najpierw wyjaśnić jaka jest różnica między reakcją jądrową, a reakcją chemiczną…
Czym jest reakcja jądrowa?
Podczas takiego procesu zmianom podlega skład jądra atomowego – liczba protonów oraz neutronów. Powstają wówczas inne pierwiastki chemiczne. Elektrony z powłok nie biorą wtedy udziału w reakcji jądrowej – ich liczba nie zmienia się.
Co dzieje się podczas reakcji chemicznej?
W tym przypadku to skład jądra atomowego pozostaje niezmienny, a w trakcie przebiegu procesu może (choć nie musi) zmieniać się skład powłok walencyjnych atomów. Dlatego reakcją chemiczną jest na przykład proces utleniania cynku (oddającego elektrony) kationom wodoru (H+):
Zn + 2H+ → Zn2+ + H2
Co oznaczają wartości liczbowe przy symbolach pierwiastków w równaniu reakcji jądrowej?
W równaniu reakcji jądrowej zapisujemy wartości – liczby masowej (A), u góry po lewej stronie symbolu pierwiastka oraz liczby atomowej (Z), u dołu po lewej stronie. W przypadku wspomnianego izotopu polonu-210 są to odpowiednio A = 210 oraz Z = 84. W równaniach reakcji jądrowych wartości A oraz Z odnoszą się wyłącznie do składu jądra atomowego, zatem pod liczbą atomową nie kryją się wtedy elektrony. Dlaczego? Ponieważ elektrony nie biorą udziału w reakcji jądrowej – znajdują się w powłokach walencyjnych, zatem nie należą do jądra atomowego. W równaniach reakcji chemicznych natomiast nie uwzględnia się zmian składu jądra atomowego, ponieważ takie zmiany nie mają wtedy miejsca. Zatem w równaniach reakcji chemicznych nie podajemy wartości liczb masowych i atomowych nuklidów, pierwiastków chemicznych.
Pozostaje jeszcze do wyjaśnienia jedna kwestia – skąd po przemianie alfa, w powietrzu pojawiają się elektrycznie obojętne atomy helu?Jony He2+ (cząstki α) oddziałują z materią jaka je otacza – przyłączając kolejno dwa elektrony, co w efekcie prowadzi do powstania atomów izotopu helu-4:
He2+ + ē → He+
następnie
He+ + ē → He
Teraz już nie tylko wiesz , że cząstka alfa jest kationem, ale również znasz podstawową różnicę między reakcją chemiczną i jądrową oraz sposobami ich opisu odpowiednimi równaniami…
Spodobał Ci się ten artykuł? Polub mój fanpage na Facebooku oraz na Instagramie, aby nie ominęły Cię żadne nowości.
© dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone