Obliczanie zmiany masy blaszki do momentu 5-krotnego zmniejszenia się stężenia jonów srebra
W kolbie umieszczono 200 cm3 roztworu azotanu(V) srebra zawierającego 1,7 g substancji rozpuszczonej. W roztworze tym zanurzono blaszkę wykonaną z ołowiu.
Na podstawie niezbędnych obliczeń ustal, o ile miligramów zmieniła się masa blaszki do momentu, w którym stężenie jonów Ag+ zmalało 5-krotnie? Rozwiązanie tego zadania dostępne jest nieodpłatnie pod poniższym linkiem: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Ocena, czy masa manganowej blaszki uległa zwiększeniu, czy zmniejszeniu (blaszki)
W wodnym roztworze chlorku kobaltu(II) zanurzono blaszkę wykonaną z manganu. Po zakończeniu reakcji chemicznej stwierdzono, że jej masa uległa zmianie.
Oceń, czy masa blaszki uległa zwiększeniu, czy zmniejszeniu? Odpowiedź uzasadnij odpowiednimi obliczeniami. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wskazanie probówek, w których masa blaszki uległa zwiększeniu po wprowadzeniu do roztworu soli niklu (blaszki)
Do czterech probówek zawierających kolejno blaszki: kadmową, miedzianą, cynkową oraz srebrną dodano wodnego roztworu NiSO4, który ma barwę zieloną.
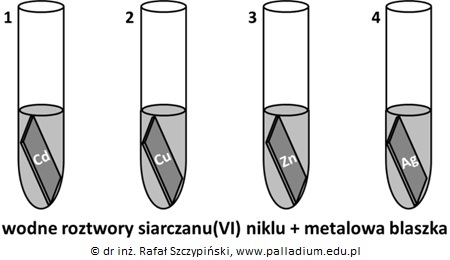
Po zakończeniu doświadczenia stwierdzono, że masy niektórych blaszek uległy zmianie.
Podaj numery tych probówek, w których masa blaszek uległa zwiększeniu. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wskazanie probówek, w których nie zaobserwowano objawów reakcji po wprowadzeniu blaszki do roztworu soli niklu (blaszki)
Do czterech probówek zawierających kolejno blaszki: kadmową, miedzianą, cynkową oraz srebrną dodano wodnego roztworu NiSO4, który ma barwę zieloną.

Wymień numery tych probówek, w których nie zaobserwowano objawów świadczących o przebiegu reakcji chemicznej oraz napisz, co zaobserwowano w probówkach, w których reakcja przebiegła? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wypieranie metalu z roztworu soli za pomocą innego metalu, skład procentowy blaszki
W roztworze azotanu(V) bizmutu(III) o objętości równej 200 cm3 zanurzono płytkę niklową o masie 29,5 g. Po całkowitym usunięciu jonów Bi3+ z roztworu stwierdzono, że masa płytki wynosi 32 g.
Określ w procentach masowych skład płytki po zakończeniu reakcji. Wyniki obliczeń podaj z dokładnością do pierwszego miejsca po przecinku. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie liczby atomów kobaltu osadzonych na blaszce (blaszki)
W wodnym roztworze chlorku kobaltu(II) zanurzono blaszkę wykonaną z manganu. Po zakończeniu reakcji chemicznej stwierdzono, że jej masa zmieniła się o 20 mg.
Oblicz, ile miligramów jonów manganu(II) pojawiło się w roztworze oraz ile atomów kobaltu osadziło się na blaszce? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie, jaki procent jonów został usunięty z roztworu (blaszki)
W 100 cm3 roztworu siarczanu(VI) miedzi(II) o stężeniu 0,5 mol∙dm–3 zanurzono płytkę niklową o masie równej 5 g. W układzie przebiegła reakcja chemiczna opisana równaniem:
Ni + Cu2+ → Ni2+ + Cu
Po jej zakończeniu płytkę przemyto wodą dejonizowaną, wysuszono i zważono. Stwierdzono, że jej masa wynosi 5,125 g.
Oblicz, jaki procent jonów miedzi(II) został usunięty z roztworu? Przyjmij, że masa mola atomów niklu wynosi 59 g, a miedzi 64 g. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie o ile procent zmienia się masa blaszki po usunięciu wszystkich jonów z roztworu (blaszki)
W 100 cm3 roztworu siarczanu(VI) miedzi(II) o stężeniu 0,5 mol∙dm–3 zanurzono płytkę niklową o masie równej 5 g. W układzie przebiegła reakcja chemiczna opisana równaniem:
Ni + Cu2+ → Ni2+ + Cu
Po jej zakończeniu płytkę przemyto wodą dejonizowaną, wysuszono i zważono. Stwierdzono, że jej masa wynosi 5,125 g.
Oblicz, o ile procent zwiększyłaby się masa wyjściowej blaszki, gdyby z roztworu usunięte zostały wszystkie jony Cu2+? Przyjmij, że masa mola atomów niklu wynosi 59 g, a miedzi 64 g. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wypieranie metalu z roztworu soli za pomocą innego metalu (blaszki), obliczanie stężenia molowego
W zlewce umieszczono 50 cm3 roztworu azotanu(V) srebra i zanurzono w nim blaszkę cynkową. Po 24 godzinach blaszkę wyjęto, przemyto i wysuszono. Po jej zważeniu stwierdzono przyrost masy równy 3,02 g.
Wiedząc, że całe srebro zostało usunięte z roztworu oblicz stężenie molowe jonów azotanowych(V). Wynik podaj z dokładnością do jednego miejsca po przecinku. Przyjmij, że objętość roztworu przed i po zakończeniu doświadczenia była taka sama. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wypieranie metalu z roztworu soli za pomocą innego metalu (blaszki), obliczanie stężenia molowego
W roztworze azotanu(V) bizmutu(III) o objętości równej 200 cm3 zanurzono płytkę niklową o masie 29,5 g. Po całkowitym usunięciu jonów Bi3+ z roztworu stwierdzono, że masa płytki wynosi 32 g.
Oblicz, jakie było stężenie jonów bizmutu(III) przed reakcją oraz jakie było stężenie jonów niklu(II) po jej zakończeniu? Wyniki obliczeń podaj z dokładnością do trzeciego miejsca po przecinku. Przyjmij, że objętość roztworu przed i po zakończeniu doświadczenia była taka sama. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie stężenia molowego roztworu azotanu(V) srebra użytego do posrebrzenia przedmiotu (blaszki)
W celu poprawienia estetyki, przedmioty wykonane z żelaza pokrywa się cienką warstwą metalicznego srebra, czemu towarzyszy przebieg reakcji chemicznej opisanej równaniem:
Fe + 3Ag+ → Fe3+ + 3Ag
W wodnym roztworze azotanu(V) srebra o objętości równej 485 cm3 całkowicie zanurzono żelazny przedmiot o masie 20 g.
Oblicz, jakie powinno być stężenie molowe opisanego roztworu azotanu(V) srebra, aby osadzone srebro stanowiło dokładnie 5% masy posrebrzonego nim przedmiotu? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zapis schematu ogniwa cynkowo-ołowiowego oraz obliczanie wartości jego SEM w stanie standardowym
Zbudowano ogniwo chemiczne z wykorzystaniem dwóch półogniw. W pierwszym z nich blaszka cynkowa zanurzona została w roztworze ZnSO4, a w drugim blaszka ołowiana w roztworze Pb(NO3)2.
Uzupełnij poniższy schemat ogniwa według tzw. konwencji sztokholmskiej, a następnie oblicz wartość siły elektromotorycznej tego ogniwa w stanie standardowym. anoda (–) || (+) katoda SEM: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone