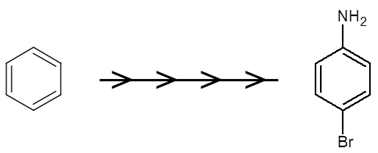
Zapis równań reakcji chemicznych na podstawie przeprowadzonego eksperymentu z udziałem proszku do pieczenia
W skład proszku do pieczenia wchodzą zwykle dwa związki chemiczne – wodorowęglan sodu (soda oczyszczona) lub wodorowęglan amonu (tzw. amoniak do pieczenia). W temperaturze wypieku równej 180 oC oba rozkładają się z wydzieleniem gazowych produktów, przy czym podczas rozkładu sody oczyszczonej powstaje dodatkowo związek chemiczny o stałym stanie skupienia, zawierający 43,4% sodu.
Do wypieku 600 g ciasta (1000 hPa) wykorzystano 15 g wodorowęglanu amonu. Gazowe produkty reakcji jego rozkładu spowodowały spulchnienie ciasta.
Napisz równania reakcji chemicznych w wyniku przebiegu których powstały związki chemiczne, które spowodowały spulchnienie ciasta, w zależności od zastosowanego proszku do pieczenia. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Równanie reakcji chemicznej soli kwasu węglowego z kwasem azotowym(V)
Na minerał zawierający po 0,1 mola każdego z węglanów: baru, srebra oraz wapnia podziałano stechiometryczną ilością stężonego roztworu kwasu azotowego(V). Zawartość naczynia ogrzewano, a po ochłodzeniu uzupełniono wodą do wyjściowej objętości roztworu.
Napisz w formie jonowej skróconej równanie przebiegającej reakcji chemicznej. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zapis równania reakcji hydrolizy siarczku glinu
Wiele soli nie istnieje w postaci wodnych roztworów, ponieważ w odpowiednich warunkach ulegają praktycznie nieodwracalnej reakcji hydrolizy.
Do wody destylowanej wprowadzono próbkę siarczku glinu i zaobserwowano zmętnienie zawartości naczynia oraz wydzielenie się gazu o charakterystycznym zapachu zgniłych jaj.
Napisz równanie reakcji chemicznej jaka przebiegła. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wybór odczynników pozwalających odróżnić mieszaniny poreakcyjne uzyskane po reakcji węglików z wodą
Niektóre węgliki w reakcji z wodą mogą posłużyć do laboratoryjnego (na niewielką skalę) otrzymywania pewnych gazowych węglowodorów. W dwóch różnych zlewkach umieszczono karbid (CaC2) oraz węglik glinu (Al4C3) i ostrożnie wprowadzano do nich wodę. Po pewnym czasie stwierdzono, że z naczyń nie wydzielają się już substancje gazowe, a uzyskane układy są białymi zawiesinami wodorotlenków.
Spośród odczynników: HCl(aq), alkoholowy roztwór fenoloftaleiny, NaNO3(aq), KOH(aq), CuSO4(aq) wybierz takie dwa, które pozwolą na odróżnienie uzyskanych mieszanin poreakcyjnych. Odpowiedź uzasadnij równaniami odpowiednich procesów zapisanymi w formie jonowej (lub jonowej skróconej) oraz obserwacjami. Pierwszy odczynnik oraz uzasadnienie: Drugi odczynnik oraz uzasadnienie: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zapis równań reakcji chemicznych prowadzących do uzyskania zanieczyszczonego siarkowodoru
Handlowy siarczek żelaza(II) otrzymuje się w wyniku stapiania opiłków żelaza z siarką. Związek ten bywa zanieczyszczony jednym z substratów opisanej przemiany i wyko-rzystywany jest między innymi do otrzymywania siarkowodoru. Reakcję prowadzi się wówczas w aparacie Kippa z udziałem kwasu solnego, przy czym powstały produkt gazowy zwykle zanieczyszczony jest wtedy najlżejszym znanym nam gazem.
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2010.
Napisz w formie jonowej skróconej równania dwóch zachodzących w aparacie Kippa reakcji chemicznych, prowadzących do uzyskania zanieczyszczonego siarkowodoru. 1. 2. Rozwiązanie tego zadania dostępne jest nieodpłatnie pod poniższym linkiem: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Otrzymywanie 3-metylopentanu z węglanu wapnia oraz innych substancji w wieloetapowym procesie
3-metylopentan można otrzymać w kilku etapach reakcyjnych, stosując jako wyjściowy substrat węglan wapnia, według ogólnego schematu:
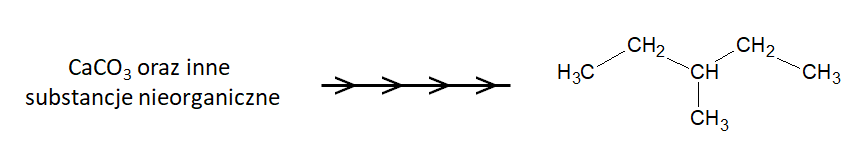
Mając do dyspozycji wymieniony substrat oraz inne substancje nieorganiczne, zaprojektuj ciąg syntez chemicznych, którego celem będzie otrzymanie 3-metylopentanu. Zapisz równania przebiegających reakcji chemicznych uwzględniając jedynie oczekiwane ich produkty organiczne i nieorganiczne oraz uwzględnij warunki prowadzenia procesów. W kolejnych etapach możesz skorzystać z uzyskanych wcześniej związków organicznych. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Otrzymywanie 2,3-dimetylobutanu z glicerolu w wieloetapowym procesie reakcyjnym
Gliceryna jest popularnym w chemii kosmetyków związkiem nawilżającym. Substancja taka może jednak również stanowić wyjściowy substrat w wielu syntezach organicznych, na przykład – w celu uzyskania alkanu o nazwie 2,3-dimetylobutan:
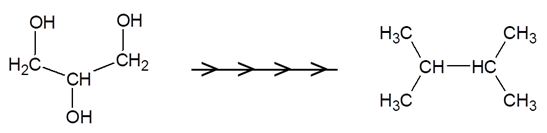
Wychodząc od gliceryny i mając do dyspozycji jeszcze dowolne substancje nieorganiczne, zaprojektuj ciąg syntez chemicznych, którego celem będzie otrzymanie opisanego alkanu. Zapisz równania przebiegających reakcji chemicznych uwzględniając jedynie oczekiwane ich produkty organiczne i nieorganiczne oraz uwzględnij warunki prowadzenia procesów. W kolejnych etapach możesz skorzystać z uzyskanych wcześniej związków organicznych. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Otrzymywanie mrówczanu metylu z gazu syntezowego oraz innych substancji w wieloetapowym procesie
Gaz syntezowy może posłużyć jako substrat wyjściowy do produkcji wielu związków organicznych. Z mieszaniny takiej można na przykład uzyskać w wieloetapowym procesie reakcyjnym ester o nazwie mrówczan metylu, co ilustruje schemat:
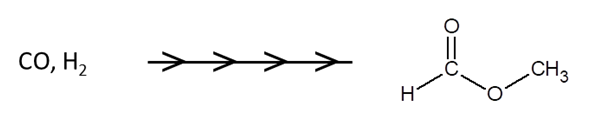
Mając do dyspozycji wymienione substraty oraz inne substancje nieorganiczne, zaprojektuj ciąg syntez chemicznych, którego celem będzie otrzymanie mrówczanu metylu. Zapisz równania przebiegających reakcji chemicznych uwzględniając jedynie oczekiwane ich produkty organiczne i nieorganiczne oraz uwzględnij warunki prowadzenia procesów. W kolejnych etapach możesz skorzystać z uzyskanych wcześniej związków organicznych. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wskazanie symboli pierwiastków chemicznych oraz ich położenia w układzie okresowym. Zadanie 1.1. Arkusz CKE chemia maj 2018 rozszerzony (1 punkt)
Pierwiastki X i Z leżą w czwartym okresie układu okresowego. Pierwiastek X jest metalem, natomiast pierwiastek Z – niemetalem. W stanie podstawowym atomów obu tych pierwiastków tylko jeden elektron jest niesparowany. Znajduje się on na ostatniej powłoce. Niesparowany elektron atomu pierwiastka X znajduje się na innej podpowłoce niż niesparowany elektron atomu pierwiastka Z. Ponadto wiadomo, że pierwiastek X tworzy tlenki o wzorach X2O i XO oraz że ten metal jest jednym z najlepszych przewodników ciepła i elektryczności. Pierwiastek Z występuje w postaci dwuatomowych cząsteczek.
Uzupełnij poniższą tabelę. Wpisz symbole pierwiastków X i Z, dane dotyczące ich położenia w układzie okresowym oraz symbol bloku konfiguracyjnego, do którego należy każdy z pierwiastków.
Zapis konfiguracji elektronowej dwudodatniego jonu. Zadanie 1.2. Arkusz CKE chemia maj 2018 rozszerzony (1 punkt)
Pierwiastki X i Z leżą w czwartym okresie układu okresowego. Pierwiastek X jest metalem, natomiast pierwiastek Z – niemetalem. W stanie podstawowym atomów obu tych pierwiastków tylko jeden elektron jest niesparowany. Znajduje się on na ostatniej powłoce. Niesparowany elektron atomu pierwiastka X znajduje się na innej podpowłoce niż niesparowany elektron atomu pierwiastka Z. Ponadto wiadomo, że pierwiastek X tworzy tlenki o wzorach X2O i XO oraz że ten metal jest jednym z najlepszych przewodników ciepła i elektryczności. Pierwiastek Z występuje w postaci dwuatomowych cząsteczek.
Przedstaw konfigurację elektronową jonu X2+ (stan podstawowy). Zastosuj skrócony zapis konfiguracji elektronowej z symbolem gazu szlachetnego.