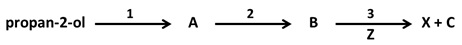Wyjaśnienie dużej różnicy w temperaturach wrzenia alkoholu oraz izomerycznego z nim nadtlenku organicznego
W wodnym 10,3-procentowym roztworze pewnego nasyconego alkoholu na jedną jego cząsteczkę przypada trzydzieści cząsteczek wody. Związek ten roztwarza świeżo strącony osad wodorotlenku miedzi(II) z utworzeniem szafirowego klarownego roztworu. Temperatura wrzenia opisanego alkoholu pod ciśnieniem normalnym wynosi 470 K. Przy identycznej wartości ciśnienia, jeden z jego izomerów wrze w temperaturze 287 K i należy do szeregu homologicznego tzw. nadtlenków organicznych, czyli związków chemicznych o wzorze ogólnym w postaci R1–O–O–R2. We wzorze tym R1 oraz R2 stanowią reszty cząsteczek tego samego, bądź różnych węglowodorów.
Na podstawie: www.pubchem.com oraz W. Mizerski, Tablice chemiczne, Warszawa 2013.
Wyjaśnij, czym spowodowana jest tak duża różnica w wartościach temperatur wrzenia wymienionych izomerycznych związków chemicznych? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
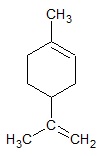
Rysowanie wzoru półstrukturalnego trans-1,2-difenyloetylenu na podstawie jego nazwy (izomeria geometryczna)
Difenyloacetylen można otrzymać w dwuetapowym procesie:
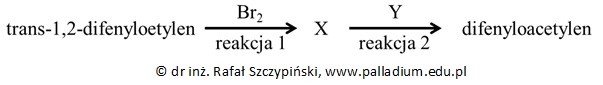
Narysuj wzór półstrukturalny (grupowy) trans-1,2-difenyloetylenu. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Bilansowanie równania reakcji nadtlenku wodoru z manganianem(VII) potasu w środowisku obojętnym
Do wodnego roztworu manganianu(VII) potasu dodano roztwór zawierający stechiometryczną względem KMnO4 ilość nadtlenku wodoru. Zaobserwowano dwie zmiany świadczące o przebiegu reakcji chemicznej. Ponadto roztwór tylko nieznaczenie uległ odbarwieniu.
Napisz, jakie dwie zmiany (poza nieznacznym odbarwieniem roztworu) odnotowano? Odpowiedź uzasadnij równaniem reakcji chemicznej zapisanym w formie jonowej skróconej. Współczynniki uzgodnij metodą bilansu jonowo-elektronowego. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Przypisywanie modelu hybrydyzacji atomom węgla w cząsteczce difenyloacetylenu oraz określanie liczby wiązań σ oraz π w cząsteczce węglowodoru
Difenyloacetylen można otrzymać w dwuetapowym procesie:
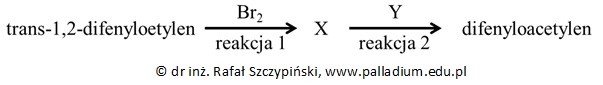
Określ typ hybrydyzacji (sp, sp2, sp3) jaką można przypisać orbitalom walencyjnym alifatycznych atomów węgla w cząsteczce difenyloacetylenu. Podaj liczbę wiązań σ oraz liczbę wiązań π znajdujących się w cząsteczce tego węglowodoru. Typ hybrydyzacji: ……….. Liczba wiązań σ: ……….. Liczba wiązań π: ……….. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wybór trwalszego spośród dwóch izomerycznych alkoholi zawierających cztery atomy węgla w cząsteczce
Trwałość alkoholi polihydroksylowych zależy od liczby grup –OH połączonych z tym samym atomem węgla w cząsteczce. Najtrwalsze są te alkohole, w cząsteczkach których dany atom węgla połączony jest z maksymalnie jedną grupą hydroksylową.
Rysunek poniżej przedstawia wzory grupowe dwóch wybranych izomerycznych związków chemicznych oznaczonych umownie literami A oraz B.
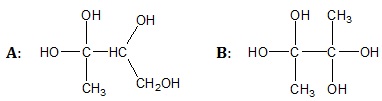
Podaj oznaczenie literowe (A lub B) trwalszego spośród wymienionych związków chemicznych oraz napisz jego nazwę systematyczną. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Reakcja nadtlenku wodoru ze stechiometryczną ilością manganianu(VII) potasu - wyjaśnienie braku całkowitego odbarwienia roztworu
Do wodnego roztworu manganianu(VII) potasu dodano roztwór zawierający stechiometryczną względem KMnO4 ilość nadtlenku wodoru. Zaobserwowano dwie zmiany świadczące o przebiegu reakcji chemicznej. Ponadto roztwór tylko nieznaczenie uległ odbarwieniu.
Wyjaśnij, dlaczego roztwór nie odbarwił się całkowicie? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zapis równania reakcji chemicznej otrzymywania difenyloacetylenu na podstawie schematu oraz określanie typu reakcji chemicznej
Difenyloacetylen można otrzymać w dwuetapowym procesie:
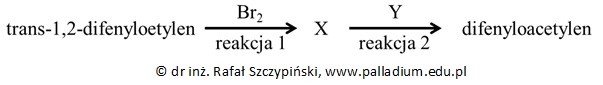
Napisz z wykorzystaniem półstrukturalnych (grupowych) wzorów związków organicznych równanie reakcji chemicznej oznaczonej numerem 2. Uwzględnij warunki (Y) prowadzenia tej reakcji i określ jej typ podkreślając odpowiedni wyraz w nawiasie: (addycja/substytucja/eliminacja). © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określanie wzoru rzeczywistego oraz półstrukturalnego najtrwalszego izomeru alkoholu na podstawie znajomości stężeń jego roztworu
Trwałość alkoholi polihydroksylowych zależy od liczby grup –OH połączonych z tym samym atomem węgla w cząsteczce. Najtrwalsze są te alkohole, w cząsteczkach których dany atom węgla połączony jest z maksymalnie jedną grupą hydroksylową.
Pewien związek chemiczny zawierający jedynie hydroksylowe grupy funkcyjne tworzy 7,5-molowy wodny roztwór o gęstości 1,15 g∙cm–3 i stężeniu procentowym równym 60%. W jego cząsteczkach stosunek liczby atomów węgla do liczby atomów tlenu równy jest 1.
Wykonaj niezbędne obliczenia, a następnie narysuj wzór półstrukturalny oraz podaj nazwę systematyczną opisanego alkoholu, wiedząc, że jest on najtrwalszym spośród jego izomerów. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Rysowanie półstrukturalnego wzoru mniej trwałego spośród izomerów geometrycznych oraz wyjaśnienie przyczyny istnienia izomerów geometrycznych (izomeria geometryczna)
Trwałość izomerów geometrycznych zależy od tzw. oddziaływania przestrzennego (sterycznego) między dwoma objętościowymi podstawnikami po tej samej stronie wiązania podwójnego. Im oddziaływanie to jest silniejsze (podstawniki zajmują więcej miejsca w przestrzeni), tym izomer wykazuje mniejszą trwałość.
Na podstawie: J. McMurry, Chemia organiczna, Warszawa 2012.
Przykładem węglowodoru, który występuje w postaci izomerów geometrycznych jest związek chemiczny o nazwie 3-metylopent-2-en.
Narysuj wzór półstrukturalny (grupowy) mniej trwałego wśród izomerów geometrycznych węglowodoru, którego nazwę systematyczną podano w informacji wprowadzającej, a następnie wyjaśnij, dlaczego 3-metylopent-2-en może występować w postaci izomerów geometrycznych cis-trans? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wskazanie czynnego optycznie produktu reakcji chemicznej oraz uzasadnienie, czy jest to produkt główny, czy uboczny (izomeria optyczna)
Trwałość izomerów geometrycznych zależy od tzw. oddziaływania przestrzennego (sterycznego) między dwoma objętościowymi podstawnikami po tej samej stronie wiązania podwójnego. Im oddziaływanie to jest silniejsze (podstawniki zajmują więcej miejsca w przestrzeni), tym izomer wykazuje mniejszą trwałość.
Na podstawie: J. McMurry, Chemia organiczna, Warszawa 2012.
Przykładem węglowodoru, który występuje w postaci izomerów geometrycznych jest związek chemiczny o nazwie 3-metylopent-2-en.
Jeden z izomerów opisanego węglowodoru o takim samym szkielecie węglowym poddano działaniu bromowodoru. Uzyskano mieszaninę czynnych optycznie związków chemicznych.
Podaj nazwę systematyczną tego produktu, który występuje w postaci diastereoizomerów. Określ, czy jest to główny, czy uboczny produkt przebiegającej reakcji chemicznej. Uzasadnij swoje stanowisko. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone