Zadanie 38. Arkusz Palladium kwiecień 2017 (1 punkt)
Kwas pantotenowy jest jedną z witamin grupy B, a jego cząsteczkę można przedstawić wzorem:
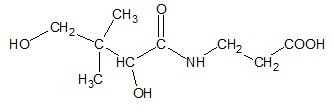
Na podstawie: M. Gumińska, Zarys biochemii ogólnej dla studentów farmacji i analityki medycznej, Kraków 1998.
Pewien białkowy aminokwas X jest izomerem aminokwasu, którego reszta buduje cząsteczkę kwasu pantotenowego.
Narysuj wzór półstrukturalny dominującej w środowisku o pH = 12 postaci aminokwasu X. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Rozszyfrowanie symbolu pierwiastka chemicznego oraz określenie jego położenia w układzie okresowym. Zadanie 1.1. Arkusz CKE chemia maj 2016 rozszerzony (1 punkt)
Z konfiguracji elektronowej atomu (w stanie podstawowym) pierwiastka X wynika, że w tym atomie:
• elektrony rozmieszczone są na czterech powłokach elektronowych
• na podpowłoce 3d liczba elektronów sparowanych jest dwa razy mniejsza od liczby elektronów niesparowanych.
Uzupełnij poniższą tabelę – wpisz symbol pierwiastka X, dane dotyczące jego położenia w układzie okresowym oraz symbol bloku konfiguracyjnego (energetycznego), do którego należy pierwiastek X.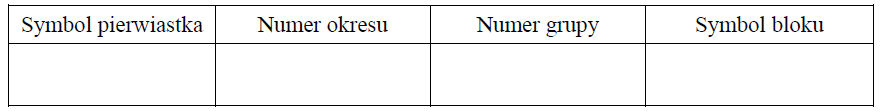
Uzupełnienie schematu klatkowego konfiguracji elektronowej rozszyfrowanego pierwiastka chemicznego. Zadanie 1.2. Arkusz CKE chemia maj 2016 rozszerzony (1 punkt)
Z konfiguracji elektronowej atomu (w stanie podstawowym) pierwiastka X wynika, że w tym atomie:
• elektrony rozmieszczone są na czterech powłokach elektronowych
• na podpowłoce 3d liczba elektronów sparowanych jest dwa razy mniejsza od liczby elektronów niesparowanych.
Uzupełnij poniższy zapis (stosując schematy klatkowe), tak aby przedstawiał on konfigurację elektronową atomu w stanie podstawowym pierwiastka X. W zapisie tym uwzględnij numery powłok i symbole podpowłok. Podkreśl ten fragment konfiguracji, który nie występuje w konfiguracji elektronowej jonu X2+ (stan podstawowy).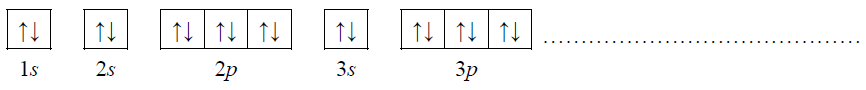
Ocena poprawności zdań dotyczących wapnia oraz potasu. Zadanie 2. Arkusz CKE chemia maj 2016 rozszerzony (1 punkt)
W poniższej tabeli zestawiono wybrane właściwości fizyczne potasu i wapnia.

Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2004.
Oceń, czy podane poniżej informacje są prawdziwe. Zaznacz P, jeśli informacja jest prawdziwa, albo F – jeśli jest fałszywa. 1. Podczas reakcji wapnia i potasu z wodą te metale pływają po powierzchni wody, ponieważ gęstość każdego z nich jest mniejsza od gęstości wody. 2. Atomy wapnia i potasu, oddając elektrony walencyjne, przechodzą w dodatnio naładowane jony o konfiguracji elektronowej tego samego gazu szlachetnego. 3. Atomy wapnia są mniejsze od atomów potasu; dwudodatnie jony wapnia są mniejsze od jednododatnich jonów potasu.
Wybór poprawnych określeń dotyczących wapnia oraz potasu. Zadanie 3. Arkusz CKE chemia maj 2016 rozszerzony (1 punkt)
W poniższej tabeli zestawiono wybrane właściwości fizyczne potasu i wapnia.

Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2004.
Na podstawie informacji i układu okresowego pierwiastków uzupełnij poniższe zdania. Wybierz i zaznacz jedno właściwe określenie spośród podanych w każdym nawiasie. 1. Węzły sieci krystalicznych wapnia, jak i potasu obsadzone są (dodatnio / ujemnie) naładowanymi jonami zwanymi rdzeniami atomowymi. Pomiędzy rdzeniami atomowymi obecne są słabo związane elektrony walencyjne, które mogą wędrować swobodnie przez kryształ metalu. Dlatego zarówno wapń, jak i potas odznaczają się (dużą / małą) przewodnością elektryczną. 2. Temperatura topnienia wapnia jest (niższa / wyższa) niż temperatura topnienia potasu, co wynika między innymi (z silniejszego / ze słabszego) wiązania metalicznego, utworzonego z udziałem (mniejszej / większej) liczby elektronów walencyjnych.