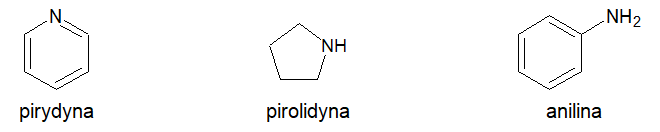
Poniżej przedstawiono wzory chemiczne cząsteczek amin – pirydyny, pirolidyny oraz aniliny.
W tabeli poniżej zebrano informacje na temat wybranych własności fizykochemicznych wymienionych substancji (1013 hPa, 298 K).
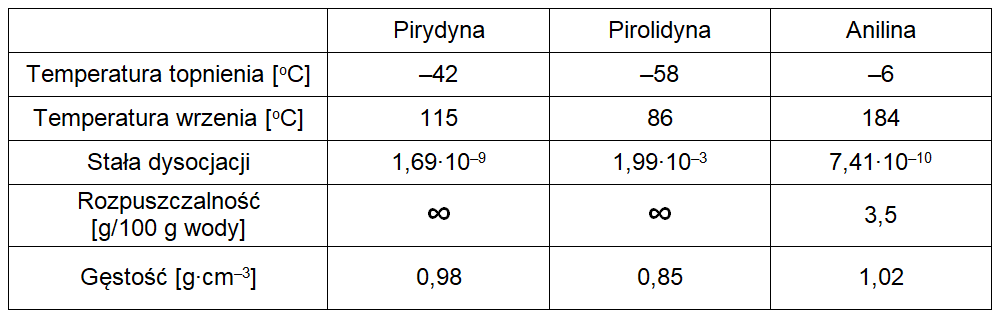
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Miareczkowanie jest metodą stosowaną do ilościowego oznaczania zawartości substancji chemicznej w jej wodnym roztworze. Podczas jego wykonywania, do roztworu analitu o znanej objętości, lecz nieznanym stężeniu, ostrożnie wprowadzany jest znajdujący się w biurecie mianowany (o ściśle określonym stężeniu molowym) roztwór titranta. Charakterystyczny podczas miareczkowania jest tzw. punkt równoważnikowy (PR). Jest to moment, w którym analit przereagował ilościowo z dodanym z biurety titrantem. W przypadku, gdy miareczkuje się roztwór słabego kwasu lub słabej zasady wartość pH w punkcie równoważnikowym może być odpowiednio – wyższa lub niższa niż 7, ponieważ w uzyskanym wówczas roztworze przebiega proces hydrolizy.
Na podstawie: R. Szczypiński, Projektowanie doświadczeń chemicznych. Dla maturzystów i nie tylko, Warszawa 2019.
W temperaturze 25 oC w trzech nieoznakowanych kolbach znajdowały się wodne roztwory opisanych amin o stężeniu molowym równym nasyconemu w tych warunkach roztworowi aniliny. Wykonano miareczkowanie 60 cm3 każdego z roztworów, a jako titrant zastosowano roztwór kwasu solnego. Ustalono wówczas, że w punktach równoważnikowych uzyskano roztwory o następujących wartościach pH:
PR1: 6,0 PR2: 2,9 PR3: 2,8
W celu wykonania miareczkowań opisanych roztworów amin wykorzystano pewne wskaźniki kwasowo-zasadowe, które znajdują się wśród niżej podanych:
fenoloftaleina, błękit bromotymolowy, czerwień krezolowa, oranż metylowy, błękit Nilu.
Przypisz odpowiedni wskaźnik kwasowo-zasadowy wykorzystany podczas miareczkowania roztworu danej aminy. Uzupełnij tabelę.

© dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone