W analizie potencjometrycznej wykorzystuje się zależność potencjału odpowiednich elektrod od stężenia jonów oznaczanych. Pomiary potencjometryczne polegają na mierzeniu SEM ogniwa zestawionego z dwóch półogniw: tzw. elektrody wskaźnikowej, zanurzonej w badanym roztworze, oraz tzw. elektrody odniesienia, zanurzonej w roztworze o niezmiennym składzie, której potencjał w warunkach pomiaru pozostaje stały.
Rozróżnia się dwa główne typy elektrod. Elektrody pierwszego rodzaju to elektrody odwracalne względem kationu: są zbudowane z metalu i są w równowadze z roztworem zawierającym jony tego metalu (M oznacza symbol metalu):
M(s) ⇄ Mn+(aq) + nē
Elektrody drugiego rodzaju są odwracalne względem anionu, tworzącego z metalem elektrody trudno rozpuszczalny związek. Elektrodą drugiego rodzaju jest elektroda halogenosrebrowa. Działanie tej elektrody opisuje równanie (X oznacza symbol halogenu):
AgX(s) + ē ⇄ Ag(s) + X–(aq)
Na podstawie: W. Szczepaniak, Metody instrumentalne w analizie chemicznej, Warszawa 2008 oraz A. Skoog, D.M. West, F.J. Holler, S.R. Crouch, Podstawy chemii analitycznej, Warszawa 2007.
Przykładem elektrody halogenosrebrowej jest elektroda chlorosrebrowa:
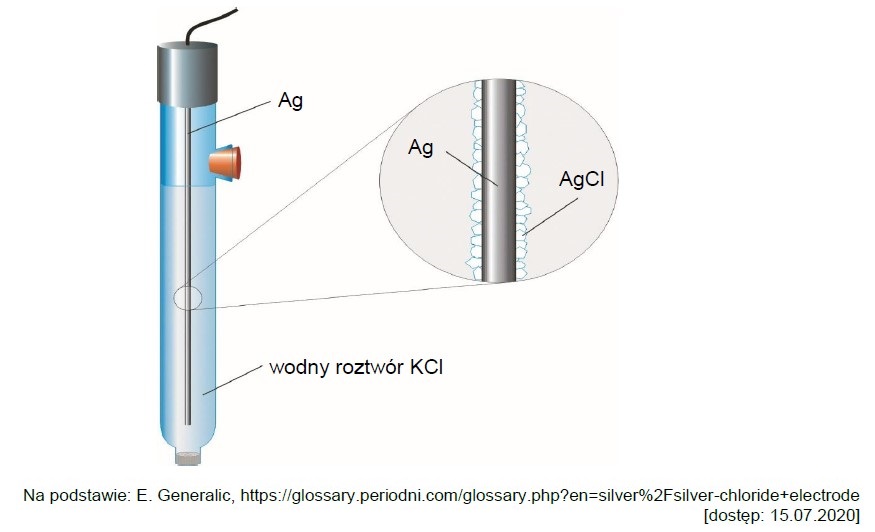
Działanie elektrody chlorosrebrowej opisuje równanie:
AgCl(s) + ē ⇄ Ag(s) + Cl–(aq)
Potencjał tej elektrody zależy od stężenia jonów chlorkowych w roztworze, który stanowi jej element, i wyraża się równaniem:
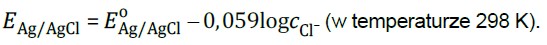
Przygotowano dwie elektrody chlorosrebrowe: elektroda I zawierała wodny roztwór chlorku potasu o stężeniu równym 0,10 mol ∙dm–3, a elektroda II – wodny roztwór tej samej soli o stężeniu równym 0,01 mol ∙dm–3.
Rozstrzygnij, która elektroda chlorosrebrowa (I czy II) ma – w tej samej temperaturze – wyższy potencjał. Odpowiedź uzasadnij.
Rozstrzygnięcie:
Uzasadnienie: