Reakcja metanu z dwutlenkiem węgla przebiega zgodnie z równaniem chemicznym:
CH4(g) + CO2(g) ⇄ 2CO(g) + 2H2(g)
W pozbawionym powietrza, szczelnie zamykanym reaktorze o pojemności 10 dm3 umieszczono 22 cm3 „suchego lodu” (stały CO2) o gęstości 1,2 g·cm–3. Następnie w warunkach normalnych odmierzono 6,72 dm3 metanu i przepompowano go do tego samego reaktora, co „suchy lód”. Po całkowitym przesublimowaniu dwutlenku węgla, w pewnych warunkach ciśnienia i temperatury zainicjowano reakcję chemiczną, która przebiegła z 60% wydajnością, co do wartości równą stopniu przereagowania substratu użytego w niedomiarze. W układzie ustaliła się wówczas równowaga dynamiczna, przedstawiona wyżej opisanym równaniem stechiometrycznym.
W pewnych warunkach ciśnienia i temperatury przeprowadzono reakcję metanu z tlenkiem węgla(IV). Po osiągnięciu pierwszego stanu równowagi t, w układzie zwiększono temperaturę mieszaniny równowagowej, co po pewnym czasie poskutkowało ustaleniem się drugiego stanu równowagi. Na załączonym schemacie przedstawiono zmiany liczb moli tlenków węgla stanowiących reagenty podczas opisanego doświadczenia.
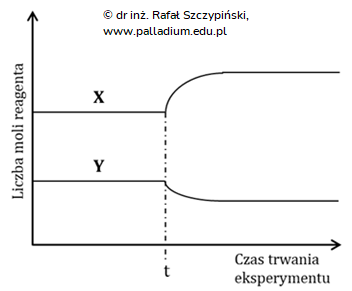
Oznaczeniom literowym X oraz Y przypisz wzory sumaryczne odpowiednich tlenków, a następnie oceń, czy opisanej reakcji chemicznej towarzyszy emisja energii cieplnej z układu do otoczenia. Uzasadnij odpowiedź.
Wzór sumaryczny reagenta X:
Wzór sumaryczny reagenta Y:
Odpowiedź:
Uzasadnienie:
© dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone