Zadanie problemowe. Uzupełnienie tabeli, rysowanie wykresu oraz obliczanie stężenia molowego drobin. Zadanie 8. Arkusz CKE chemia maj 2023 rozszerzony (4 punkty)
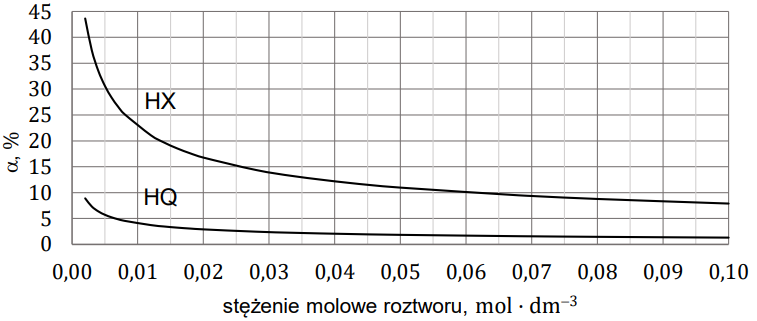
W wodnych roztworach słabych kwasów jednoprotonowych zachodzi dysocjacja. Dla danej wartości stężenia molowego roztworu i w danej temperaturze ustala się stan równowagi między cząsteczkami i jonami obecnymi w roztworze. Na poniższym wykresie przedstawiono zależność stopnia dysocjacji (a) dwóch kwasów jednoprotonowych HX i HQ od stężenia molowego roztworu w temperaturze 20 °C.
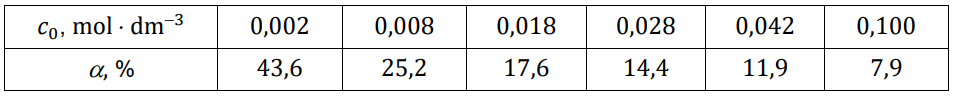
Wartości stopnia dysocjacji kwasu HX dla wybranych stężeń molowych (𝑐0) zebrano w tabeli (𝑡 = 20 °C).
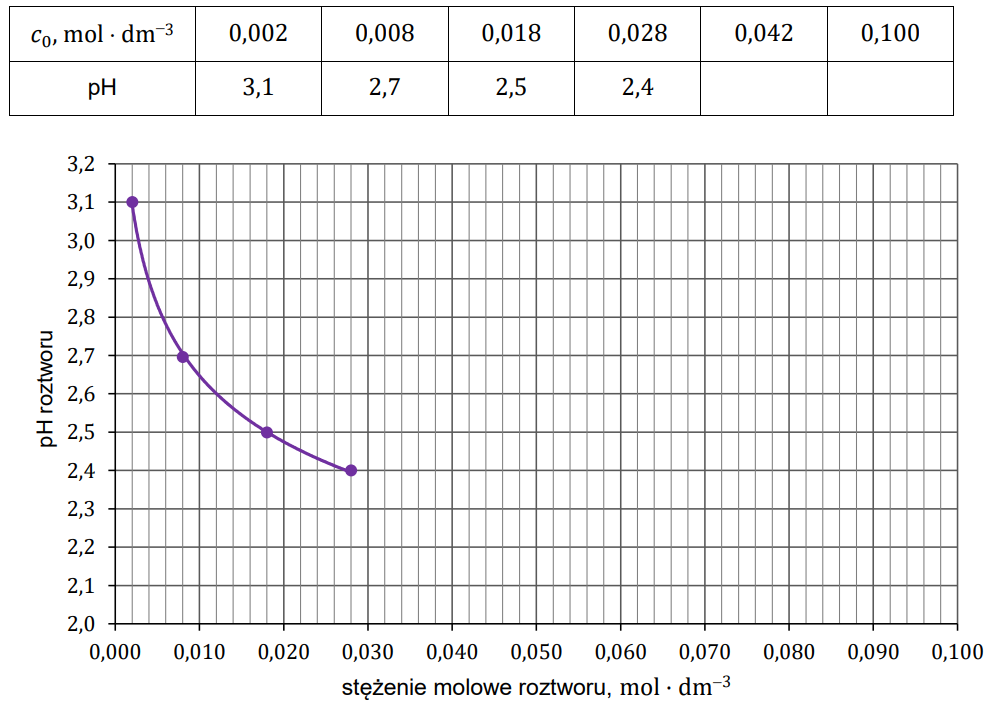
W poniższej tabeli umieszczono wartości pH czterech roztworów kwasu HX o wybranych stężeniach molowych, a na wykresie przedstawiono logarytmiczną zależność pH roztworu tego kwasu od jego stężenia molowego w zakresie stężeń od 0,002 mol × dm−3 do 0,028 mol × dm−3 (𝑡 = 20 °C).
Uzupełnij tabelę brakującymi wartościami pH (z dokładnością do jednego miejsca po przecinku) oraz dokończ wykres zależności pH roztworu kwasu HX od jego stężenia molowego. Następnie oblicz stężenie molowe jonów X− i stężenie molowe niezdysocjowanych cząsteczek HX w roztworze o pH = 𝟐,𝟐. Odczyt z wykresu wykonaj z dokładnością do 𝟎, 𝟎𝟎𝟐 𝐦𝐨𝐥 · 𝐝𝐦−𝟑 , a wartości stężenia molowego jonów X− i cząsteczek HX podaj z dokładnością do 𝟎, 𝟎𝟎𝟏 𝐦𝐨𝐥 · 𝐝𝐦−𝟑. W roztworze o pH = 2,2 stężenie molowe jonów X– jest równe , a stężenie molowe niezdysocjowanych cząsteczek kwasu HX jest równe . Rozwiązanie tego zadania dostępne jest nieodpłatnie pod poniższym linkiem: