Wybór właściwego równania reakcji chemicznej na podstawie diagramu opisującego zawartość reagenta w zależności od ciśnienia i temperatury. Zadanie 7. Arkusz CKE chemia maj 2016 rozszerzony (1 punkt)
W wyniku pewnej odwracalnej reakcji chemicznej z dwóch substratów powstaje jeden produkt. Przemiana przebiega w fazie gazowej, co oznacza, że oba substraty i produkt są gazami. Reakcję tę przeprowadzono w zamkniętym reaktorze przy użyciu stechiometrycznych ilości substratów w różnych temperaturach i pod różnym ciśnieniem. Na poniższym diagramie przedstawiono, jaki procent objętości mieszaniny poreakcyjnej w reaktorze stanowiła objętość produktu tej reakcji w zależności od warunków temperatury i ciśnienia, w jakich przebiegała.
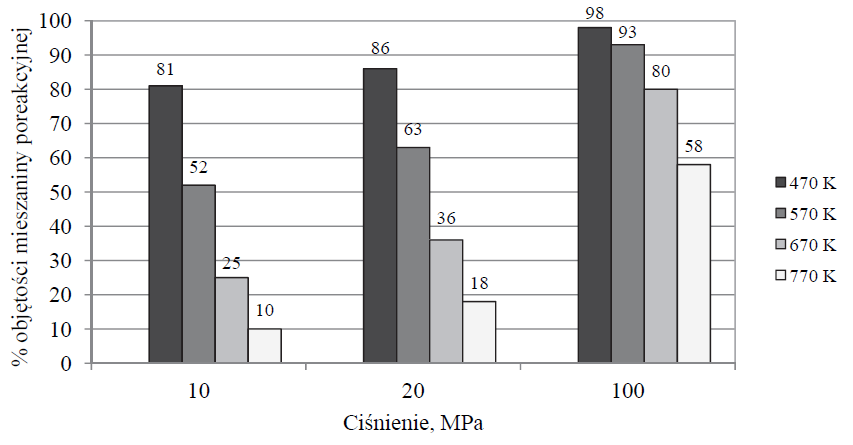
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2010.
Spośród reakcji, których równania przedstawiono poniżej, wybierz tę, do której mógłby odnosić się przedstawiony diagram. Zaznacz wybraną odpowiedź. 1. H2 (g) + Cl2 (g) → 2HCl (g) ΔH < 0 2. H2 (g) + I2 (g) → 2HI (g) ΔH > 0 3. N2 (g) + 3H2 (g) → 2NH3 (g) ΔH < 0 4. 2Cl2 (g) + O2 (g) → 2Cl2O (g) ΔH > 0