Obliczanie sumarycznego stężenia molowego jonów w wodnym roztworze kwasu glikolowego
W wodzie kwas glikolowy ulega jednoetapowej dysocjacji elektrolitycznej na jony. W temperaturze 25 oC przygotowano 350 cm3 roztworu kwasu glikolowego o stężeniu równym 0,5 mol∙dm–³. W roztworze tym dysocjacji ulega 17 na każde 1000 cząsteczek kwasu.
Oblicz sumaryczne stężenie molowe jonów powstałych w wyniku dysocjacji elektrolitycznej kwasu glikolowego. Wynik podaj z dokładnością do trzeciego miejsca po przecinku. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie liczby anionów reszty kwasu glikolowego w jego wodnym roztworze
W wodzie kwas glikolowy ulega jednoetapowej dysocjacji elektrolitycznej na jony. W temperaturze 25 oC przygotowano 350 cm3 roztworu kwasu glikolowego o stężeniu równym 0,5 mol∙dm–³. W roztworze tym dysocjacji ulega 17 na każde 1000 cząsteczek kwasu.
Oblicz liczbę anionów reszty kwasu glikolowego, jakie znajdują się w przygotowanym roztworze. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie stopnia dysocjacji w roztworze wody amoniakalnej
W wyniku nasycania wody amoniakiem uzyskuje się roztwór zwany wodą amoniakalną. W celu przygotowania opisanego roztworu, odmierzono pewną objętość amoniaku, a następnie wprowadzono do naczynia zawierającego wodę destylowaną, uzyskując roztwór wody amoniakalnej o stężeniu równym 0,5 mol∙dm–3.
Oblicz, jaki procent cząsteczek amoniaku przekształca się w jony amonowe w roztworze o podanym w informacji wprowadzającej stężeniu molowym? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Porównanie stopni dysocjacji w wodnych roztworach związków chemicznych
W tabeli zamieszczono dane na temat wybranych wskaźników kwasowo-zasadowych:
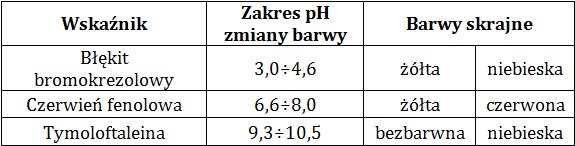
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
W trzech probówkach umieszczono kolejno po 5 cm3 wodnych roztworów związków chemicznych o stężeniach:
Ba(OH)2 2·10–4 mol·dm–3, HClO2 2·10–2 mol·dm–3 oraz HClO 2·10–4 mol·dm–3.
W wykropkowane pola wstaw odpowiedni znak („>”, „=” lub „<”), opisujący relację między wartościami stopnia dysocjacji (α) związków chemicznych w roztworach, których stężenia podano w informacji wprowadzającej. Ba(OH)2 ……… HClO Ba(OH)2 ……… HClO2 HClO ……… HClO2 © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Uszeregowanie roztworów elektrolitów według wzrastającego stopnia dysocjacji
W temperaturze 25 oC przygotowano wodne roztwory kilku związków chemicznych. Dane zebrano w tabeli:
HF o stężeniu 0,2 mol·dm–3
HClO2 o stężeniu 1 mol·dm–3
CH3COOH o stężeniu 0,05 mol·dm–3
(CH3)3N o stężeniu 0,08 mol·dm–3
HCOOH o stężeniu 3 mol·dm–3
C6H5COOH o stężeniu 0,001 mol·dm–3.
Uszereguj podane w informacji wstępnej roztwory według wzrastającego stopnia dysocjacji znajdujących się w nich związków chemicznych. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Stężenie cząsteczek niezdysocjowanych w roztworze kwasu fluorowodorowego
Roztwory kwasu fluorowodorowego są słabymi elektrolitami.
Oblicz stężenie molowe niezdysocjowanych cząsteczek fluorowodoru w jego wodnym roztworze o stężeniu równym 0,6 mol∙dm–3, jeśli stała równowagi procesu dysocjacji elektrolitycznej wynosi 6,3∙10–4. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zapis równania procesu autodysocjacji kwasu mrówkowego ze wskazaniem par kwas-zasada Brønsteda
W temperaturze 298 K bezwodny kwas mrówkowy (HCOOH) jest cieczą o gęstości 1,213 g∙cm–3. Związek ten ulega procesowi autodysocjacji, a jednym z jego produktów jest anion mrówczanowy. W temperaturze 298 K iloczyn jonowy kwasu mrówkowego ma wartość stałą i wynosi 6∙10–7.
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Napisz równanie procesu autodysocjacji kwasu mrówkowego. Wskaż biorące w nim udział sprzężone pary kwas-zasada Brønsteda. W tym celu uzupełnij tabelę. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone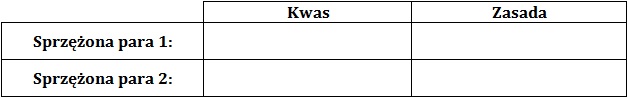
Obliczanie procentu cząsteczek kwasu mrówkowego ulegających autodysocjacji
W temperaturze 298 K bezwodny kwas mrówkowy (HCOOH) jest cieczą o gęstości 1,213 g∙cm–3. Związek ten ulega procesowi autodysocjacji, a jednym z jego produktów jest anion mrówczanowy. W temperaturze 298 K iloczyn jonowy kwasu mrówkowego ma wartość stałą i wynosi 6∙10–7.
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
W laboratorium przechowywano 1 dm3 kwasu mrówkowego.
Oblicz, jaki procent cząsteczek tego związku chemicznego ulega procesowi autodysocjacji w temperaturze 298 K? Wynik podaj z dokładnością do czwartego miejsca po przecinku. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Opis obserwacji na podstawie obliczeń dotyczących zmiany pH roztworu wodorotlenku baru
W tabeli zamieszczono dane na temat wybranych wskaźników kwasowo-zasadowych:

Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
W trzech probówkach umieszczono kolejno po 5 cm3 wodnych roztworów związków chemicznych o stężeniach:
Ba(OH)2 2·10–4 mol·dm–3, HClO2 2·10–2 mol·dm–3 oraz HClO 2·10–4 mol·dm–3.
Do probówki z podanym roztworem wodorotlenku baru dodano tymoloftaleinę. Po wstrząśnięciu zawartość naczynia przelano do zlewki i dodano 595 cm3 wody destylowanej.
Napisz, co zaobserwowano w wyniku rozcieńczenia roztworu? Swoją odpowiedź uzasadnij odpowiednimi obliczeniami. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie sumarycznego stężenia jonów w roztworze o określonej wartości pH
W temperaturze 25 ⁰C stała równowagi reakcji dysocjacji kwasu chlorowego(III) ma wartość 1,1∙10–².
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Oblicz, jakie powinno być sumaryczne stężenie molowe jonów H+ oraz Cl– w roztworze kwasu solnego, aby wartość pH tego roztworu była identyczna, jak roztworu kwasu chlorowego(III) o stężeniu 0,1 mol∙dm–³? Wynik obliczeń podaj z dokładnością do trzeciego miejsca po przecinku. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określanie barwy wskaźnika kwasowo-zasadowego na podstawie wartości pH roztworu uzyskanego po zmieszaniu roztworów kwasu i zasady
Roztwory wodne o wartości pH poniżej 3,2, zawierające oranż metylowy mają barwę czerwoną, a o wartości pH powyżej 4,4 – żółtą.
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Określ, jaką barwę przyjmie oranż metylowy w roztworze uzyskanym w wyniku zmieszania 10 cm³ roztworu wodorotlenku potasu (0,001 mol∙dm–³) z 10 cm³ roztworu kwasu solnego (0,05 mol∙dm–³)? Odpowiedź uzasadnij obliczeniami. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie wartości pH roztworu kwasu bromowodorowego na podstawie liczby jonów bromkowych
W 300 cm3 pewnego roztworu kwasu bromowodorowego znajduje się 2,71·1020 anionów bromkowych.
Ustal na podstawie niezbędnych obliczeń wartość pH tego roztworu. Wynik podaj z dokładnością do pierwszego miejsca po przecinku. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie wartości pH roztworu kwasu chlorowego(III) na podstawie liczby jonów chloranowych(III)
W temperaturze 298 K pewien wodny roztwór kwasu chlorowego(III) o objętości 200 cm3 jest układem homogenicznym, w którym znajduje się 1,204·1021 anionów chloranowych(III).
Oblicz wartość pH opisanej mieszaniny. Wynik podaj z dokładnością do cyfry jedności. Rozwiązanie tego zadania dostępne jest nieodpłatnie pod poniższym linkiem: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określenie, których drobin jest więcej w roztworze kwasu chlorowego(III) o określonej liczbie jonów chloranowych(III)
W temperaturze 298 K pewien wodny roztwór kwasu chlorowego(III) o objętości 200 cm3 jest układem homogenicznym, w którym znajduje się 1,204·1021 anionów chloranowych(III).
Ustal na podstawie niezbędnych obliczeń, jakich drobin jest więcej w opisanym roztworze – cząsteczek kwasu, czy anionów chloranowych(III)? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie zakresu pH odpowiedniego dla prawidłowego funkcjonowania organizmu
W celu zapewnienia właściwych warunków funkcjonowania organizmu ludzkiego, wartości stężeń jonów wodorowych we wszystkich jego przestrzeniach wodnych powinny mieścić się w zakresie 35÷45 nmol/l. Stężenie wyższe, niż podana wartość graniczna występuje w przypadku tzw. kwasicy, natomiast niższe, gdy mamy do czynienia z zasadowicą.
Na podstawie: W. Noszczyk, Chirurgia, Warszawa 2016.
Oblicz, jakiemu zakresowi pH odpowiada stężenie jonów wodorowych zapewniające właściwe warunki jego funkcjonowania? Wynik podaj z dokładnością do trzech cyfr znaczących, zaczynając od najniższej obliczonej wartości pH. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone

