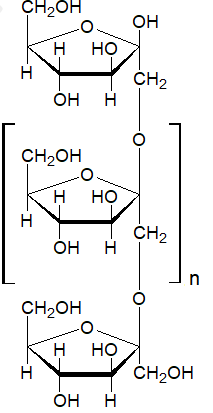
Zadanie 32. Arkusz Palladium kwiecień 2025 (1 punkt)
Aminy mogą reagować z kwasami karboksylowymi tworząc sole amoniowe, które w wyniku ogrzewania w odpowiedniej temperaturze ulegają przekształceniu w wodę oraz amidy. W przypadku amidów II-rzędowych, reszta pochodząca od kwasu karboksylowego oraz I-rzędowej aminy połączone są wiązaniem peptydowym.
Uzupełnij poniższy schemat wzorami grupowymi odpowiednich związków organicznych. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone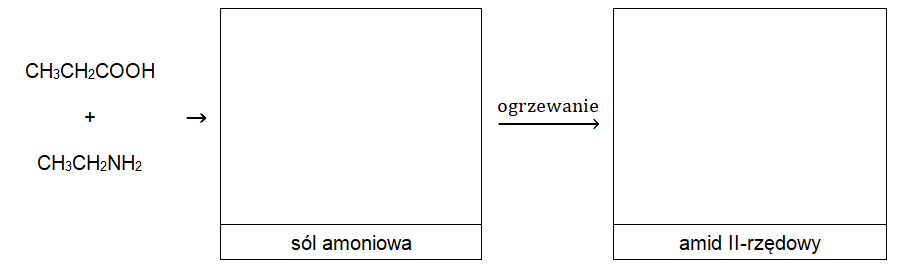
Zadanie 33. Arkusz Palladium kwiecień 2025 (1 punkt)
Zamieszczony rysunek przedstawia strukturę cząsteczki D-ksylozy.
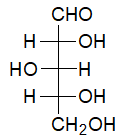
W wyniku jej redukcji powstaje związek chemiczny X zawierający wyłącznie jeden rodzaj grup funkcyjnych.
Oceń, czy wodny roztwór D-ksylozy oraz wodny roztwór związku chemicznego X wykazują czynność optyczną. Uzasadnij odpowiedź. Ocena odnośnie D-ksylozy wraz z uzasadnieniem: Ocena odnośnie związku X wraz z uzasadnieniem: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 1. Zapis równania reakcji spalania oraz wskazanie modelu cząsteczki. Doświadczenia chemiczne w zadaniach część 1. Rozdział 1(1 punkt)
Fotografia 1. ilustruje pewien pierwiastek chemiczny, którego atomy mają trzy powłoki elektronowe. Substancja ta spalając się w tlenie ulega przekształceniu w gazowy (298 K, 1013 hPa) związek chemiczny, powodujący widoczną na fotografii 2. zmianę barwy uniwersalnego papierka wskaźnikowego.

Napisz równanie reakcji spalania opisanego pierwiastka w tlenie, a następnie wybierz kształt cząsteczki powstałego produktu, zaznaczając jeden z zamieszczonych niżej modeli. Równanie reakcji: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone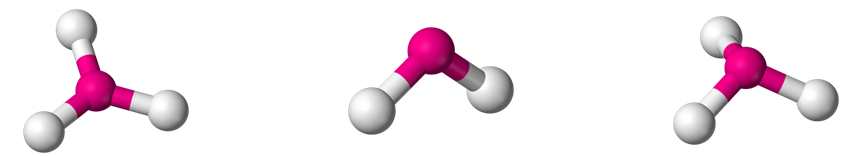
Zadanie 2. Ocena poprawności zdań. Doświadczenia chemiczne w zadaniach część 1. Rozdział 1 (1 punkt)
Fotografia 1. ilustruje pewien pierwiastek chemiczny, którego atomy mają trzy powłoki elektronowe. Substancja ta spalając się w tlenie ulega przekształceniu w gazowy (298 K, 1013 hPa) związek chemiczny, powodujący widoczną na fotografii 2. zmianę barwy uniwersalnego papierka wskaźnikowego.

Oceń poprawność poniższych zdań dotyczących pierwiastka, którego próbkę przedstawia fotografia 1. Wpisz literę „P” (prawda) lub literę „F” (fałsz). 1. Pierwiastek ten nie występuje w postaci odmian alotropowych. 2. Produkt spalania tego pierwiastka w tlenie można przekształcić w tlenek, w którym pierwiastek ten przyjmuje swój maksymalny stopień utlenienia. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 3. Wybór właściwych słów w nawiasach. Doświadczenia chemiczne w zadaniach część 1. Rozdział 1 (1 punkt)
W temperaturze 25 oC próbkę pewnego pierwiastka chemicznego X tworzącego cząsteczki dwuatomowe umieszczono w probówce. Zawartość naczynia ogrzano wykorzystując palnik gazowy, a następnie powoli ochłodzono do temperatury początkowej. Schemat opisanego doświadczenia ilustrują fotografie:

Podkreśl odpowiednie słowa w nawiasach, aby powstały zdania prawdziwe. W celu wykonania opisanego doświadczenia wykorzystano próbkę (siarki / jodu / bromu / rtęci), w której znajdujące się cząsteczki zbudowane są z (jednego / dwóch / czterech) atomów. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 4. Nazywanie przemian fizycznych. Doświadczenia chemiczne w zadaniach część 1. Rozdział 1 (1 punkt)
W temperaturze 25 oC próbkę pewnego pierwiastka chemicznego X tworzącego cząsteczki dwuatomowe umieszczono w probówce. Zawartość naczynia ogrzano wykorzystując palnik gazowy, a następnie powoli ochłodzono do temperatury początkowej. Schemat opisanego doświadczenia ilustrują fotografie:

Podczas ogrzewania próbki, w układzie panowały takie warunki, że równolegle przebiegały trzy procesy fizyczne – topnienie, sublimacja oraz parowanie.
Schematom podanych niżej przemian z udziałem pierwiastka chemicznego X przyporządkuj odpowiednie nazwy odpowiadającym im procesów fizycznych. Uzupełnij tabelę. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone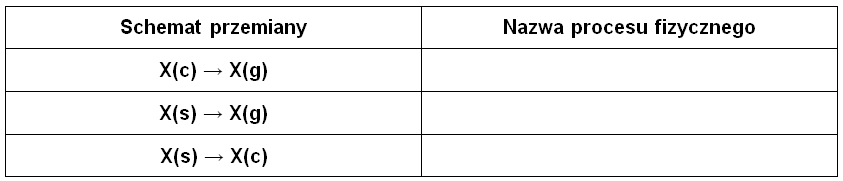
Zadanie 5. Nazywanie przemian fizycznych. Doświadczenia chemiczne w zadaniach część 1. Rozdział 1 (1 punkt)
W temperaturze 25 oC próbkę pewnego pierwiastka chemicznego X tworzącego cząsteczki dwuatomowe umieszczono w probówce. Zawartość naczynia ogrzano wykorzystując palnik gazowy, a następnie powoli ochłodzono do temperatury początkowej. Schemat opisanego doświadczenia ilustrują fotografie:

Podczas chłodzenia zawartości naczynia widocznej na fotografii 2., barwna substancja znajdująca się w fazie gazowej przekształciła się w krystaliczną postać widoczną na ściankach probówki 3.
Podaj nazwę opisanej przemiany oraz określ jej rodzaj (chemiczna, fizyczna). Nazwa przemiany: Typ przemiany: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 6. Nazywanie przemian fizycznych. Doświadczenia chemiczne w zadaniach część 1. Rozdział 1 (1 punkt)
Jedna z odmian alotropowych pewnego niemetalicznego pierwiastka chemicznego X tworzy cząsteczki o kształcie zilustrowanym modelem widocznym na fotografii 1. Próbkę innej odmiany alotropowej tego pierwiastka chemicznego ilustruje fotografia 2. W wyniku spalenia tej substancji w tlenie powstaje związek chemiczny, który po wprowadzeniu do wody z dodatkiem kilku kropli roztworu oranżu metylowego daje roztwór związku Y widoczny na fotografii 3. Jeśli do roztworu zawierającego 0,1 mola tej substancji wprowadzonych zostanie 1,204∙1023 lub 1,806∙1023 jonów OH–, uzyskuje się wtedy efekt widoczny na fotografii 4. Gdy jednak stosunek molowy związku Y względem wprowadzonych jonów wodorotlenkowych wyniesie 1:1, taka mieszanina osiągnie pH niższe niż 7.

Określ typ hybrydyzacji orbitali walencyjnych atomów pierwiastka X budujących cząsteczki, których model ilustruje fotografia 1. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 7. Zapis równania procesu chemicznego zgodnie z teorią Brønsteda-Lowry’ego. Doświadczenia chemiczne w zadaniach część 1. Rozdział 1 (1 punkt)
Jedna z odmian alotropowych pewnego niemetalicznego pierwiastka chemicznego X tworzy cząsteczki o kształcie zilustrowanym modelem widocznym na fotografii 1. Próbkę innej odmiany alotropowej tego pierwiastka chemicznego ilustruje fotografia 2. W wyniku spalenia tej substancji w tlenie powstaje związek chemiczny, który po wprowadzeniu do wody z dodatkiem kilku kropli roztworu oranżu metylowego daje roztwór związku Y widoczny na fotografii 3. Jeśli do roztworu zawierającego 0,1 mola tej substancji wprowadzonych zostanie 1,204∙1023 lub 1,806∙1023 jonów OH–, uzyskuje się wtedy efekt widoczny na fotografii 4. Gdy jednak stosunek molowy związku Y względem wprowadzonych jonów wodorotlenkowych wyniesie 1:1, taka mieszanina osiągnie pH niższe niż 7.

Stosując teorię protonową kwasów i zasad Brønsteda-Lowry’ego, napisz równanie procesu chemicznego warunkującego odczyn roztworu związku Y, jaki swoją barwą opisuje zawartość probówki widoczna na fotografii 3. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone