Wybór doświadczeń podczas których zaobserwowano jednakowy wzrost temperatury. Zadanie 21.2. Arkusz CKE chemia maj 2016 rozszerzony (1 punkt)
W celu zbadania efektu cieplnego reakcji chemicznych przeprowadzono cztery doświadczenia oznaczone numerami I–IV. Mieszano po 100 cm3 wodnych roztworów substancji, wymienionych w odpowiednich wierszach tabeli, o stężeniu molowym 0, 2 mol ⋅dm−3 i o początkowej temperaturze równej 25 oC. Następnie zmierzono temperaturę każdej z otrzymanych mieszanin.
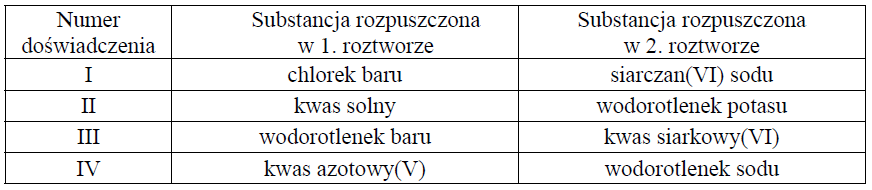
Zaobserwowano, że w każdym doświadczeniu temperatura uzyskanych mieszanin była wyższa niż temperatura użytych roztworów i że przyrost temperatury ΔT w niektórych doświadczeniach był taki sam.
Napisz numery wszystkich doświadczeń, w których zaobserwowany wzrost temperatury ΔT był jednakowy.
Wskazanie właściwej blaszki oraz zapis równania reakcji chemicznej. Zadanie 22. Arkusz CKE chemia maj 2016 rozszerzony (1 punkt)
Przeprowadzono doświadczenie zilustrowane poniższym schematem.
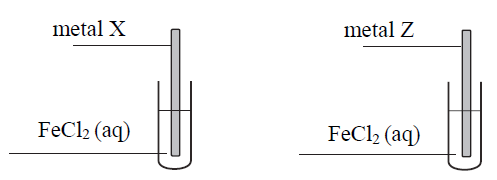
Celem doświadczenia było odróżnienie dwóch, oznaczonych umownie literami X i Z, metali,z których wykonano płytki. Wiadomo, że jednym metalem był cynk, a drugim – nikiel. Po pewnym czasie obie płytki wyjęto z roztworów, osuszono i zważono. Stwierdzono, że zmieniła się tylko masa płytki wykonanej z metalu X.
Uzupełnij poniższe zdania. Wybierz i zaznacz właściwe określenie spośród podanych w każdym nawiasie oraz napisz w formie jonowej skróconej równanie zachodzącej reakcji. Masa płytki wykonanej z metalu X się (zmniejszyła / zwiększyła). Podczas przeprowadzonego doświadczenia przebiegła reakcja zilustrowana równaniem: Metalem Z był (cynk / nikiel).
Ustalanie wzoru sumarycznego alkanu na podstawie ilości produktu uzyskanej w wyniku ciągu reakcji chemicznych. Zadanie 23. Arkusz CKE chemia maj 2016 rozszerzony (2 punkty)
Próbkę 0,86 grama pewnego alkanu poddano całkowitemu spaleniu, a cały otrzymany w tej reakcji tlenek węgla(IV) pochłonięto w wodzie wapiennej, w której zaszła reakcja zgodnie z równaniem:
CO2 + Ca(OH)2 → CaCO3 + H2O
Otrzymany osad ważył po wysuszeniu 6 gramów.
Ustal wzór sumaryczny tego alkanu. W obliczeniach zastosuj wartości masy molowej reagentów zaokrąglone do jedności.
Ustalenie wzorów grupowych alkenów na podstawie reakcji rozszczepienia ich cząsteczek zakwaszonym roztworem manganianu(VII) potasu. Zadanie 24.1. Arkusz CKE chemia maj 2016 rozszerzony (2 punkty)
Do określania położenia podwójnego wiązania w cząsteczkach alkenów wykorzystuje się ich utlenianie, np. za pomocą roztworu KMnO4 w środowisku kwasowym i w podwyższonej temperaturze. W tych warunkach dochodzi do rozerwania wiązania podwójnego węgiel – węgiel. W zależności od budowy cząsteczki alkenu mogą powstać kwasy karboksylowe, ketony lub tlenek węgla(IV).

Na podstawie: R. Morrison, R. Boyd, Chemia organiczna, Warszawa 1985.
Izomeryczne alkeny A i B utleniano KMnO4 w środowisku kwasowym. W wyniku przemiany, której uległ alken A, otrzymano jeden organiczny produkt, natomiast w wyniku utleniania alkenu B powstały dwa związki należące do różnych grup związków organicznych. W reakcji 1 mola alkenu B z 1 molem wodoru powstaje 2-metylopentan. Alken A występuje w postaci izomerów geometrycznych cis–trans.
Napisz wzory półstrukturalne (grupowe) alkenów A i B. Wyjaśnij, dlaczego alken B nie występuje w postaci izomerów geometrycznych cis–trans. Wyjaśnienie:
Zapis nazw systematycznych organicznych produktów rozszczepienia cząsteczek alkenów zakwaszonym roztworem manganianu(VII) potasu. Zadanie 24.2. Arkusz CKE chemia maj 2016 rozszerzony (1 punkt)
Do określania położenia podwójnego wiązania w cząsteczkach alkenów wykorzystuje się ich utlenianie, np. za pomocą roztworu KMnO4 w środowisku kwasowym i w podwyższonej temperaturze. W tych warunkach dochodzi do rozerwania wiązania podwójnego węgiel – węgiel. W zależności od budowy cząsteczki alkenu mogą powstać kwasy karboksylowe, ketony lub tlenek węgla(IV).

Na podstawie: R. Morrison, R. Boyd, Chemia organiczna, Warszawa 1985.
Izomeryczne alkeny A i B utleniano KMnO4 w środowisku kwasowym. W wyniku przemiany, której uległ alken A, otrzymano jeden organiczny produkt, natomiast w wyniku utleniania alkenu B powstały dwa związki należące do różnych grup związków organicznych. W reakcji 1 mola alkenu B z 1 molem wodoru powstaje 2-metylopentan. Alken A występuje w postaci izomerów geometrycznych cis–trans.
Podaj nazwy wszystkich związków organicznych, które powstały w wyniku utleniania alkenów A i B.
Wybór właściwych wyrazów dotyczących mechanizmu addycji wody do alkenów w środowisku kwasowym. Zadanie 25.1. Arkusz CKE chemia maj 2016 rozszerzony (1 punkt)
Woda przyłącza się do alkenów w obecności silnie kwasowego katalizatora H3O+. Addycja ta przebiega poprzez tworzenie kationów z ładunkiem dodatnim zlokalizowanym na atomie węgla, czyli tzw. karbokationów. Mechanizm tej reakcji dla alkenów o wzorze ogólnym R–CH=CH2 (R – grupa alkilowa) można przedstawić w trzech etapach.
Uwaga: w poniższych równaniach etapów reakcji wzór wody przedstawiono jako :OH2, a wzór kwasowego katalizatora zapisano jako H:OH2+.
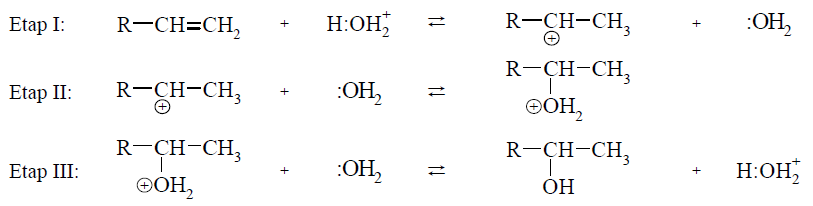
Na podstawie: R. Morrison, R. Boyd, Chemia organiczna, Warszawa 1985.
Uzupełnij poniższe zdania. Wybierz i zaznacz jedno właściwe określenie spośród podanych w każdym nawiasie.
Podczas etapu I alken ulega działaniu reagenta (wolnorodnikowego / nukleofilowego / elektrofilowego). W etapie II karbokation łączy się z cząsteczką wody, w wyniku czego powstaje protonowany alkohol. Na tym etapie przemiany woda działa jako (nukleofil / elektrofil). Podczas etapu III protonowany alkohol (oddaje / pobiera) proton, co prowadzi do powstania obojętnego alkoholu oraz do odtworzenia katalizatora.
Wybór wzorów alkoholi, których nie można otrzymać metodą opisaną w treści wprowadzającej do zadania. Zadanie 25.2. Arkusz CKE chemia maj 2016 rozszerzony (1 punkt)
Woda przyłącza się do alkenów w obecności silnie kwasowego katalizatora H3O+. Addycja ta przebiega poprzez tworzenie kationów z ładunkiem dodatnim zlokalizowanym na atomie węgla, czyli tzw. karbokationów. Mechanizm tej reakcji dla alkenów o wzorze ogólnym R–CH=CH2 (R – grupa alkilowa) można przedstawić w trzech etapach.
Uwaga: w poniższych równaniach etapów reakcji wzór wody przedstawiono jako :OH2, a wzór kwasowego katalizatora zapisano jako H:OH2+.
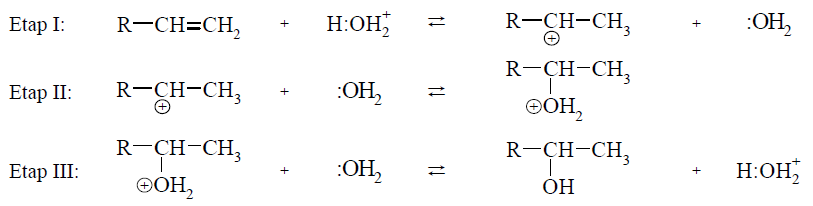
Na podstawie: R. Morrison, R. Boyd, Chemia organiczna, Warszawa 1985.
Spośród alkoholi o podanych niżej wzorach wybierz te, których nie można (jako produktu głównego) otrzymać podczas hydratacji alkenów prowadzonej w obecności kwasu. Podkreśl wzory wybranych alkoholi i uzasadnij swój wybór. CH3CH2OH CH3CH(OH)CH3 CH3CH2CH2OH CH3CH2CH(OH)CH3 CH3CH2CH2CH2OH Uzasadnienie:
Wybór nieczynnych optycznie związków chemicznych z uzasadnieniem wyboru. Zadanie 26. Arkusz CKE chemia maj 2016 rozszerzony (2 punkty)
Poniżej przedstawiono wzory stereochemiczne Fischera trzech związków organicznych. Dwa z nich nie są optycznie czynne – ich cząsteczki nie są chiralne.
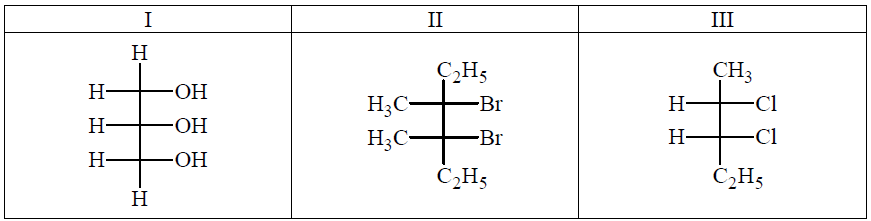
Spośród podanych wzorów związków chemicznych wybierz wzory tych, które nie są optycznie czynne. Wpisz do poniższej tabeli numery, którymi oznaczono te związki, i w każdym przypadku uzasadnij swój wybór.
Zapis równania reakcji chemicznej na podstawie schematu ciągu przemian. Zadanie 27. Arkusz CKE chemia maj 2016 rozszerzony (1 punkt)
Przeprowadzono ciąg przemian opisany poniższym schematem.
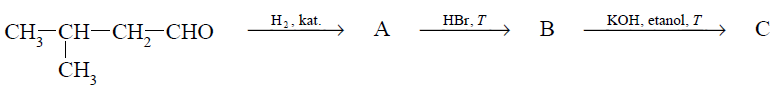
Napisz równanie reakcji prowadzącej do otrzymania produktu A. Zastosuj wzory półstrukturalne (grupowe) związków organicznych.
Zapis grupowy wzoru związku chemicznego oraz określenie typu reakcji chemicznej. Zadanie 28. Arkusz CKE chemia maj 2016 rozszerzony (1 punkt)
Przeprowadzono ciąg przemian opisany poniższym schematem.
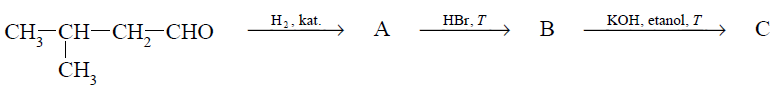
Uzupełnij poniższą tabelę. Podaj wzór półstrukturalny (grupowy) związku organicznego oznaczonego na schemacie literą B. Określ typ reakcji (addycja, eliminacja, substytucja), w wyniku której powstaje związek C.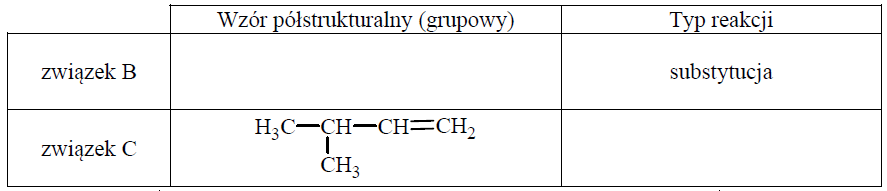
Rysowanie wzoru izomeru trans aldehydu cynamonowego. Zadanie 29. Arkusz CKE chemia maj 2016 rozszerzony (1 punkt)
Aldehyd cynamonowy to związek o wzorze:
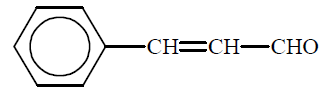
Aldehyd ten występuje w przyrodzie w konfiguracji trans.
Napisz wzór izomeru trans aldehydu cynamonowego.
Zapis obserwacji na podstawie doświadczenia przeprowadzonego z udziałem aldehydu cynamonowego. Zadanie 30. Arkusz CKE chemia maj 2016 rozszerzony (1 punkt)
W celu zbadania właściwości aldehydu cynamonowego wykonano eksperyment, którego przebieg zilustrowano na rysunku.
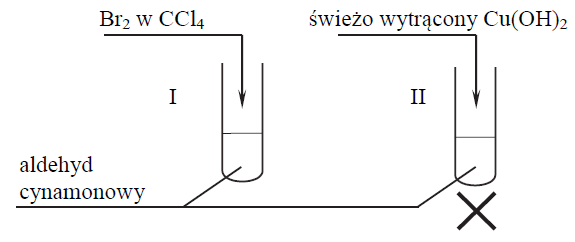
Porównaj przebieg reakcji w obu probówkach. Dokończ poniższe zdania – wybierz i podkreśl właściwe opisy spostrzeżeń spośród podanych w nawiasach. 1. Po dodaniu odczynnika do probówki I zaobserwowano, że roztwór bromu (uległ odbarwieniu / zabarwił się na fioletowo / nie zmienił zabarwienia). 2. W probówce II w wyniku ogrzewania zawiesiny wodorotlenku miedzi(II) z aldehydem cynamonowym powstał (szafirowy roztwór / ceglasty osad / różowy roztwór).
Obliczanie wartości pH roztworu. Zadanie 31. Arkusz CKE chemia maj 2016 rozszerzony (2 punkty)
Przygotowano dwa wodne roztwory kwasu metanowego (mrówkowego) o temperaturze t = 20 oC: roztwór pierwszy o pH = 1,9 i roztwór drugi o nieznanym pH. Stopień dysocjacji kwasu w roztworze pierwszym jest równy 1,33%, a w roztworze drugim wynosi 4,15%.
Na podstawie: Z. Dobkowska, K. Pazdro, Szkolny poradnik chemiczny, Warszawa 1990.
Oblicz pH roztworu, w którym stopień dysocjacji kwasu metanowego jest równy 4,15%. Wynik końcowy zaokrąglij do pierwszego miejsca po przecinku. Oceń, czy wyższa wartość stopnia dysocjacji kwasu w roztworze oznacza, że roztwór ten ma bardziej kwasowy odczyn. Ocena:
Ustalenie wzoru związku chemicznego biorącego udział w reakcji estryfikacji z kwasem 2-hydroksypropanowym. Zadanie 32. Arkusz CKE chemia maj 2016 rozszerzony (1 punkt)
Kwas 2-hydroksypropanowy w reakcji ze związkiem X tworzy ester o wzorze sumarycznym C5H8O4. Orbitalom walencyjnym każdego z atomów węgla budujących cząsteczkę związku X przypisuje się inny typ hybrydyzacji. Ponadto wiadomo, że w cząsteczce związku X występuje tylko jedna grupa funkcyjna.
Ustal wzór związku X, którego użyto do estryfikacji kwasu 2-hydroksypropanowego, i napisz równanie reakcji otrzymywania opisanego estru. Zastosuj wzory półstrukturalne (grupowe) związków organicznych.
Wskazanie enolowych oraz asymetrycznych atomów węgla w cząsteczce kwasu askorbinowego. Zadanie 33. Arkusz CKE chemia maj 2016 rozszerzony (1 punkt)
W cząsteczce kwasu askorbinowego (witaminy C) występują dwa enolowe atomy węgla, czyli atomy węgla o hybrydyzacji sp2 z przyłączonymi grupami hydroksylowymi. Cząsteczka tego związku zawiera ponadto dwa asymetryczne atomy węgla – o hybrydyzacji sp3 z przyłączonymi czterema różnymi podstawnikami. Poniżej przedstawiono wzór witaminy C, w którym małymi literami oznaczono poszczególne atomy węgla.
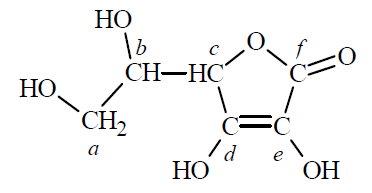
Napisz litery (a–f), którymi oznaczono w powyższym wzorze kwasu askorbinowego wszystkie enolowe atomy węgla oraz wszystkie asymetryczne atomy węgla. Enolowe atomy węgla: Asymetryczne atomy węgla:

