Zadanie 21.3. Zapis równania reakcji chemicznej. Doświadczenia chemiczne w zadaniach część 1. Rozdział 4.1 (1 punkt)
Przeprowadzono doświadczenie chemiczne według schematu:
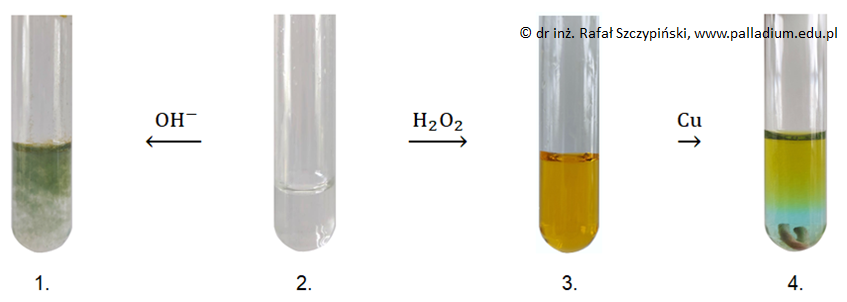
W probówce 2. znajdował się wodny roztwór powstały w wyniku reakcji nadmiaru kwasu solnego z próbką metalu pochodzącą ze stalowego pręta. Po zakończeniu reakcji w wyniku której powstał roztwór w 3. probówce, nie stwierdzono obecności nadtlenku wodoru w tym naczyniu.
Po wprowadzeniu wodnego roztworu odpowiedniego odczynnika – nadtlenku wodoru lub w wodorotlenku sodu – do widocznych na fotografiach 1. oraz 3. zawartości probówek można uzyskać ten sam związek chemiczny, którego zawiesinę przedstawia zamieszczona poniżej fotografia.

W wyniku prażenia ciała stałego stanowiącego przedstawiony czerwonobrunatny osad powstaje związek chemiczny, który reaguje z glinem przekształcając go w tlenek. Z uwagi na wysoką wartość efektu cieplnego tej przemiany, powstający w trakcie jej przebiegu metal występuje w ciekłym stanie skupienia.
Napisz równanie tej reakcji chemicznej, jaka przebiega z udziałem glinu. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 22. Zapis równania reakcji chemicznej. Doświadczenia chemiczne w zadaniach część 1. Rozdział 4.1 (1 punkt)
Przeprowadzono doświadczenie chemiczne według schematu:

W probówce 2. znajdował się wodny roztwór powstały w wyniku reakcji nadmiaru kwasu solnego z próbką metalu pochodzącą ze stalowego pręta. Po zakończeniu reakcji w wyniku której powstał roztwór w 3. probówce, nie stwierdzono obecności nadtlenku wodoru w tym naczyniu.
Napisz w formie jonowej skróconej równanie reakcji chemicznej prowadzącej do powstania zawartości 4. probówki. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 23.1. Wybór fotografii z uzasadnieniem. Doświadczenia chemiczne w zadaniach część 1. Rozdział 4.1 (1 punkt)
Cynk w reakcji z mocnymi zasadami tworzy hydroksokompleksy o liczbie koordynacyjnej 4. Do wodnego roztworu wodorotlenku potasu wprowadzono próbkę cynku.
Spośród zamieszczonych niżej fotografii wybierz tę, która przedstawia opisane naczynie chwilę po umieszczeniu w nim próbki metalu. Uzasadnij swój wybór – odnieś się do określonych objawów reakcji. Wybrana fotografia: Uzasadnienie: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 23.2. Zapis równania reakcji chemicznej cynku z zasadą potasową. Doświadczenia chemiczne w zadaniach część 1. Rozdział 4.1 (1 punkt)
Cynk w reakcji z mocnymi zasadami tworzy hydroksokompleksy o liczbie koordynacyjnej 4. Do wodnego roztworu wodorotlenku potasu wprowadzono próbkę cynku.
Napisz w formie jonowej skróconej równanie reakcji chemicznej cynku z zasadą potasową. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 24. Wskazanie metali wchodzących w skład monety. Doświadczenia chemiczne w zadaniach część 1. Rozdział 4.1 (1 punkt)
W celu ustalenia składu jakościowego pewnej monety przeprowadzono kilkuetapowe doświadczenie chemiczne. W tym celu analizowany stop metali podzielony został na dwie próbki.
Próbkę 1. wprowadzono do nadmiaru kwasu solnego. Po usunięciu nieprzereagowanego ciała stałego, do roztworu dodano najpierw zasadę potasową (fotografia 1.), a następnie roztwór H2O2 (fotografia 2.).
Próbkę 2. poddano działaniu stężonego roztworu kwasu azotowego(V). Powstały klarowny roztwór poddano działaniu wody amoniakalnej w niedomiarze (fotografia 3.) i w nadmiarze (fotografia 4.).

Spośród wymienionych niżej symboli metali podkreśl takie dwa, które na pewno wchodziły w skład badanej monety. Ca Fe Ag Cu Pb Au © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 1. Zapis równania reakcji oraz wybór właściwych słów w nawiasach. Doświadczenia chemiczne w zadaniach część 1. Rozdział 4.2 (2 punkty)
Przeprowadzono doświadczenie chemiczne z wykorzystaniem roztworu CuSO4 oraz jednego spośród metali – srebra, żelaza, glinu lub chromu. Schemat tego eksperymentu ilustrują fotografie:

Zapisz w formie jonowej skróconej równanie reakcji chemicznej w wyniku przebiegu której powstała zawartość probówki widoczna na 2. fotografii, a następnie podkreśl właściwe słowa w nawiasach odnoszące się do zmiany mas – blaszki wykorzystanej w tym doświadczeniu oraz roztworu. Równanie reakcji: Masa widocznej na 2. fotografii fazy wodnej była (większa / mniejsza) niż przed rozpoczęciem reakcji chemicznej. Masa blaszki wraz z osadzonym na niej metalem była (większa / mniejsza) niż przed rozpoczęciem doświadczenia. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 2.1. Wybór właściwej fotografii oraz zapis równania reakcji. Doświadczenia chemiczne w zadaniach część 1. Rozdział 4.2 (1 punkt)
Przeprowadzono doświadczenie chemiczne z wykorzystaniem roztworu CuSO4 oraz jednego spośród metali – srebra, żelaza, glinu lub chromu. Schemat tego eksperymentu ilustrują fotografie:

Blaszkę widoczną na fotografii 3. umieszczono w stosunkowo dużym nadmiarze kwasu bromowodorowego. Jedna z spośród fotografii A – D przedstawia zmianę możliwą do zaobserwowania po wykonaniu tej czynności.

Wybierz właściwą fotografię, a następnie napisz w formie jonowej skróconej równanie reakcji chemicznej, której przebieg jest przyczyną zmiany o której mowa. Oznaczenie literowe wybranej fotografii: Równanie reakcji chemicznej: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 2.2. Ocena z uzasadnieniem, czy obecna będzie faza stała. Doświadczenia chemiczne w zadaniach część 1. Rozdział 4.2 (1 punkt)
Przeprowadzono doświadczenie chemiczne z wykorzystaniem roztworu CuSO4 oraz jednego spośród metali – srebra, żelaza, glinu lub chromu. Schemat tego eksperymentu ilustrują fotografie:

Blaszkę widoczną na fotografii 3. umieszczono w stosunkowo dużym nadmiarze kwasu bromowodorowego. Jedna z spośród fotografii A – D przedstawia zmianę możliwą do zaobserwowania po wykonaniu tej czynności.

Oceń, czy po zakończeniu doświadczenia w wybranej przez Ciebie probówce będzie znajdować się również faza stała. Odpowiedź uzasadnij odnosząc się do potencjałów redukcji odpowiednich półogniw. Ocena: Uzasadnienie: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 3. Zapis równania reakcji chemicznej. Doświadczenia chemiczne w zadaniach część 1. Rozdział 4.2 (1 punkt)
Do wodnego roztworu siarczanu(VI) miedzi(II) wprowadzono wiórki magnezowe. Fotografie 1.–4. przedstawiają zmiany zawartości naczynia jakie nastąpiły w ciągu 15 minut od momentu rozpoczęcia doświadczenia chemicznego.

Napisz w formie jonowej skróconej równanie reakcji chemicznej w wyniku której nastąpiła widoczna na fotografii 4. względem fotografii 1. zmiana barwy fazy wodnej. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 4.1. Zapis równań procesów - katodowego oraz anodowego. Doświadczenia chemiczne w zadaniach część 1. Rozdział 4.2 (1 punkt)
Do wodnego roztworu siarczanu(VI) miedzi(II) wprowadzono wiórki magnezowe. Fotografie 1.–4. przedstawiają zmiany zawartości naczynia jakie nastąpiły w ciągu 15 minut od momentu rozpoczęcia doświadczenia chemicznego.

W trakcie opisanego doświadczenia na powierzchni magnezu tworzy się ogniwo chemiczne, w którym anodę stanowi aktywniejszy z metali. Na katodzie przebiega wówczas redukcja wody, co objawia się wydzielaniem widocznych na fotografiach 1.–3. drobnych pęcherzyków gazu.
Napisz w formie elektronowo-jonowej równania reakcji połówkowych jakie przebiegają na katodzie oraz anodzie w opisanym ogniwie. Proces katodowy: Proces anodowy: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 33.3. Wskazanie numeru właściwej probówki z zawartością. Doświadczenia chemiczne w zadaniach część 1. Rozdział 5 (1 punkt)
Fotografie 1.–4. przedstawiają albuminę (białko jaja kurzego) poddaną procesowi denaturacji przy użyciu odczynników:
H2SO4(stężony), CuSO4(aq), HNO3(stężony), NaOH(stężony).

Wskaż numer tej probówki, w której za denaturację odpowiada wyłącznie obecność kationów metalu ciężkiego. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 4.2. Wybór właściwego słowa w nawiasie. Doświadczenia chemiczne w zadaniach część 1. Rozdział 4.2 (1 punkt)
Do wodnego roztworu siarczanu(VI) miedzi(II) wprowadzono wiórki magnezowe. Fotografie 1.–4. przedstawiają zmiany zawartości naczynia jakie nastąpiły w ciągu 15 minut od momentu rozpoczęcia doświadczenia chemicznego.

W trakcie opisanego doświadczenia na powierzchni magnezu tworzy się ogniwo chemiczne, w którym anodę stanowi aktywniejszy z metali. Na katodzie przebiega wówczas redukcja wody, co objawia się wydzielaniem widocznych na fotografiach 1.–3. drobnych pęcherzyków gazu.
Porównaj zawartości naczyń przedstawione na fotografiach 1. oraz 4. Następnie podkreśl właściwe słowo w nawiasie. Magnez jest metalem o gęstości (większej / mniejszej) niż miedź w stanie standardowym. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 5. Wskazanie właściwej fotografii oraz zapis równania reakcji chemicznej. Doświadczenia chemiczne w zadaniach część 1. Rozdział 4.2 (1 punkt)
Glin jest pierwiastkiem, którego powierzchnię pokrywa pasywna warstwa tlenku, dlatego wiele reakcji chemicznych z udziałem tego metalu przebiega dopiero po mechanicznym usunięciu tlenku, lub po umieszczeniu w roztworze o odczynie silnie zasadowym.
W trzech probówkach umieszczono blaszki aluminiowe, przy czym tylko jedną z nich zarysowano usuwając w ten sposób pasywną warstwę tlenku. Do dwóch probówek wprowadzono roztwór azotanu(V) srebra, do trzeciej natomiast – wodny roztwór odczynnika Tollensa – mocnego elektrolitu zawierającego związek kompleksowy o wzorze [Ag(NH3)2]OH. W jednej z probówek objawy reakcji zaobserwowano praktycznie natychmiast, a w kolejnej – dopiero po kilkunastu godzinach. Fotografie 1.–3. w sposób losowy przedstawiają zawartość każdej z probówek po 24 godzinach od momentu rozpoczęcia eksperymentu.

Wskaż numer tej probówki, w której umieszczona blaszka została zarysowana. Odpowiedź uzasadnij równaniem reakcji chemicznej zapisanym w formie jonowej skróconej. Numer fotografii: Równanie reakcji: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone

