Wybór właściwego metalu jako protektora antykorozyjnego. Zadanie 19. Arkusz CKE chemia maj 2010 rozszerzony (1 punkt)
Wilgotne powietrze stanowi środowisko korozyjne, w którym metalowe przedmioty narażone są na zniszczenie. Metale można chronić przed korozją przez powlekanie ich powierzchni innymi metalami. Jeżeli w tym celu zastosuje się metal o potencjale większym od potencjału metalu chronionego (powłoka katodowa), pełne zabezpieczenie uzyskuje się tylko wówczas, gdy powłoka jest całkowicie szczelna. Jeżeli natomiast zastosuje się powłokę wykonaną z metalu o potencjale mniejszym od potencjału metalu chronionego (powłoka anodowa), jej uszkodzenie nie powoduje korozji metalu podłoża. O charakterze danej powłoki metalicznej na stali można wnioskować, porównując wartości standardowych potencjałów odpowiednich elektrod (typu Me/Men+).
Oceń, który metal (cynk czy miedź) powinien być zastosowany do ochrony przed korozją w wilgotnym powietrzu stalowego przedmiotu narażonego na zarysowania. Wybrany metal:
Rysowanie wzoru grupowego węglowodoru o o kreślonej strukturze cząsteczki. Zadanie 21. Arkusz CKE chemia maj 2010 rozszerzony (1 punkt)
Narysuj wzór strukturalny lub półstrukturalny (grupowy) węglowodoru, w którego cząsteczce występuje osiem wiązań σ i jedno wiązanie π.
Zapis równań reakcji chemicznych na podstawie ciągu przemian. Zadanie 22. Arkusz CKE chemia maj 2010 rozszerzony (3 punkty)
Alkeny bardzo łatwo przyłączają bromowodór lub chlorowodór. Reakcje te nie wymagają użycia katalizatorów ani podwyższenia temperatury. Powstałe w wyniku tej przemiany halogenki alkilowe mogą ulegać reakcji podstawienia lub reakcji eliminacji. Temperatura pokojowa i użycie wody jako rozpuszczalnika sprzyja reakcji podstawienia, natomiast użycie alkoholowego roztworu wodorotlenku potasu w podwyższonej temperaturze (około 80 oC) prowadzi do reakcji eliminacji. W obecności kwasu siarkowego(VI) alkeny mogą reagować także z wodą, dając alkohole. Poniżej przedstawiono ciąg przemian:
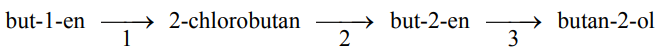
Skorzystaj z powyższej informacji i napisz równania reakcji 1, 2 oraz 3, stosując wzory półstrukturalne (grupowe) związków organicznych. Jeżeli reakcja wymaga użycia katalizatora, odpowiedniego środowiska lub podwyższenia temperatury, napisz to nad strzałką równania reakcji. Równania reakcji: 1: 2: 3:
Rysowanie wzorów grupowych dwóch związków organicznych. Zadanie 23a. Arkusz CKE chemia maj 2010 rozszerzony (2 punkty)
Poniżej podano dwa ciągi przemian chemicznych, w wyniku których otrzymano związki organiczne B i D.
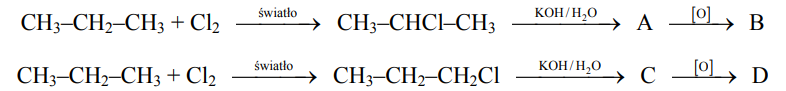
Narysuj wzór półstrukturalny (grupowy) związku oznaczonego literą B oraz podaj nazwę systematyczną związku oznaczonego literą D. Wzór związku B: Nazwa związku D:
Wskazanie typów reakcji w chemii organicznej. Zadanie 23b. Arkusz CKE chemia maj 2010 rozszerzony (1 punkt)
Poniżej podano dwa ciągi przemian chemicznych, w wyniku których otrzymano związki organiczne B i D.
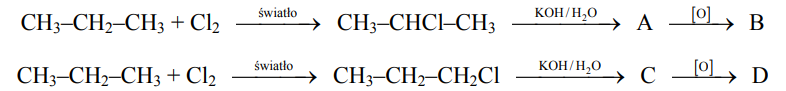
Stosując podział charakterystyczny dla chemii organicznej, określ typ reakcji, w wyniku których powstały związki oznaczone literami A i C.
Uzupełnienie schematu, aby uzyskać izomer cis alkenu. Zadanie 24. Arkusz CKE chemia maj 2010 rozszerzony (1 punkt)
Uzupełnij poniższy schemat, tak aby otrzymać wzór izomeru geometryczngo cis węglowodoru o wzorze grupowym CH3–CH2–CH=CH–CH2–CH3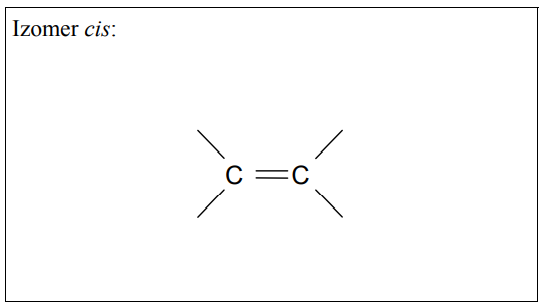
Przypisanie wartości stopni utlenienia atomom węgla. Zadanie 25. Arkusz CKE chemia maj 2010 rozszerzony (1 punkt)
Określ stopnie utlenienia atomów węgla w cząsteczce kwasu etanowego (octowego). Wypełnij tabelę, wpisując stopień utlenienia atomu węgla, którego symbol został podkreślony.
Wybór izomerów 1,2-dimetylobenzenu. Zadanie 26. Arkusz CKE chemia maj 2010 rozszerzony (1 punkt)
Spośród poniższych wzorów wybierz wszystkie, które są wzorami izomerów 1,2-dimetylobenzenu (napisz numery, którymi je oznaczono). Wzory izomerów 1,2-dimetylobenzenu: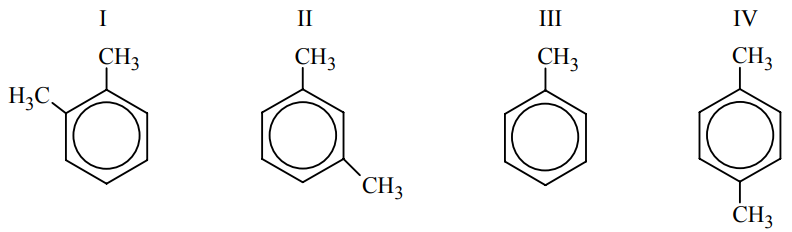
Zapis równania reakcji próby jodoformowej. Zadanie 27a. Arkusz CKE chemia maj 2010 rozszerzony (1 punkt)
Reakcją pozwalającą wykryć w związkach organicznych grupę
![]()
jest próba jodoformowa. Polega ona na reakcji związku organicznego z jodem w obecności NaOH w podwyższonej temperaturze. Po oziębieniu mieszaniny poreakcyjnej do temperatury pokojowej powstaje żółty, krystaliczny osad o charakterystycznym zapachu.
Jeżeli badanym związkiem jest propanon (aceton), produktami próby jodoformowej są: trijodometan, etanian sodu (octan sodu), jodek sodu i woda.
Korzystając z powyższych informacji, uzupełnij schemat, tak aby przedstawiał równanie opisanej reakcji w formie cząsteczkowej (wpisz wzory produktów reakcji i odpowiednie współczynniki stechiometryczne).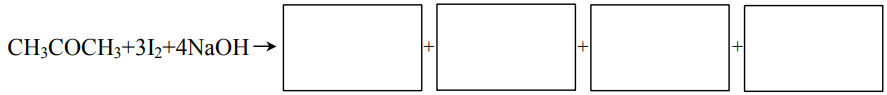
Zapis wzoru związku chemicznego stanowiącego osad o określonej barwie oraz zapachu. Zadanie 27b. Arkusz CKE chemia maj 2010 rozszerzony (1 punkt)
Reakcją pozwalającą wykryć w związkach organicznych grupę
![]()
jest próba jodoformowa. Polega ona na reakcji związku organicznego z jodem w obecności NaOH w podwyższonej temperaturze. Po oziębieniu mieszaniny poreakcyjnej do temperatury pokojowej powstaje żółty, krystaliczny osad o charakterystycznym zapachu.
Jeżeli badanym związkiem jest propanon (aceton), produktami próby jodoformowej są: trijodometan, etanian sodu (octan sodu), jodek sodu i woda.
Napisz wzór tego produktu przemiany, który tworzy żółty, krystaliczny osad o charakterystycznym zapachu.
Wskazanie, czy próba jodoformowa może posłużyć do odróżnienia acetonu od acetaldehydu. Zadanie 27c. Arkusz CKE chemia maj 2010 rozszerzony (1 punkt)
Reakcją pozwalającą wykryć w związkach organicznych grupę
![]()
jest próba jodoformowa. Polega ona na reakcji związku organicznego z jodem w obecności NaOH w podwyższonej temperaturze. Po oziębieniu mieszaniny poreakcyjnej do temperatury pokojowej powstaje żółty, krystaliczny osad o charakterystycznym zapachu.
Jeżeli badanym związkiem jest propanon (aceton), produktami próby jodoformowej są: trijodometan, etanian sodu (octan sodu), jodek sodu i woda.
Napisz, czy próba jodoformowa pozwala na odróżnienie propanonu (acetonu) od etanalu, i uzasadnij swoje stanowisko.
Ocena poprawności zdań dotyczących amin. Zadanie 28. Arkusz CKE chemia maj 2010 rozszerzony (2 punkty)
Oceń prawdziwość poniższych zdań i uzupełnij tabelę. Wpisz literę P, jeżeli uznasz zdanie za prawdziwe, lub literę F, jeżeli uznasz je za fałszywe. 1. Zasadowy charakter amin związany jest z obecnością wolnej pary elektronowej atomu azotu grupy aminowej, umożliwiającej przyłączenie jonu H+. 2. Wartości temperatury wrzenia amin alifatycznych są wyższe niż n-alkanów o porównywalnej masie molowej, gdyż między cząsteczkami amin tworzą się
wiązania wodorowe.
3. Fenyloaminę (anilinę) otrzymuje się przez utlenienie nitrobenzenu.
Zapis wzoru sumarycznego oraz grupowego związku chemicznego. Zadanie 29ab. Arkusz CKE chemia maj 2010 rozszerzony (2 punkty)
Pewien dwufunkcyjny związek organiczny ma masę molową równą 90 g/mol. W jego cząsteczce stosunek liczby atomów węgla, wodoru i tlenu wynosi 1:2:1.
a) Napisz wzór sumaryczny opisanego związku. b) Wiedząc, że związek ten w roztworze wodnym dysocjuje z odszczepieniem jonu wodorowego oraz że jego cząsteczka jest achiralna, narysuj wzór półstrukturalny (grupowy) tego związku.
Rysowanie wzoru jonu aminokwasu dominującego przy określonej wartości pH roztworu. Zadanie 30. Arkusz CKE chemia maj 2010 rozszerzony (1 punkt)
Punkt izoelektryczny (pI) aminokwasu to pH roztworu, w którym cząsteczki tego aminokwasu występują głównie w formie jonów obojnaczych. Kwas 2-aminobutanodiowy (asparaginowy) jest dikarboksylowym aminokwasem o wzorze sumarycznym C4H7O4N. Jego punkt izoelektryczny pI = 2,87.
Narysuj wzór półstrukturalny (grupowy) jonu, który jest dominującą formą tego aminokwasu w roztworze o pH = 1.

