Wybór związków chemicznych, które nie ulegają reakcji aldolowej. Zadanie 26.1. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (1 punkt)
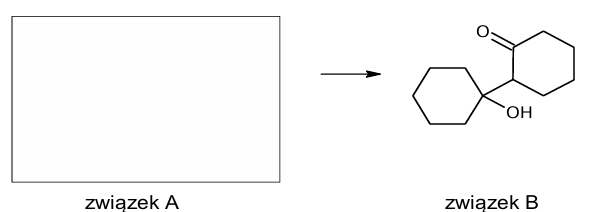
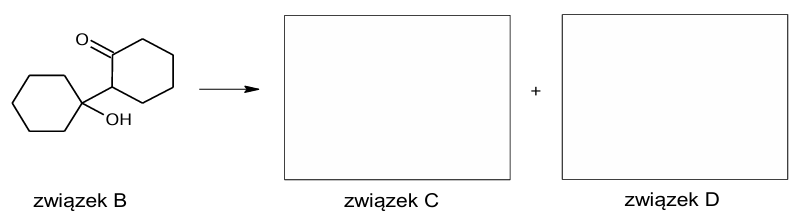
Aldehydy i ketony, których cząsteczki zawierają co najmniej jeden atom wodoru przy atomie węgla połączonym z grupą karbonylową (atomie węgla 𝛼), w środowisku zasadowym ulegają tzw. reakcji aldolowej. Ta reakcja prowadzi do połączenia dwóch cząsteczek aldehydów lub ketonów i do utworzenia wiązania między atomem węgla α jednej cząsteczki i karbonylowym atomem węgla drugiej cząsteczki. Bezpośrednim produktem reakcji aldolowej jest β-hydroksyaldehyd (aldol) lub β-hydroksyketon.
Na poniższym schemacie zielonym kolorem oznaczono wiązanie C – C utworzone w takiej reakcji.
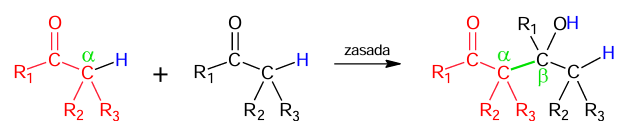
R1, R2, R3 – grupy węglowodorowe lub atomy wodoru.
Na podstawie: J. McMurry, Chemia organiczna, Warszawa 2018.
Spośród poniższych aldehydów i ketonów wybierz te, które nie ulegają reakcji aldolowej. Zaznacz ich nazwy. 2,2-dimetylopropanal acetaldehyd (etanal) benzaldehyd (benzenokarboaldehyd) 3,3-dimetylobutan-2-on
Rysowanie wzoru elektronowego drobiny. Zadanie 27. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (1 punkt)
Zbadano właściwości kwasu mrówkowego (metanowego). Przeprowadzono doświadczenie, w którym do probówki z zawiesiną wodorotlenku miedzi(II) wprowadzono wodny roztwór kwasu mrówkowego. Wygląd zawartości probówki przed dodaniem kwasu mrówkowego (zdjęcie 1.) i po jego dodaniu (zdjęcie 2.) przedstawiono poniżej.
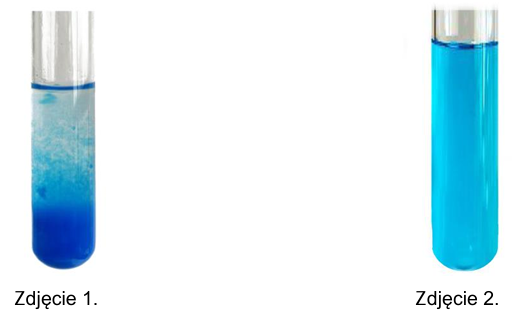
Napisz wzór elektronowy organicznej drobiny, która występuje w produkcie reakcji. Zaznacz kreskami pary elektronowe wiązań chemicznych oraz wolne pary elektronowe.
Zapis równania reakcji hydrolizy zasadowej octanu fenylu. Zadanie 28. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (1 punkt)
Ester o podanym poniżej wzorze poddano reakcji hydrolizy z nadmiarem wodnego roztworu wodorotlenku potasu.
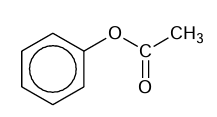
Uzupełnij schemat. Napisz w formie jonowej skróconej równanie reakcji hydrolizy zasadowej, której uległ przedstawiony ester.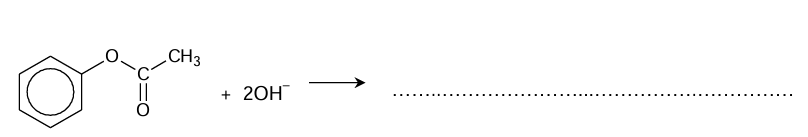
Zapis równania reakcji jonu obojnaczego kwasu asparaginowego z jonem wodorotlenkowym. Zadanie 29. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (1 punkt)
Kwas asparaginowy w roztworze wodnym może występować w postaci czterech form jonowych różniących się ładunkiem.
Wodny roztwór kwasu asparaginowego zakwaszono do pH = 1, a następnie miareczkowano roztworem wodorotlenku sodu. Podczas tego procesu kwas asparaginowy ulegał deprotonacji zgodnie z poniższym schematem:
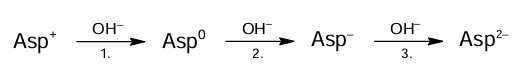
W powyższym schemacie zaznaczono sumaryczne ładunki elektryczne poszczególnych form tego aminokwasu. Forma kwasu asparaginowego oznaczona Asp0 to jon obojnaczy.
Napisz równanie reakcji 2. zachodzącej podczas przemiany jonu obojnaczego Asp0 w jon Asp–. Uzupełnij poniższy schemat. Wpisz wzory brakujących grup.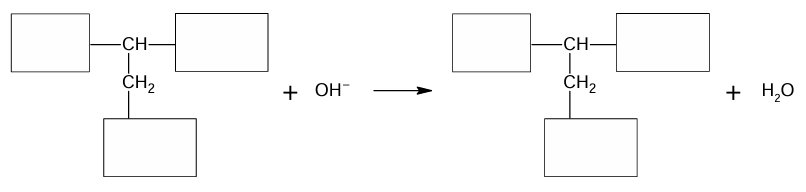
Ustalanie wzoru sumarycznego dipeptydu oraz nazwy aminokwasu. Zadanie 30. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (2 punkty)
W celu zidentyfikowania aminokwasów białkowych, których reszty wchodzą w skład pewnego dipeptydu X, przeprowadzono dwuetapową analizę.
Etap 1. Próbkę dipeptydu X poddano reakcji całkowitego spalania, której produktami były tlenek węgla(IV), azot i para wodna. Stosunek molowy substratów i produktów biorących udział w tej przemianie jest następujący:
![]()
Etap 2. Drugą próbkę badanego dipeptydu poddano hydrolizie i ustalono, że jeden z aminokwasów był związkiem achiralnym.
Wykonaj obliczenia i ustal wzór sumaryczny dipeptydu X. Napisz nazwę chiralnego aminokwasu, którego reszta wchodzi w skład dipeptydu. Wzór sumaryczny dipeptydu X: Nazwa aminokwasu chiralnego:
Wskazanie właściwej nazwy określonej formy D-tagatozy. Zadanie 31.1. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (1 punkt)
Poniżej przedstawiono – w projekcji Hawortha – wzór pewnej formy tagatozy.
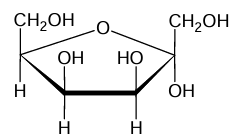
Zaznacz prawidłową nazwę przedstawionej formy D-tagatozy. α-D-tagatopiranoza β-D-tagatopiranoza α-D-tagatofuranoza β-D-tagatofuranoza
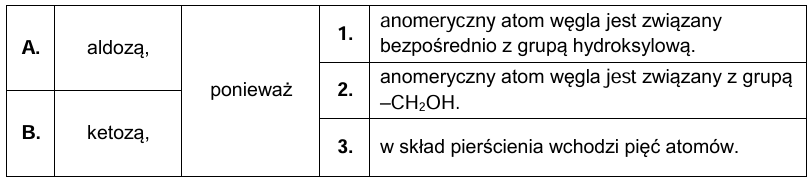
Przypisanie tagatozy do aldoz lub ketoz z uzasadnieniem. Zadanie 31.2. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (1 punkt)
Poniżej przedstawiono – w projekcji Hawortha – wzór pewnej formy tagatozy.

Dokończ zdanie. Zaznacz odpowiedź A albo B oraz uzasadnienie 1., 2. albo 3. Na podstawie przedstawionego wzoru stereochemicznego tagatozy można stwierdzić, że ten cukier jest