Zapis wzoru półstrukturalnego produktu reakcji kwasu winowego z nadmiarem metanolu. Zadanie 34. Arkusz CKE chemia maj 2017 rozszerzony (1 punkt)
Poniżej przedstawiono wzór kwasu winowego:
HOOC–CH(OH)–CH(OH)–COOH
Napisz wzór półstrukturalny (grupowy) organicznego produktu reakcji kwasu winowego z metanolem użytym w nadmiarze w środowisku stężonego kwasu siarkowego(VI).
Wybór właściwego odczynnika w celu przeprowadzenia doświadczenia chemicznego. Zadanie 35.1. Arkusz CKE chemia maj 2017 rozszerzony (1 punkt)
Wykonano doświadczenie, w którym do dwóch probówek z tym samym odczynnikiem wprowadzono wodne roztwory dwóch związków chemicznych. Do probówki I wprowadzono wodny roztwór winianu disodu (NaOOC–CH(OH)–CH(OH)–COONa), a do probówki II – wodny roztwór etanianu (octanu) sodu (CH3COONa). W warunkach doświadczenia obydwa wodne roztwory były bezbarwnymi cieczami.
Zaprojektuj doświadczenie, którego przebieg pozwoli na potwierdzenie, że roztwór winianu disodu wprowadzono do probówki I, a roztwór octanu sodu – do probówki II.
Uzupełnij schemat doświadczenia. Podkreśl nazwę odczynnika, który – po dodaniu do niego roztworów opisanych związków i wymieszaniu zawartości probówek – umożliwi zaobserwowanie różnic w przebiegu doświadczenia z udziałem winianu disodu i octanu sodu.
Opis zmian na podstawie przeprowadzonego doświadczenia potwierdzających obecność określonych substancji w probówkach. Zadanie 35.2. Arkusz CKE chemia maj 2017 rozszerzony (1 punkt)
Wykonano doświadczenie, w którym do dwóch probówek z tym samym odczynnikiem wprowadzono wodne roztwory dwóch związków chemicznych. Do probówki I wprowadzono wodny roztwór winianu disodu (NaOOC–CH(OH)–CH(OH)–COONa), a do probówki II – wodny roztwór etanianu (octanu) sodu (CH3COONa). W warunkach doświadczenia obydwa wodne roztwory były bezbarwnymi cieczami.
Zaprojektuj doświadczenie, którego przebieg pozwoli na potwierdzenie, że roztwór winianu disodu wprowadzono do probówki I, a roztwór octanu sodu – do probówki II.
Opisz zmiany możliwe do zaobserwowania w czasie doświadczenia, pozwalające na potwierdzenie, że do probówki I wprowadzono roztwór winianu disodu, a do probówki II – roztwór octanu sodu. Probówka I: Probówka II:
Określenie nazw związków chemicznych zidentyfikowanych w kolejnych etapach doświadczenia. Zadanie 36.1. Arkusz CKE chemia maj 2017 rozszerzony (1 punkt)
W trzech probówkach (I, II i III) znajdowały się wodne roztwory:
mocznika (CO(NH2)2), chlorku amonu (NH4Cl) i acetamidu (CH3CONH2).
W celu ich identyfikacji przeprowadzono dwie serie doświadczeń. W pierwszej serii doświadczeń do każdej probówki zanurzono żółty uniwersalny papierek wskaźnikowy. Zmianę barwy wskaźnika zaobserwowano tylko w probówce III. W drugiej serii doświadczeń do probówek I i II dodano wodny roztwór wodorotlenku sodu i ogrzano zawartości obu naczyń. U wylotu obu probówek wyczuwalny był ten sam charakterystyczny zapach. Następnie do probówek I i II dodano wodny roztwór azotanu(V) baru. Pojawienie się białego osadu zaobserwowano tylko w probówce I.
Podaj nazwy związków, które zidentyfikowano podczas przeprowadzonych doświadczeń. Probówka I: Probówka II: Probówka III:
Określenie odczynu roztworu wraz z uzasadnieniem równaniem procesu chemicznego. Zadanie 36.2. Arkusz CKE chemia maj 2017 rozszerzony (1 punkt)
W trzech probówkach (I, II i III) znajdowały się wodne roztwory:
mocznika (CO(NH2)2), chlorku amonu (NH4Cl) i acetamidu (CH3CONH2).
W celu ich identyfikacji przeprowadzono dwie serie doświadczeń. W pierwszej serii doświadczeń do każdej probówki zanurzono żółty uniwersalny papierek wskaźnikowy. Zmianę barwy wskaźnika zaobserwowano tylko w probówce III. W drugiej serii doświadczeń do probówek I i II dodano wodny roztwór wodorotlenku sodu i ogrzano zawartości obu naczyń. U wylotu obu probówek wyczuwalny był ten sam charakterystyczny zapach. Następnie do probówek I i II dodano wodny roztwór azotanu(V) baru. Pojawienie się białego osadu zaobserwowano tylko w probówce I.
Określ odczyn roztworu znajdującego się w probówce III i napisz w formie jonowej skróconej równanie reakcji, które potwierdzi wskazany odczyn. Odczyn roztworu: Równanie reakcji:
Zapis wzoru substancji o charakterystycznym zapachu oraz zapis równania reakcji chemicznej. Zadanie 36.3. Arkusz CKE chemia maj 2017 rozszerzony (1 punkt)
W trzech probówkach (I, II i III) znajdowały się wodne roztwory:
mocznika (CO(NH2)2), chlorku amonu (NH4Cl) i acetamidu (CH3CONH2).
W celu ich identyfikacji przeprowadzono dwie serie doświadczeń. W pierwszej serii doświadczeń do każdej probówki zanurzono żółty uniwersalny papierek wskaźnikowy. Zmianę barwy wskaźnika zaobserwowano tylko w probówce III. W drugiej serii doświadczeń do probówek I i II dodano wodny roztwór wodorotlenku sodu i ogrzano zawartości obu naczyń. U wylotu obu probówek wyczuwalny był ten sam charakterystyczny zapach. Następnie do probówek I i II dodano wodny roztwór azotanu(V) baru. Pojawienie się białego osadu zaobserwowano tylko w probówce I.
Napisz wzór substancji, której charakterystyczny zapach był wyczuwalny u wylotu probówek I i II, oraz napisz w formie jonowej skróconej równanie reakcji, w wyniku której w probówce I powstał biały osad. Wzór substancji: Równanie reakcji:
Wskazanie nazw substancji z uzasadnieniem zidentyfikowanych w wyniku przeprowadzenia dwóch prób. Zadanie 37. Arkusz CKE chemia maj 2017 rozszerzony (2 punkty)
W czterech nieopisanych naczyniach znajdują się oddzielnie: tyrozyna (Tyr), glicyna (Gly), biuret (H2N-CO-NH-CO-NH2) i alanina (Ala). Przeprowadzono doświadczenie, podczas którego wykonano dwie próby. Podczas pierwszej próby na czterech szkiełkach zegarkowych umieszczono niewielkie ilości wymienionych substancji i na każdą naniesiono kilka kropli stężonego wodnego roztworu kwasu azotowego(V). Wynik próby pozwolił na identyfikację jednej substancji. Podczas drugiej próby sporządzono wodne roztwory trzech pozostałych substancji i do każdego roztworu dodano świeżo wytrącony wodorotlenek miedzi(II). Wynik próby pozwolił na identyfikację drugiej substancji.
Uzupełnij poniższą tabelę. Podaj nazwę substancji, która została zidentyfikowana po przeprowadzeniu pierwszej próby, oraz nazwę substancji, która została zidentyfikowana po przeprowadzeniu drugiej próby. W każdym przypadku uzasadnij wybór substancji.
Zapis równań chemicznych reakcji prowadzących do utworzenia określonych form alaniny. Zadanie 38. Arkusz CKE chemia maj 2017 rozszerzony (2 punkty)
Do zakwaszonego roztworu alaniny dodawano kroplami wodny roztwór wodorotlenku sodu i mierzono pH mieszaniny reakcyjnej. Na poniższym wykresie zilustrowano zależność pH mieszaniny od objętości dodanego roztworu wodorotlenku sodu (w jednostkach umownych).
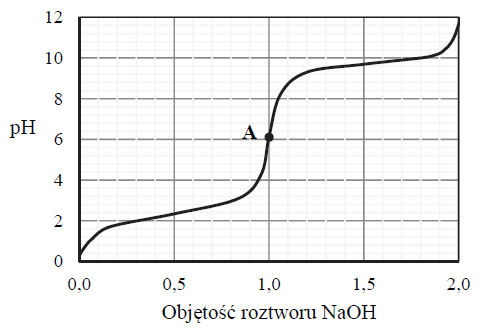
Aminokwasy istnieją głównie w formie jonów. W roztworach o niskim pH cząsteczka aminokwasu jest protonowana. W roztworach o wysokim pH aminokwas traci proton. Istnieje także pH, przy którym aminokwas występuje jako jon obojnaczy.
Na podstawie: J. McMurry, Chemia organiczna, Warszawa 2005.
Podczas opisanego miareczkowania przebiegły reakcje chemiczne zilustrowane schematem:
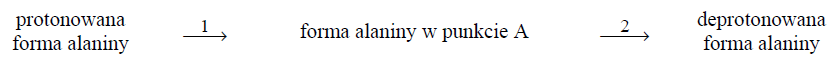
Napisz równania reakcji oznaczonych na schemacie numerami 1 i 2. Zastosuj wzory półstrukturalne (grupowe) form alaniny. Równanie reakcji 1: Równanie reakcji 2:
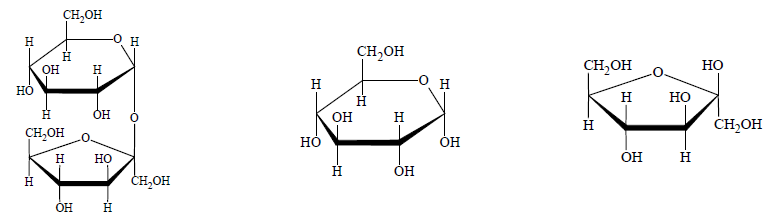
Wskazanie właściwego cukru na podstawie opisu jego zachowania się wobec określonego odczynnika. Zadanie 39. Arkusz CKE chemia maj 2017 rozszerzony (1 punkt)
Wodny roztwór pewnego cukru zmieszany w środowisku wodorowęglanu sodu (NaHCO3) z wodą bromową nie powoduje jej odbarwienia. Ponadto ten cukier daje pozytywny wynik próby Trommera i próby Tollensa.
Wybierz i podkreśl wzór cukru, którego może dotyczyć powyższy opis.