Zapis równania reakcji chemicznej w formie jonowej skróconej oraz wybór właściwej probówki. Zadanie 9.1. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
W dwóch probówkach oznaczonych numerami I i II umieszczono jednakową ilość wiórków magnezowych o tym samym stopniu rozdrobnienia. Następnie do probówek wprowadzono jednakowe objętości roztworów o tej samej temperaturze:
– do probówki I – kwas solny o pH = 1
– do probówki II – wodny roztwór kwasu siarkowego(VI) o stężeniu 0,1 mol·dm–3 .
Przebieg doświadczenia zilustrowano poniższym rysunkiem.
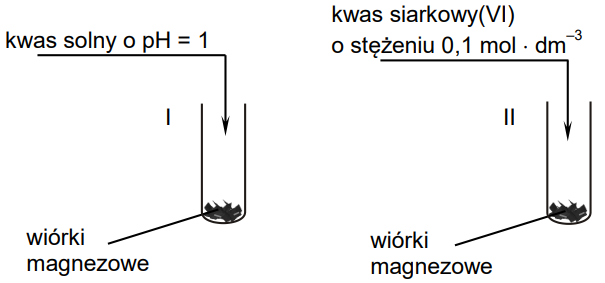
Podczas opisanego doświadczenia w każdej probówce wiórki magnezowe uległy całkowitemu roztworzeniu i powstały klarowne, bezbarwne roztwory, ale w jednej z probówek reakcja przebiegła szybciej.
Napisz w formie jonowej skróconej równanie reakcji, która zaszła podczas opisanego doświadczenia w obu probówkach. Wskaż numer probówki (I albo II), w której wiórki magnezowe roztworzyły się szybciej. Równanie reakcji: Wiórki magnezowe roztworzyły się szybciej w probówce numer
Wybór właściwych określeń dotyczących przebiegu doświadczenia chemicznego. Zadanie 9.2. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
W dwóch probówkach oznaczonych numerami I i II umieszczono jednakową ilość wiórków magnezowych o tym samym stopniu rozdrobnienia. Następnie do probówek wprowadzono jednakowe objętości roztworów o tej samej temperaturze:
– do probówki I – kwas solny o pH = 1
– do probówki II – wodny roztwór kwasu siarkowego(VI) o stężeniu 0,1 mol·dm–3 .
Przebieg doświadczenia zilustrowano poniższym rysunkiem.

Podczas opisanego doświadczenia w każdej probówce wiórki magnezowe uległy całkowitemu roztworzeniu i powstały klarowne, bezbarwne roztwory, ale w jednej z probówek reakcja przebiegła szybciej.
Uzupełnij poniższe zdanie – wybierz i zaznacz jedną odpowiedź spośród podanych w każdym nawiasie. Stężenie molowe roztworów obu kwasów było (równe / różne), a stężenie jonów H+ w tych roztworach było (równe / różne), dlatego opisane doświadczenie pozwoliło określić wpływ (stężenia molowego / pH) roztworów użytych kwasów na szybkość reakcji.
Wybór czynności pozwalającej na wyodrębnienie składnika z mieszaniny. Zadanie 10. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
W dwóch probówkach oznaczonych numerami I i II umieszczono jednakową ilość wiórków magnezowych o tym samym stopniu rozdrobnienia. Następnie do probówek wprowadzono jednakowe objętości roztworów o tej samej temperaturze:
– do probówki I – kwas solny o pH = 1
– do probówki II – wodny roztwór kwasu siarkowego(VI) o stężeniu 0,1 mol·dm–3 .
Przebieg doświadczenia zilustrowano poniższym rysunkiem.

Podczas opisanego doświadczenia w każdej probówce wiórki magnezowe uległy całkowitemu roztworzeniu i powstały klarowne, bezbarwne roztwory, ale w jednej z probówek reakcja przebiegła szybciej.
Którą czynność należy wykonać w celu wyodrębnienia z mieszaniny poreakcyjnej jonowego produktu otrzymanego w probówce I? Zaznacz właściwą odpowiedź spośród podanych. A. Sączenie B. Dekantacja C. Odwirowanie D. Odparowanie pod wyciągiem
Zapis w formie jonowej skróconej równania reakcji chemicznej oraz wybór właściwego odczynnika. Zadanie 12.1. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
W trzech probówkach (I–III) umieszczono wodne roztwory soli potasu zawierających chrom na VI stopniu utlenienia. Zawartość probówki III zakwaszono. Następnie do każdej probówki dodano jeden odczynnik wybrany z poniższej listy:
– wodny roztwór wodorotlenku potasu
– wodny roztwór azotanu(V) sodu
– wodny roztwór azotanu(V) srebra(I)
– wodny roztwór siarczanu(IV) potasu.
Schemat doświadczenia i opis wyglądu zawartości probówek I–III przed reakcją i po jej zakończeniu przedstawiono w poniższej tabeli.
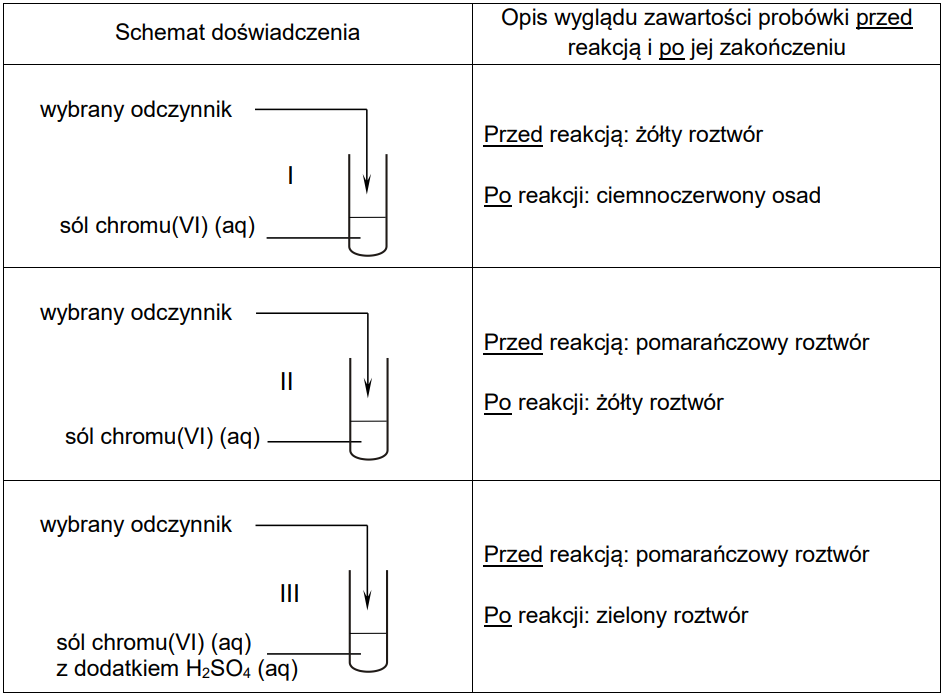
Napisz w formie jonowej skróconej równanie reakcji zachodzącej w probówce I po dodaniu wybranego odczynnika do roztworu soli chromu(VI) oraz napisz nazwę lub wzór odczynnika, który dodano do probówki II w opisanym doświadczeniu. Równanie reakcji zachodzącej w probówce I: Nazwa lub wzór odczynnika dodanego do probówki II:
Zapis w formie jonowej skróconej równania reakcji chemicznej. Zadanie 12.2. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
W trzech probówkach (I–III) umieszczono wodne roztwory soli potasu zawierających chrom na VI stopniu utlenienia. Zawartość probówki III zakwaszono. Następnie do każdej probówki dodano jeden odczynnik wybrany z poniższej listy:
– wodny roztwór wodorotlenku potasu
– wodny roztwór azotanu(V) sodu
– wodny roztwór azotanu(V) srebra(I)
– wodny roztwór siarczanu(IV) potasu.
Schemat doświadczenia i opis wyglądu zawartości probówek I–III przed reakcją i po jej zakończeniu przedstawiono w poniższej tabeli.

Napisz w formie jonowej skróconej równanie reakcji zachodzącej w probówce III po dodaniu wybranego odczynnika do roztworu soli chromu(VI) z dodatkiem H2SO4.
Wybór właściwych odpowiedzi dotyczących przeprowadzonego doświadczenia. Zadanie 12.3. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
W trzech probówkach (I–III) umieszczono wodne roztwory soli potasu zawierających chrom na VI stopniu utlenienia. Zawartość probówki III zakwaszono. Następnie do każdej probówki dodano jeden odczynnik wybrany z poniższej listy:
– wodny roztwór wodorotlenku potasu
– wodny roztwór azotanu(V) sodu
– wodny roztwór azotanu(V) srebra(I)
– wodny roztwór siarczanu(IV) potasu.
Schemat doświadczenia i opis wyglądu zawartości probówek I–III przed reakcją i po jej zakończeniu przedstawiono w poniższej tabeli.

Uzupełnij poniższe zdania – wybierz i zaznacz jedną odpowiedź spośród podanych w każdym nawiasie. Reakcja redoks przebiegła w probówce (I / II / III). Sól chromu(VI) pełni w tej przemianie funkcję (reduktora / utleniacza).
Zapis równań reakcji utleniania oraz redukcji z udziałem związków manganu. Zadanie 13. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
Wykonano doświadczenie zilustrowane poniższym schematem.
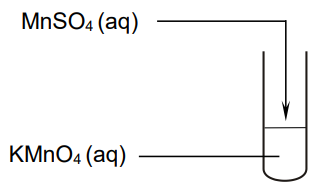
Po zakończeniu reakcji w probówce widoczne były bezbarwny roztwór i brunatny osad.
Napisz w formie jonowej skróconej, z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy), równania procesów redukcji i utleniania zachodzących podczas opisanej przemiany. Uwzględnij, że reakcja zachodzi w środowisku obojętnym. Równanie procesu redukcji: Równanie procesu utleniania:
Wskazanie najsłabszego oraz najsilniejszego reduktora na podstawie doświadczenia z blaszkami metali. Zadanie 14.1. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
O trzech metalach umownie oznaczonych symbolami A, X i Z wiadomo, że tworzą wyłącznie kationy o wzorach X+, A2+, Z3+. Stwierdzono, że właściwości utleniające kationów tych metali maleją w szeregu: X+, A2+, Z3+.
Przeprowadzono doświadczenie z udziałem metali Z i X oraz wodnych roztworów soli, w których były obecne jony X+ i A2+. Schemat doświadczenia przedstawiono poniżej.
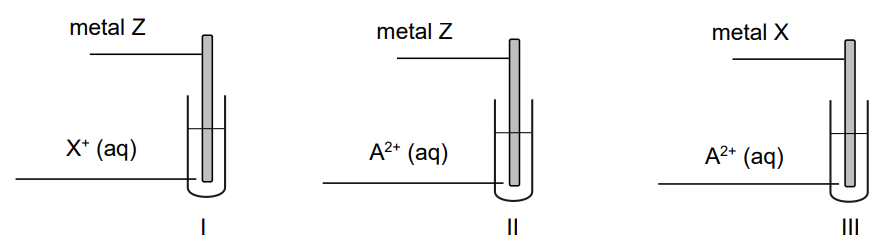
Wskaż metal, który jest najsłabszym reduktorem, oraz metal, który jest najsilniejszym reduktorem. Użyj symboli A, X albo Z. Najsłabszy reduktor: Najsilniejszy reduktor:
Wybór właściwej probówki oraz zapis równań reakcji chemicznych. Zadanie 14.2. Arkusz CKE chemia maj 2022 rozszerzony (2 punkty)
O trzech metalach umownie oznaczonych symbolami A, X i Z wiadomo, że tworzą wyłącznie kationy o wzorach X+, A2+, Z3+. Stwierdzono, że właściwości utleniające kationów tych metali maleją w szeregu: X+, A2+, Z3+.
Przeprowadzono doświadczenie z udziałem metali Z i X oraz wodnych roztworów soli, w których były obecne jony X+ i A2+. Schemat doświadczenia przedstawiono poniżej.

W jednej probówce nie zaobserwowano objawów reakcji.
Napisz numer probówki, w której nie zaobserwowano objawów reakcji. Napisz w formie jonowej skróconej równania dwóch reakcji, które przebiegły podczas przeprowadzonego doświadczenia. Użyj symboli A, X, Z. Numer probówki: Równania reakcji:
Obliczanie pH roztworu kwasu azotowego(V) po rozcieńczeniu. Zadanie 15. Arkusz CKE chemia maj 2022 rozszerzony (2 punkty)
Do 1,00 dm3 wody destylowanej wprowadzono 90,0 cm3 wodnego roztworu kwasu azotowego(V) o stężeniu 5,00% masowych i gęstości równej 1,03 g·cm–3.
Na podstawie: W. Sawicka, A. Janich-Kilian, W. Cejner-Mania, G. Urbańczyk, Tablice chemiczne, Gdańsk 2015.
Oblicz pH otrzymanego roztworu kwasu azotowego(V). W obliczeniach przyjmij, że objętość powstałego roztworu jest sumą objętości użytych roztworu i wody. Wynik zaokrąglij do drugiego miejsca po przecinku
Ocena poprawności zdań dotyczących doświadczenia z udziałem roztworów - kwasu azotowego(V) oraz KOH. Zadanie 16. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
Zmieszano wodny roztwór kwasu azotowego(V) z wodnym roztworem wodorotlenku potasu w stosunku objętościowym VHNO3 : VKOH = 2 : 1. Otrzymano klarowny roztwór o pH = 7.
Oceń, czy podane poniżej informacje są prawdziwe. Zaznacz P, jeśli informacja jest prawdziwa, albo F – jeśli jest fałszywa. 1. Stężenie molowe roztworu kwasu azotowego(V) było dwa razy mniejsze niż stężenie molowe roztworu wodorotlenku potasu. 2. Po odparowaniu wody z otrzymanego roztworu pozostanie ciało stałe, w którym stosunek liczby jonów NO3– i K+ 𝑛NO3− : 𝑛K+ = 2 : 1.
Zapis równania reakcji chemicznej zgodnie z teorią Brønsteda. Zadanie 17.1. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
Przygotowano wodne roztwory trzech różnych soli – CH3COONa, NaNO2, NaF – o takim samym stężeniu molowym. Odczyn wszystkich przygotowanych roztworów był zasadowy, ale pH każdego roztworu było inne.
Wpisz do poniższego schematu wzory odpowiednich drobin, tak aby powstało równanie potwierdzające zasadowy odczyn roztworu azotanu(III) sodu – zastosuj definicję kwasu i zasady Brønsteda.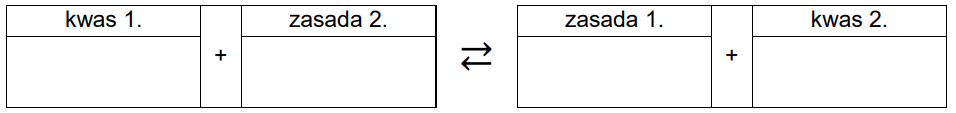
Zapis wzoru soli, której roztwór miał najwyższe pH. Zadanie 17.2. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
Przygotowano wodne roztwory trzech różnych soli – CH3COONa, NaNO2, NaF – o takim samym stężeniu molowym. Odczyn wszystkich przygotowanych roztworów był zasadowy, ale pH każdego roztworu było inne.
Napisz wzór lub nazwę tej soli, której wodny roztwór miał najwyższe pH.
Wskazanie związku chemicznego, którego roztwór poddano miareczkowaniu alkacymetrycznemu. Zadanie 18.1. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
W celu wyznaczenia dokładnego stężenia pewnej zasady przeprowadzono następujące doświadczenie. Do 60,0 cm3 badanego roztworu (KOH albo NH3 o stężeniu około 0,1 mol·dm−3) dodawano powoli wodny roztwór HCl o stężeniu 0,10 mol·dm−3 i mierzono pH mieszaniny reakcyjnej. Otrzymaną zależność pH roztworu miareczkowanego od objętości dodanego kwasu przedstawiono na poniższym wykresie.
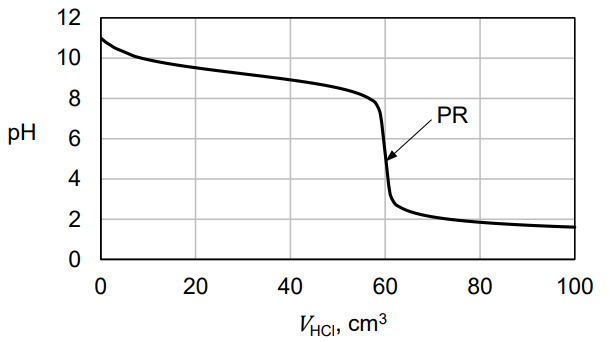
Po dodaniu takiej objętości roztworu HCl, w jakiej ilość kwasu jest równoważna początkowej ilości zasady w badanym roztworze, w układzie zostaje osiągnięty punkt równoważnikowy (PR).
Rozstrzygnij, czy w opisanym doświadczeniu użyto roztworu KOH czy NH3. Odpowiedź uzasadnij. Rozstrzygnięcie: Uzasadnienie: