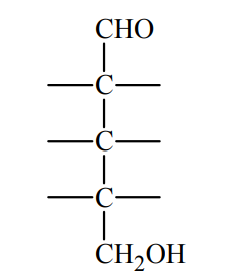
Zapis równania reakcji próby jodoformowej. Zadanie 27a. Arkusz CKE chemia maj 2010 rozszerzony (1 punkt)
Reakcją pozwalającą wykryć w związkach organicznych grupę
![]()
jest próba jodoformowa. Polega ona na reakcji związku organicznego z jodem w obecności NaOH w podwyższonej temperaturze. Po oziębieniu mieszaniny poreakcyjnej do temperatury pokojowej powstaje żółty, krystaliczny osad o charakterystycznym zapachu.
Jeżeli badanym związkiem jest propanon (aceton), produktami próby jodoformowej są: trijodometan, etanian sodu (octan sodu), jodek sodu i woda.
Korzystając z powyższych informacji, uzupełnij schemat, tak aby przedstawiał równanie opisanej reakcji w formie cząsteczkowej (wpisz wzory produktów reakcji i odpowiednie współczynniki stechiometryczne).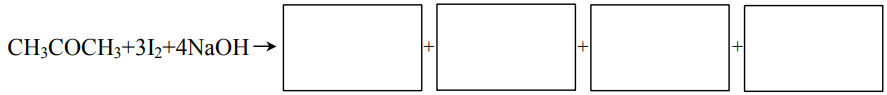
Zapis wzoru związku chemicznego stanowiącego osad o określonej barwie oraz zapachu. Zadanie 27b. Arkusz CKE chemia maj 2010 rozszerzony (1 punkt)
Reakcją pozwalającą wykryć w związkach organicznych grupę
![]()
jest próba jodoformowa. Polega ona na reakcji związku organicznego z jodem w obecności NaOH w podwyższonej temperaturze. Po oziębieniu mieszaniny poreakcyjnej do temperatury pokojowej powstaje żółty, krystaliczny osad o charakterystycznym zapachu.
Jeżeli badanym związkiem jest propanon (aceton), produktami próby jodoformowej są: trijodometan, etanian sodu (octan sodu), jodek sodu i woda.
Napisz wzór tego produktu przemiany, który tworzy żółty, krystaliczny osad o charakterystycznym zapachu.
Wskazanie, czy próba jodoformowa może posłużyć do odróżnienia acetonu od acetaldehydu. Zadanie 27c. Arkusz CKE chemia maj 2010 rozszerzony (1 punkt)
Reakcją pozwalającą wykryć w związkach organicznych grupę
![]()
jest próba jodoformowa. Polega ona na reakcji związku organicznego z jodem w obecności NaOH w podwyższonej temperaturze. Po oziębieniu mieszaniny poreakcyjnej do temperatury pokojowej powstaje żółty, krystaliczny osad o charakterystycznym zapachu.
Jeżeli badanym związkiem jest propanon (aceton), produktami próby jodoformowej są: trijodometan, etanian sodu (octan sodu), jodek sodu i woda.
Napisz, czy próba jodoformowa pozwala na odróżnienie propanonu (acetonu) od etanalu, i uzasadnij swoje stanowisko.
Ocena poprawności zdań dotyczących amin. Zadanie 28. Arkusz CKE chemia maj 2010 rozszerzony (2 punkty)
Oceń prawdziwość poniższych zdań i uzupełnij tabelę. Wpisz literę P, jeżeli uznasz zdanie za prawdziwe, lub literę F, jeżeli uznasz je za fałszywe. 1. Zasadowy charakter amin związany jest z obecnością wolnej pary elektronowej atomu azotu grupy aminowej, umożliwiającej przyłączenie jonu H+. 2. Wartości temperatury wrzenia amin alifatycznych są wyższe niż n-alkanów o porównywalnej masie molowej, gdyż między cząsteczkami amin tworzą się
wiązania wodorowe.
3. Fenyloaminę (anilinę) otrzymuje się przez utlenienie nitrobenzenu.
Zapis wzoru sumarycznego oraz grupowego związku chemicznego. Zadanie 29ab. Arkusz CKE chemia maj 2010 rozszerzony (2 punkty)
Pewien dwufunkcyjny związek organiczny ma masę molową równą 90 g/mol. W jego cząsteczce stosunek liczby atomów węgla, wodoru i tlenu wynosi 1:2:1.
a) Napisz wzór sumaryczny opisanego związku. b) Wiedząc, że związek ten w roztworze wodnym dysocjuje z odszczepieniem jonu wodorowego oraz że jego cząsteczka jest achiralna, narysuj wzór półstrukturalny (grupowy) tego związku.
Rysowanie wzoru jonu aminokwasu dominującego przy określonej wartości pH roztworu. Zadanie 30. Arkusz CKE chemia maj 2010 rozszerzony (1 punkt)
Punkt izoelektryczny (pI) aminokwasu to pH roztworu, w którym cząsteczki tego aminokwasu występują głównie w formie jonów obojnaczych. Kwas 2-aminobutanodiowy (asparaginowy) jest dikarboksylowym aminokwasem o wzorze sumarycznym C4H7O4N. Jego punkt izoelektryczny pI = 2,87.
Narysuj wzór półstrukturalny (grupowy) jonu, który jest dominującą formą tego aminokwasu w roztworze o pH = 1.
Wybór właściwych wyrazów dotyczących doświadczenia z udziałem glukozy oraz fruktozy. Zadanie 31. Arkusz CKE chemia maj 2010 rozszerzony (3 punkty)
Badano działanie świeżo strąconego wodorotlenku miedzi(II) na próbki wodnych roztworów glukozy i fruktozy. Używając uniwersalnego papierka wskaźnikowego, zbadano także odczyn wodnych roztworów obu związków. Obserwacje zestawiono w tabeli.

Korzystając z podanej informacji, uzupełnij poniższe zdania, wpisując w odpowiedniej formie gramatycznej określenia wybrane z poniższego zestawu. związek kompleksowy, kwasowy, zasadowy, obojętny, utleniający, redukujący, hydroksylowa, alkilowa, aldehydowa, ketonowa, aldoza, ketoza 1. Glukoza i fruktoza są białymi, krystalicznymi substancjami stałymi. Bardzo dobrze rozpuszczają się w wodzie. Odczyn ich wodnych roztworów jest . 2. Reakcja glukozy z wodorotlenkiem miedzi(II) prowadzona na zimno potwierdza obecność w jej cząsteczce kilku grup związanych z sąsiednimi atomami węgla. Glukoza w reakcji z wodorotlenkiem miedzi(II) przeprowadzanej na gorąco 3. Fruktoza, podobnie jak glukoza, tworzy z wodorotlenkiem miedzi(II) rozpuszczalne , dlatego obserwujemy powstanie szafirowego roztworu. Wynik reakcji fruktozy z wodorotlenkiem miedzi(II) prowadzonej w podwyższonej temperaturze wskazuje, że związek ten ma także właściwości , mimo że fruktoza zaliczana jest do .
wykazuje właściwości , co wiąże się z obecnością w jej cząsteczce grupy .
Projektowanie doświadczenia, którego przebieg pozwoli odróżnić trójglicerydy. Zadanie 32ab. Arkusz CKE chemia maj 2010 rozszerzony (2 punkty)
Zaprojektuj doświadczenie, którego przebieg pozwoli na rozróżnienie roztworów dwóch triglicerydów: trioleinianu glicerolu i tristearynianiu glicerolu.
a) Uzupełnij schemat doświadczenia, wpisując nazwę odczynnika wybranego spośród następujących: Zgodnie z powyższym schematem do probówki I wprowadzono roztwór trioleinianu glicerolu w CCl4, a do probówki II roztwór tristearynianu glicerolu w tym samym rozpuszczalniku. Następnie do obu probówek dodano wybrany odczynnik i ich zawartość energicznie wymieszano. b) Napisz, co potwierdzi obecność roztworu trioleinianu glicerolu w probówce I i roztworu tristearynianu glicerolu w probówce II (porównaj przebieg doświadczenia w obu probówkach). Probówka I: Probówka II:
– stężony wodny roztwór wodorotlenku sodu NaOH (aq)
– woda bromowa Br2 (aq)
– rozcieńczony wodny roztwór kwasu etanowego (octowego) CH3COOH (aq)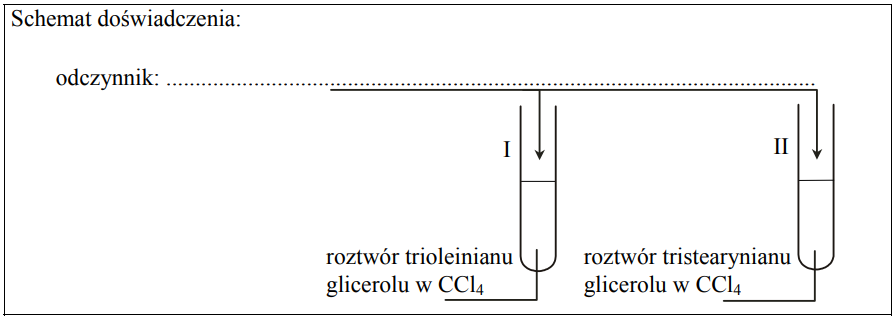
Zapis równania reakcji polimeryzacji metakrylan metylu. Zadanie 33. Arkusz CKE chemia maj 2010 rozszerzony (1 punkt)
Ester metylowy kwasu 2-metylopropenowego (metakrylan metylu) jest monomerem poli(metakrylanu metylu).
Dokończ, stosując wzory półstrukturalne (grupowe), równanie reakcji polimeryzacji tego estru.
Rysowanie wzoru Fischera będącego enancjomerem D-arabinozy. Zadanie 34. Arkusz CKE chemia maj 2010 rozszerzony (1 punkt)
Poniżej przedstawiono wzór D-arabinozy (w projekcji Fischera).
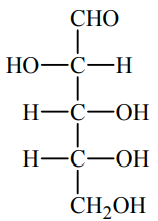
Uzupełnij poniższy schemat, tak aby otrzymać wzór enancjomeru D-arabinozy.