Skład mieszaniny można wyrazić za pomocą ułamków molowych. Ułamek molowy składnika A, 𝑥n(A), to iloraz liczby moli tego składnika, 𝑛A, i sumy liczb moli wszystkich składników mieszaniny. Np. dla mieszaniny trójskładnikowej A, B, C:
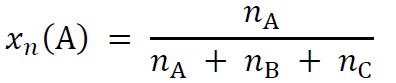
W pewnych warunkach ciśnienia i temperatury sporządzono mieszaninę dwóch gazowych substancji: wodoru i jodu, w zamkniętym reaktorze o objętości V = 20,0 dm3.
Po zainicjowaniu procesu opisanego równaniem:
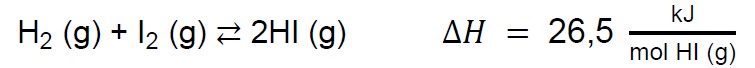
uzyskano w stanie równowagi mieszaninę o składzie: 𝑚(I2) = 381 g, 𝑛(HI) = 1,50 mol oraz pewną ilość wodoru. Sumaryczna liczba moli wszystkich składników uzyskanej mieszaniny równowagowej wynosiła 6,00 moli.
Oceń prawdziwość poniższych zdań. Zaznacz P, jeśli zdanie jest prawdziwe, albo F – jeśli jest fałszywe.
1. Wraz ze wzrostem temperatury, w warunkach izobarycznych, wartość stałej równowagi reakcji syntezy jodowodoru będzie malała.
2. Wraz ze wzrostem temperatury, w warunkach izobarycznych, wartość ułamka molowego jodowodoru w mieszaninie równowagowej będzie wzrastała.
3. Szybkość reakcji H2 (g) + I2 (g) → 2HI (g) na początku eksperymentu jest większa od szybkości reakcji 2HI (g) → H2 (g) + I2 (g) mierzonej w tym samym momencie.