Obliczanie ciśnienia mieszaniny poreakcyjnej po zmianie objętości w stałej temperaturze (równanie Clapeyrona)
Zgodnie z prawem Boyle’a, w stałej temperaturze ciśnienie próbki gazu jest odwrotnie proporcjonalne do jego objętości.
Na podstawie: P. W. Atkins, Chemia fizyczna, Warszawa 2012.
Izomery to związki chemiczne mające taki sam wzór sumaryczny, ale różny strukturalny. W reaktorze o pojemności 1 m3, w pewnej temperaturze T, pod ciśnieniem 1000 hPa znajdował się propen (CH3–CH=CH2). Związek ten przekształcono w izomeryczny względem niego cyklopropan, co ilustruje równanie chemiczne:
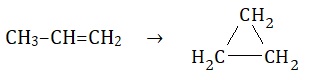
Po zakończeniu doświadczenia mieszaninę poreakcyjną zawierającą 90% objętościowych produktu oraz 10% nieprzereagowanego substratu przepompowano do naczynia o pojemności 400 dm3 i doprowadzono do wyjściowej temperatury T.
Oblicz, jakie ciśnienie miała uzyskana w opisany sposób mieszanina? Wynik podaj w MPa (megapaskalach) z dokładnością do dwóch cyfr znaczących. Rozwiązanie tego zadania dostępne jest nieodpłatnie pod poniższym linkiem: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone