Metaliczna cyna ulega reakcji ze stężonym kwasem solnym. Podczas takiej przemiany powstają między innymi dwudodatnie jony, które w kontakcie z tlenem, w środowisku kwasowym utleniają się do jonów cyny(IV). W reakcji z roztworami wodorotlenków litowców cyna tworzy dwuujemny jon kompleksowy o liczbie koordynacyjnej równej sześć. Podczas przebiegu wymienionych reakcji chemicznych z udziałem metalicznej cyny wydziela się również bezbarwny, bezwonny, łatwopalny produkt gazowy.
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2010.
Przeprowadzono doświadczenie chemiczne, którego schemat ilustruje rysunek poniżej.
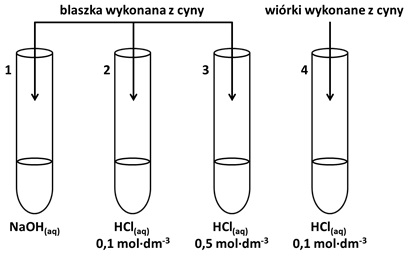
Objętość początkowa każdego ze znajdujących się w probówkach roztworów była taka sama, podobnie jak masa wprowadzonej do nich cyny. Przed rozpoczęciem doświadczenia temperatura każdego z reagentów wynosiła 22 oC, a po jego zakończeniu stwierdzono, że uzyskana w każdej z probówek zawartość ma wyraźnie wyższą temperaturę niż początkowa.
Oceń poprawność poniższych zdań dotyczących reakcji, jakie przebiegły w probówkach o numerach 2, 3 oraz 4. Wpisz literę „P” (prawda) lub literę „F” (fałsz).
1. Opisane trzy przemiany są procesami egzotermicznymi, dlatego ich szybkość początkowa będzie mniejsza w temperaturze 60 oC niż w temperaturze 22 oC.
2. Gdy reakcji ulegnie połowa początkowej ilości cyny wprowadzonej do probówki nr 2, wówczas w tym samym czasie, w naczyniu nr 4 reakcji ulegnie ponad połowa początkowej ilości cyny.
3. Reakcja przebiegła szybciej w probówce oznaczonej cyfrą 2, niż w probówce oznaczonej cyfrą 3.
© dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone