W określonych warunkach wodoroaniony mogą być klasyfikowane jako kwasy Brønsteda. Miarą mocy tych kwasów jest wielkość zwana stałą równowagi dysocjacji kwasowej (Ka). W tabeli poniżej zebrano dane na temat wartości stałych dysocjacji (Ka) w temperaturze 25 oC kilku wybranych wodoroanionów.
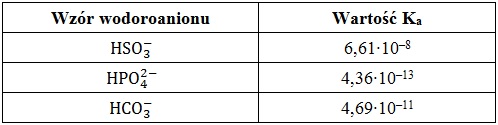
Na podstawie: K.-H. Lautenschläger, W. Schröter, A. Wanninger, Nowoczesne kompendium chemii, Warszawa 2018. oraz W. Mizerski, Tablice chemiczne, Warszawa 2013.
W celu odróżnienia probówek zawierających wodne roztwory K2HPO4 oraz KHCO3 do zawartości każdej z nich wprowadzono jeden z odczynników:
Ba(OH)2(aq), KOH(aq), KHSO4(aq).
Zamieszczone fotografie ilustrują zawartość naczyń praktycznie natychmiast po umieszczeniu w nich wybranego odczynnika:

Zapisz wzór jednego spośród trzech wyżej wymienionych odczynników, którego należy użyć, w celu odróżnienia opisanych roztworów wodorosoli. Podaj numer tej probówki, w której przebiegła reakcja chemiczna stanowiąca podstawę odróżnienia roztworów wodorosoli i napisz jej równanie w formie jonowej skróconej. Uzupełnij tabelę.

© dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone