Loperamid jest popularnym środkiem leczniczym stosowanym w objawowej terapii biegunki. Uproszczony wzór chemiczny cząsteczki tego związku ilustruje rysunek:
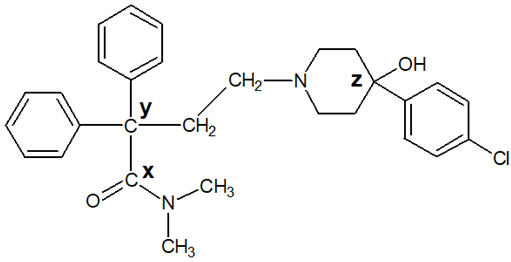
Na podstawie: D. Steinhilber, M. Schubert-Zsilavecz, H. J. Roth, Chemia medyczna. Cele leków. Substancje czynne. Biologia chemiczna, Wrocław 2012.
Przeprowadzono doświadczenie chemiczne, którego schemat ilustruje rysunek:
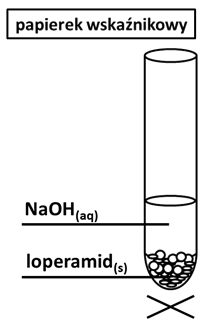
Podczas tego eksperymentu zaobserwowano, że zwilżony wodą uniwersalny papierek wskaźnikowy zmienił barwę na kolor niebieski oraz wyczuwalny był „rybi” zapach. Za opisane obserwacje odpowiedzialny był lotny związek chemiczny o temperaturze wrzenia 6,9 oC (ciśnienie normalne), stanowiący produkt hydrolizy wiązania amidowego znajdującego się w cząsteczce loperamidu.
Podkreśl wyrażenia w nawiasach tak, aby powstały zdania prawdziwe.
Opisany lotny związek chemiczny ma izomer o (wyższej / niższej) od niego temperaturze wrzenia. Można zatem wnioskować, że rzędowość tego izomeru konstytucyjnego jest (większa / mniejsza) niż rzędowość powstałego związku o temperaturze wrzenia 6,9 oC. Między cząsteczkami wymienionych izomerycznych substancji chemicznych (mogą / nie mogą) tworzyć się wiązania wodorowe, ponieważ w cząsteczce każdej z nich znajduje się pierwiastek o (małej / dużej) wartości elektroujemności, połączony z atomem wodoru i zawierający wolną parę elektronową.
© dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone