Obliczanie początkowego stężenia bromometanu. Zadanie 6. Arkusz CKE chemia czerwiec 2023 rozszerzony (2 punkty)
W roztworze alkoholowo-wodnym zawierającym bromometan oraz wodorotlenek sodu przebiega reakcja opisana równaniem:
CH3Br + OH− → CH3OH + Br−
Zależność szybkości tej reakcji od stężeń reagentów przedstawia równanie kinetyczne:
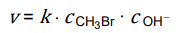
W temperaturze 55 °C wartość k jest równa 2,14·10–2 dm3 · mol–1 · s–1.
Na podstawie: R.T. Morrison, R.N. Boyd, Chemia organiczna, Warszawa 1996.
Reakcję CH3Br z NaOH prowadzono w temperaturze 55 °C. Po pewnym czasie stężenie jonów OH− – wskutek przebiegu reakcji chemicznej – zmalało z 0,060 mol · dm–3 do wartości 0,050 mol · dm–3, a szybkość reakcji wynosiła 1,07·10–5 · mol dm–3 · s–1.
Oblicz początkowe stężenie molowe bromometanu.