Obliczanie masy hydratu oraz roztworu siarczanu(VI) magnezu w celu uzyskania nasyconego roztworu soli (rozpuszczalność substancji)
W temperaturze 20 oC rozpuszczalność siarczanu(VI) magnezu-woda (1/7) ma wartość równą 105,5 g/100 g wody.
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Rozpuszczając w wodzie w danych warunkach określoną masę hydratu można uzyskać nasycony roztwór soli bezwodnej.
Oblicz, jaką masę opisanego hydratu oraz 15% roztworu siarczanu(VI) magnezu należy zmieszać, aby w temperaturze 20 oC uzyskać 845 g nasyconego roztworu MgSO4? Rozwiązanie tego zadania dostępne jest nieodpłatnie pod poniższym linkiem: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie masy hydratu oraz wody destylowanej w celu uzyskania nasyconego roztworu soli siarczanu(VI) magnezu (rozpuszczalność substancji)
W temperaturze 20 oC rozpuszczalność siarczanu(VI) magnezu-woda (1/7) ma wartość równą 105,5 g/100 g wody.
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Rozpuszczając w wodzie w danych warunkach określoną masę hydratu można uzyskać nasycony roztwór soli bezwodnej.
Oblicz, jaką masę opisanego hydratu oraz wody destylowanej należy zmieszać, aby w temperaturze 20 oC uzyskać 244 g nasyconego roztworu MgSO4? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie stężenia molowego jonów chlorkowych w roztworze powstałym z udziałem hydratu chlorku żelaza(III)
W temperaturze 20 oC rozpuszczalność sześciowodnego chlorku żelaza(III) ma wartość 395 g/ 100g wody.
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
W zlewce z wodą destylowaną rozpuszczono taką ilość opisanego hydratu chlorku żelaza(III), że uzyskano 25 g nasyconego w temperaturze 20 oC roztworu soli bezwodnej. Następnie w kolbie miarowej o pojemności 50 cm3 umieszczono 10 g opisanego roztworu i uzupełniono wodą destylowaną „do kreski”, a do pozostałej w zlewce substancji dodano 100 cm3 wody destylowanej.
Oblicz stężenie molowe jonów chlorkowych w docelowym roztworze, jaki znajdował się w kolbie miarowej. Wynik podaj z dokładnością do trzech cyfr znaczących © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie procentu wagowego jonów żelaza(III) w roztworze uzyskanym z wykorzystaniem hydratu chlorku żelaza(III)
W temperaturze 20 oC rozpuszczalność sześciowodnego chlorku żelaza(III) ma wartość 395 g/ 100g wody.
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
W zlewce z wodą destylowaną rozpuszczono taką ilość opisanego hydratu chlorku żelaza(III), że uzyskano 25 g nasyconego w temperaturze 20 oC roztworu soli bezwodnej. Następnie w kolbie miarowej o pojemności 50 cm3 umieszczono 10 g opisanego roztworu i uzupełniono wodą destylowaną „do kreski”, a do pozostałej w zlewce substancji dodano 100 cm3 wody destylowanej.
Oblicz, jaki procent masy znajdującego się w zlewce docelowego roztworu stanowiły jony żelaza(III)? Wynik podaj z dokładnością do drugiego miejsca po przecinku. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie masy pozostałego roztworu po odparowaniu wody oraz wykrystalizowaniu hydratu
Hydrat o wzorze CuSO4·5H2O w temperaturze 40 oC ma rozpuszczalność 53,2 g/100 g wody. Przygotowano 200 g nasyconego w 40 oC roztworu soli bezwodnej. Po pewnym czasie stwierdzono, że w opisanych warunkach temperaturowych masa zawartości naczynia zmalała o 10 g, a na jego dnie pojawiły się kryształki opisanego hydratu, które odsączono.
Oblicz masę roztworu pozostałego po odsączeniu wykrystalizowanego hydratu. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określanie wzoru sumarycznego hydratu jodku sodu na podstawie jego rozpuszczalności oraz soli bezwodnej
W temperaturze 20 oC wyrażona w g/100 g wody rozpuszczalność pewnego hydratu jodku sodu oraz soli bezwodnej wynoszą odpowiednio 383 g oraz 177,4 g. W tej samej temperaturze nasycone roztwory wodne uzyskane w wyniku rozpuszczenia hydratu lub jego soli bezwodnej charakteryzują się identyczną wartością stężenia procentowego.
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013 oraz R. Szczypiński, Projektowanie doświadczeń chemicznych. Dla maturzystów i nie tylko, Warszawa 2019.
Wykonując niezbędne obliczenia ustal wzór sumaryczny opisanego w informacji wprowadzającej hydratu jodku sodu. Rozwiązanie tego zadania dostępne jest nieodpłatnie pod poniższym linkiem: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie ilości wody, jaka pozwoliłaby na rozpuszczenie określonej porcji związku trudno rozpuszczalnego (iloczyn rozpuszczalności)
W temperaturze 25 ⁰C iloczyn rozpuszczalności wodorotlenku magnezu ma wartość 7,94∙10−12, a węglanu wapnia 3,31∙10–9.
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Oblicz minimalną objętość wody destylowanej, jaką należałoby dodać do 100 cm3 nasyconego w temperaturze 25 ⁰C roztworu wodorotlenku magnezu, aby możliwe było rozpuszczenie dodatkowej porcji tego związku chemicznego o masie 5,8 mg. Wynik podaj w centymetrach sześciennych, z dokładnością do cyfry jedności. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie rozpuszczalności wodorotlenku w roztworze o odczynie zasadowym (iloczyn rozpuszczalności)
W temperaturze 25 ⁰C iloczyn rozpuszczalności wodorotlenku magnezu ma wartość 7,94∙10−12, a węglanu wapnia 3,31∙10–9.
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Oblicz rozpuszczalność wodorotlenku magnezu w temperaturze 25 ⁰C, w roztworze o wartości pH równej 12. Wynik podaj w μg/dm3 (mikrogramach na decymetr sześcienny roztworu), z dokładnością do dwóch cyfr znaczących. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określanie, czy strąci się osad substancji trudno rozpuszczalnej (iloczyn rozpuszczalności)
Iloczyn rozpuszczalności jest wielkością opisującą równowagę dynamiczną, jaka ustala się między osadem substancji trudno rozpuszczalnej, a jej nasyconym roztworem. W tabeli zebrano dane na temat wartości iloczynów rozpuszczalności trzech soli baru w temperaturze 25 ⁰C.
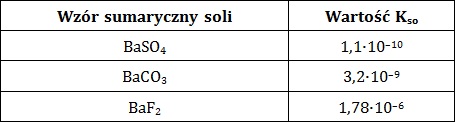
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Uzasadnij (wykonując stosowne obliczenia), czy strąci się osad węglanu baru, jeśli w temperaturze 25 ⁰C zmieszamy ze sobą 10 cm3 0,001-molowego roztworu chlorku baru z 15 cm3 0,002-molowego roztworu węglanu potasu? Rozwiązanie tego zadania dostępne jest nieodpłatnie pod poniższym linkiem: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie masy związku chemicznego, jaką można rozpuścić w roztworze zawierającym wspólny jon (iloczyn rozpuszczalności)
Iloczyn rozpuszczalności jest wielkością opisującą równowagę dynamiczną, jaka ustala się między osadem substancji trudno rozpuszczalnej, a jej nasyconym roztworem. W tabeli zebrano dane na temat wartości iloczynów rozpuszczalności trzech soli baru w temperaturze 25 ⁰C.

Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Oblicz masę fluorku baru, jaką można rozpuścić w 100 cm3 roztworu azotanu(V) baru o stężeniu równym 0,005 mol∙dm–3 w temperaturze 25 ⁰C. Wynik podaj w miligramach, z dokładnością do cyfry jedności. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie liczby jonów w nasyconym roztworze trudno rozpuszczalnego związku chemicznego (iloczyn rozpuszczalności)
Iloczyn rozpuszczalności jest wielkością opisującą równowagę dynamiczną, jaka ustala się między osadem substancji trudno rozpuszczalnej, a jej nasyconym roztworem. W tabeli zebrano dane na temat wartości iloczynów rozpuszczalności trzech soli baru w temperaturze 25 ⁰C.

Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Oblicz liczbę jonów pochodzących z dysocjacji siarczanu(VI) baru, jakie znajdują się w 500 cm3 nasyconego w temperaturze 25 ⁰C wodnego roztworu tej soli. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określanie objętości roztworu, jaką należy dodać do nasyconego roztworu zawierającego wspólny jon, aby doszło do zmniejszenia się rozpuszczalności (iloczyn rozpuszczalności)
W temperaturze 25 ⁰C iloczyn rozpuszczalności wodorotlenku magnezu ma wartość 7,94∙10−12, a węglanu wapnia 3,31∙10–9.
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Oblicz, jaką objętość 0,05-molowego roztworu wodorotlenku potasu należy dodać do 220 cm3 nasyconego w 25 ⁰C roztworu wodorotlenku magnezu, aby rozpuszczalność Mg(OH)2 zmalała 20-krotnie? Wynik podaj w centymetrach sześciennych, z dokładnością do cyfry jedności. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wybór poprawnych określeń dotyczących układu zawierającego trudno rozpuszczalny siarczan(VI) wapnia (iloczyn rozpuszczalności)
W temperaturze 25 ⁰C do zlewki zawierającej 250 cm3 wody destylowanej wprowadzono 30 g siarczanu(VI) wapnia, którego iloczyn rozpuszczalności (Kso) w opisanych warunkach ma wartość 3,16∙10–5. Zawartość naczynia zamieszano bagietką i odstawiono na kilka godzin utrzymując podaną wyżej temperaturę. W ten sposób uzyskano układ, którego schemat ilustruje rysunek poniżej. Literami A i B oznaczono pewne jego składniki.
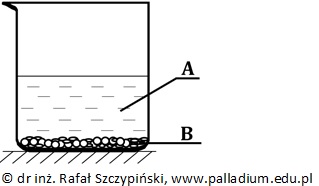
Zakładając, że ubytek wody powstały na skutek jej parowania został uzupełniony do ilości wyjściowej, podkreśl wyrażenia w nawiasach tak, by powstały zdania prawdziwe. W opisanym układzie klarowny roztwór znajdujący się nad osadem siarczanu(VI) wapnia jest roztworem (nienasyconym/nasyconym). Literą A oznaczono substancję (prostą/złożoną), która jest mieszaniną (jednorodną/niejednorodną), natomiast literą B substancję (prostą/złożoną), którą jest związek chemiczny tworzący kryształy (molekularne/jonowe). © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Opis obserwacji towarzyszących przeprowadzonemu doświadczeniu z udziałem wodnej zawiesiny siarczanu(VI) wapnia wraz z uzasadnieniem (iloczyn rozpuszczalności)
W temperaturze 25 ⁰C do zlewki zawierającej 250 cm3 wody destylowanej wprowadzono 30 g siarczanu(VI) wapnia, którego iloczyn rozpuszczalności (Kso) w opisanych warunkach ma wartość 3,16∙10–5. Zawartość naczynia zamieszano bagietką i odstawiono na kilka godzin utrzymując podaną wyżej temperaturę. W ten sposób uzyskano układ, którego schemat ilustruje rysunek poniżej. Literami A i B oznaczono pewne jego składniki.

Opisaną w informacji wprowadzającej zawartość zlewki przesączono. Do przesączu dodano pewną ilość wodnego roztworu chlorku wapnia i zaobserwowano objaw świadczący o przebiegu reakcji chemicznej. Napisz, co zaobserwowano w wyniku przeprowadzonego w temperaturze 25 ⁰C doświadczenia? Odpowiedź uzasadnij równaniem reakcji chemicznej, zapisanym w formie jonowej skróconej. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone

