Obliczanie rozpuszczalności glicyny na podstawie objętości rozpuszczalnika oraz masy nasyconego roztworu (rozpuszczalność substancji)
Do 0,4 dm3 wody destylowanej wprowadzono glicynę i w temperaturze 40 oC uzyskano 532,8 g nasyconego roztworu aminokwasu.
Oblicz rozpuszczalność glicyny w opisanych warunkach. Wynik podaj w g/100 g wody z dokładnością do trzech cyfr znaczących. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie stężenia procentowego nasyconego roztworu chlorku sodu o znanej rozpuszczalności (rozpuszczalność substancji)
Rozpuszczalność chlorku sodu w temperaturze 80 oC wynosi 38 g/100 g wody.
Oblicz stężenie procentowe nasyconego w tej temperaturze roztworu podanej soli. Wynik podaj z dokładnością do pierwszego miejsca po przecinku. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie rozpuszczalności azotanu(V) sodu na podstawie stężenia procentowego nasyconego roztworu (rozpuszczalność substancji)
W temperaturze 40 oC nasycony wodny roztwór azotanu(V) sodu ma stężenie 51%.
Oblicz rozpuszczalność (g/100 g wody) tej soli w podanych warunkach. Wynik podaj z dokładnością do trzech cyfr znaczących. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie jaki procent masy wyjściowego roztworu stanowi przesącz uzyskany w wyniku odparowania wody i wykrystalizowania bezwodnego chlorku potasu
W temperaturze 80 oC rozpuszczalność bezwodnego chlorku potasu wynosi 51,2 g/100 g wody. Z 300 g nasyconego w tej temperaturze roztworu odparowano 25 g wody, a powstały osad odsączono.
Oblicz, jaki procent masy wyjściowego roztworu stanowił przesącz, jeśli wiadomo, że wykrystalizowana sól nie była hydratem? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie objętości roztworu wodorotlenku niezbędnej do zobojętnienia nasyconego roztworu kwasu solnego
Rysunek poniżej ilustruje charakterystyki zmian rozpuszczalności chlorowodoru oraz azotanu(V) ołowiu(II) w 100 g wody, w zakresie temperatur 0 ⁰C ÷ 100 ⁰C, pod ciśnieniem 1013 hPa.
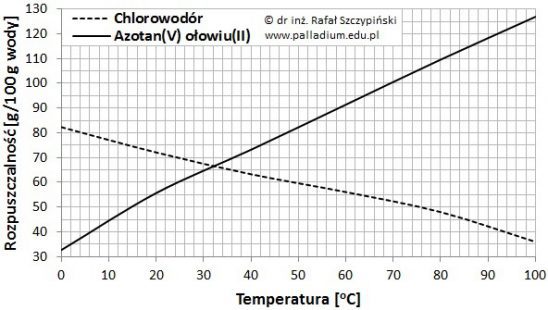
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Przygotowano nasycony w temperaturze 24 ⁰C roztwór kwasu solnego o masie 68 g.
Oblicz, jaką objętość 2,3-molowego roztworu wodorotlenku potasu należy użyć, w celu zobojętnienia podanego roztworu kwasu solnego? Wynik podaj w centymetrach sześciennych, stosując przybliżenie do pierwszego miejsca po przecinku. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie objętości wody, jaką należy wprowadzić do mieszaniny, w celu uzyskania roztworu nasyconego (rozpuszczalność substancji)
Rysunek poniżej ilustruje charakterystyki zmian rozpuszczalności chlorowodoru oraz azotanu(V) ołowiu(II) w 100 g wody, w zakresie temperatur 0 ⁰C ÷ 100 ⁰C, pod ciśnieniem 1013 hPa.

Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
W temperaturze równej 36 ⁰C przygotowano mieszaninę złożoną z 35 g azotanu(V) ołowiu(II) oraz 40 g wody destylowanej.
Oblicz, ile cm3 wody należałoby dodatkowo wprowadzić do tej mieszaniny, aby w podanej temperaturze uzyskać roztwór nasycony? Rozwiązanie tego zadania dostępne jest nieodpłatnie pod poniższym linkiem: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie dodatkowej ilości substancji, jaką należy rozpuścić, aby uzyskać roztwór nasycony (rozpuszczalność substancji)
Rysunek poniżej ilustruje charakterystyki zmian rozpuszczalności chlorowodoru oraz azotanu(V) ołowiu(II) w 100 g wody, w zakresie temperatur 0 ⁰C ÷ 100 ⁰C, pod ciśnieniem 1013 hPa.

Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
W temperaturze 25 ⁰C przygotowano 250 gramów 25-procentowego roztworu azotanu(V) ołowiu(II).
Oblicz, jaką masę soli należy wprowadzić do tego roztworu, aby po jej rozpuszczeniu, w temperaturze 25 ⁰C uzyskać roztwór nasycony? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie masy wykrystalizowanej soli w wyniku ochładzania roztworu (rozpuszczalność substancji)
Rysunek poniżej ilustruje charakterystyki zmian rozpuszczalności chlorowodoru oraz azotanu(V) ołowiu(II) w 100 g wody, w zakresie temperatur 0 ⁰C ÷ 100 ⁰C, pod ciśnieniem 1013 hPa.

Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
W temperaturze równej 42 ⁰C sporządzono 300 g nasyconego roztworu azotanu(V) ołowiu(II).
Oblicz, jaka masa soli wykrystalizuje po ochłodzeniu tego roztworu o 20 ⁰C? Określ, czy proces ten jest reakcją chemiczną, czy zjawiskiem fizycznym – uzasadnij swoją odpowiedź. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określanie o ile stopni Celsjusza należy podnieść temperaturę, aby uzyskać układ jednofazowy (rozpuszczalność substancji)
Rysunek poniżej ilustruje charakterystyki zmian rozpuszczalności chlorowodoru oraz azotanu(V) ołowiu(II) w 100 g wody, w zakresie temperatur 0 ⁰C ÷ 100 ⁰C, pod ciśnieniem 1013 hPa.

Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Do 100 g nasyconego w temperaturze 20 ⁰C roztworu Pb(NO3)2 dosypano 10 g czystej soli.
Oblicz, o ile stopni Celsjusza należy podnieść temperaturę, aby uzyskać układ jednofazowy? Wynik podaj z dokładnością do dwóch cyfr znaczących. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określanie rodzaju sporządzonego roztworu (rozpuszczalność substancji)
Rysunek poniżej ilustruje charakterystyki zmian rozpuszczalności chlorowodoru oraz azotanu(V) ołowiu(II) w 100 g wody, w zakresie temperatur 0 ⁰C ÷ 100 ⁰C, pod ciśnieniem 1013 hPa.

Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
W temperaturze 25 ⁰C przygotowano 80 g wodnego roztworu azotanu(V) ołowiu(II), przy czym w roztworze tym stosunek wagowy soli do rozpuszczalnika wynosił 1:2.
Określ, czy uzyskano roztwór nasycony, czy nienasycony? Odpowiedź uzasadnij obliczeniami. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wybór poprawnych określeń na podstawie wykresów rozpuszczalności (rozpuszczalność substancji)
Rysunek poniżej ilustruje charakterystyki zmian rozpuszczalności chlorowodoru oraz azotanu(V) ołowiu(II) w 100 g wody, w zakresie temperatur 0 ⁰C ÷ 100 ⁰C, pod ciśnieniem 1013 hPa.

Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Podkreśl wyrażenia w nawiasach tak, aby powstały zdania prawdziwe. Handlowo dostępny kwas solny jest wodnym roztworem (HBr/HCl/HI/HF) o stężeniu 38%. Jest to roztwór nasycony w temperaturze około (25/35/45/55) ⁰C. W identycznych warunkach temperaturowych, mieszanina złożona ze 100 g wody i 60 g rozpuszczonego w niej Pb(NO3)2 jest roztworem (nasyconym/nienasyconym), o stężeniu soli bliskim (38/44/52/60) %. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Uzyskiwanie roztworu nasyconego na drodze odparowania rozpuszczalnika (rozpuszczalność substancji)
W temperaturze 20 ⁰C rozpuszczalność siarczanu(VI) sodu wynosi 19,1 g/100 g wody. 100 ml roztworu kwasu siarkowego(VI) o stężeniu 30% i gęstości 1,22 g/cm3 poddano reakcji z taką ilością 10% roztworu wodorotlenku sodu, że nastąpiło całkowite zobojętnienie kwasu.
Oblicz, jaką ilość wody należy odparować z uzyskanego w wyniku zobojętnienia kwasu siarkowego(VI) roztworu, aby otrzymać nasycony w tej temperaturze roztwór soli? Wynik podaj z dokładnością do trzech cyfr znaczących. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie rozpuszczalności hydratu chlorku żelaza(II) na podstawie stężenia procentowego nasyconego roztworu (rozpuszczalność substancji)
Nasycony w temperaturze 20 oC wodny roztwór chlorku żelaza(II) ma stężenie równe 38,5%.
Oblicz (wyrażoną w g/100 g wody) rozpuszczalność hydratu o wzorze sumarycznym FeCl2∙4H2O użytego do sporządzenia opisanego nasyconego roztworu chlorku żelaza(II). Wynik podaj z dokładnością do całkowitej liczby gramów. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie rozpuszczalności siarczanu(VI) magnezu na podstawie rozpuszczalności jego hydratu (rozpuszczalność substancji)
W temperaturze 20 oC rozpuszczalność siarczanu(VI) magnezu-woda (1/7) ma wartość równą 105,5 g/100 g wody.
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Rozpuszczając w wodzie w danych warunkach określoną masę hydratu można uzyskać nasycony roztwór soli bezwodnej.
Oblicz rozpuszczalność bezwodnego siarczanu(VI) magnezu w temperaturze 20 oC. Wynik podaj w g/ 100 g wody, z dokładnością do trzech cyfr znaczących. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie stężenia procentowego nasyconego roztworu siarczanu(VI) magnezu na podstawie rozpuszczalności jego hydratu (rozpuszczalność substancji)
W temperaturze 20 oC rozpuszczalność siarczanu(VI) magnezu-woda (1/7) ma wartość równą 105,5 g/100 g wody.
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Rozpuszczając w wodzie w danych warunkach określoną masę hydratu można uzyskać nasycony roztwór soli bezwodnej.
Oblicz stężenie procentowe nasyconego w temperaturze 20 oC roztworu siarczanu(VI) magnezu. Wynik podaj z dokładnością do cyfry jedności. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone

