Wyznaczanie równania kinetycznego reakcji chemicznej na podstawie zmiany stężenia jednego substratu przy stałym stężeniu drugiego
Zbadano wpływ zmiany stężeń początkowych substratów A i B na szybkość pewnej reakcji chemicznej biegnącej według schematu:
3A(g) + 2B(g) → X(g)
Każde z doświadczeń przeprowadzono w temperaturze 400 K. Dane zebrano w tabeli.
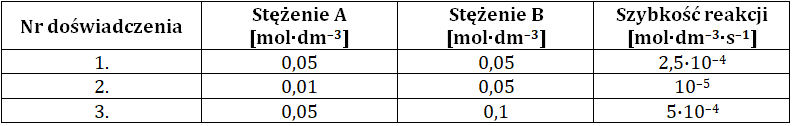
Uwzględniając wartość stałej szybkości opisanej reakcji chemicznej napisz jej równanie kinetyczne oraz określ całkowitą rzędowość. Równanie kinetyczne: …………………………………………..……… Rząd reakcji: …………………. Rozwiązanie tego zadania dostępne jest nieodpłatnie pod poniższym linkiem: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Ustalanie wzoru sumarycznego pochodnej kwasu karboksylowego na podstawie procentu wagowego węgla
Wiadomo, że w dwudodatnich jonach metalicznego pierwiastka Y elektrony opisane są czternastoma orbitalami, przy czym elektrony sparowane – trzynastoma orbitalami. Wodny roztwór pewnego związku chemicznego zawiera wyżej opisane jony pierwiastka Y oraz aniony reszty kwasowej nasyconego kwasu monokarboksylowego. W cząsteczkach tego kwasu atomy węgla stanowią 40% masy.
Wykonaj niezbędne obliczenia, a następnie ustal wzór sumaryczny oraz nazwę systematyczną związku chemicznego, o którego wodnym roztworze mowa. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Ustalanie wzorów grupowych cząsteczek dwóch izomerycznych kwasów karboksylowych
W cząsteczkach pewnych kwasów karboksylowych stosunek wagowy pierwiastków (C:H:O) wynosi 9:1:12, przy czym liczba atomów węgla równa jest liczbie atomów tlenu.
Narysuj wzory półstrukturalne cząsteczek opisanych związków chemicznych, wiedząc, że ich wzór rzeczywisty jest taki sam, jak wzór empiryczny, a atomy węgla połączone są wyłącznie wiązaniami typu sigma (σ). © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Rysowanie wzorów półstrukturalnych cząsteczek salicylamidu oraz paracetamolu
Paracetamol oraz salicylamid są amidami o działaniu leczniczym. Pierwszy z wymienionych związków chemicznych jest pochodną 4-hydroksyaniliny i kwasu octowego, drugi natomiast – kwasu salicylowego i amoniaku. Przeprowadzono doświadczenie z wykorzystaniem wodnych zawiesin paracetamolu i salicylamidu oraz sproszkowanego mocznika i węglanu potasu. Po dodaniu do każdej z probówek stechiometrycznej ilości kwasu siarkowego(VI), ich zawartość ogrzewano na łaźni wodnej.
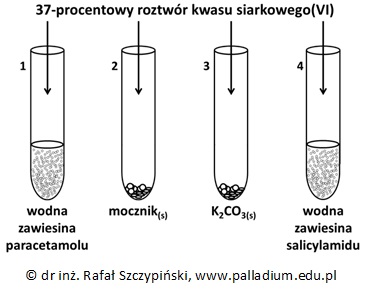
Narysuj półstrukturalne wzory cząsteczek paracetamolu oraz salicylamidu. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Opis obserwacji towarzyszących przeprowadzonemu doświadczeniu z udziałem amidów oraz soli
Paracetamol oraz salicylamid są amidami o działaniu leczniczym. Pierwszy z wymienionych związków chemicznych jest pochodną 4-hydroksyaniliny i kwasu octowego, drugi natomiast – kwasu salicylowego i amoniaku. Przeprowadzono doświadczenie z wykorzystaniem wodnych zawiesin paracetamolu i salicylamidu oraz sproszkowanego mocznika i węglanu potasu. Po dodaniu do każdej z probówek stechiometrycznej ilości kwasu siarkowego(VI), ich zawartość ogrzewano na łaźni wodnej.

Określ zmiany jakie zaobserwowano w każdej z probówek podczas prowadzenia opisanego doświadczenia. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zapis równań reakcji chemicznych na podstawie przeprowadzonego eksperymentu z udziałem mocznika i węglanu potasu
Paracetamol oraz salicylamid są amidami o działaniu leczniczym. Pierwszy z wymienionych związków chemicznych jest pochodną 4-hydroksyaniliny i kwasu octowego, drugi natomiast – kwasu salicylowego i amoniaku. Przeprowadzono doświadczenie z wykorzystaniem wodnych zawiesin paracetamolu i salicylamidu oraz sproszkowanego mocznika i węglanu potasu. Po dodaniu do każdej z probówek stechiometrycznej ilości kwasu siarkowego(VI), ich zawartość ogrzewano na łaźni wodnej.

Dla probówek o numerach 2 oraz 3 napisz równania przebiegających w nich reakcji chemicznych. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określanie odczynu roztworu uzyskanego w punkcie równoważnikowym miareczkowania roztworu jednokarboksylowego kwasu
W kolbie stożkowej zawierającej 100 cm3 wody destylowanej z dodatkiem kilku kropli fenoloftaleiny umieszczono 2,96 g próbki pewnego nasyconego alifatycznego kwasu jednokarboksylowego. Zawartość naczynia wymieszano i uzupełniono wodą destylowaną do objętości 150 cm3, a następnie zmiareczkowano wodnym roztworem wodorotlenku sodu o stężeniu 0,4 mol∙dm-3. Punkt równoważnikowy osiągnięto w momencie wykorzystania 100 cm3 roztworu wodorotlenku.
Określ, jaki odczyn miał uzyskany w punkcie równoważnikowym miareczkowania roztwór? Odpowiedź uzasadnij równaniem reakcji chemicznej zapisanym w formie jonowej skróconej. Skorzystaj ze wzoru ogólnego szeregu homologicznego kwasów, do którego należy związek chemiczny opisany w informacji wprowadzającej. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określanie wzoru sumarycznego kwasu jednokarboksylowego wykorzystując miareczkowanie
W kolbie stożkowej zawierającej 100 cm3 wody destylowanej z dodatkiem kilku kropli fenoloftaleiny umieszczono 2,96 g próbki pewnego nasyconego alifatycznego kwasu jednokarboksylowego. Zawartość naczynia wymieszano i uzupełniono wodą destylowaną do objętości 150 cm3, a następnie zmiareczkowano wodnym roztworem wodorotlenku sodu o stężeniu 0,4 mol∙dm-3. Punkt równoważnikowy osiągnięto w momencie wykorzystania 100 cm3 roztworu wodorotlenku.
Wykonaj niezbędne obliczenia i ustal wzór sumaryczny kwasu, którego wodny roztwór poddano miareczkowaniu. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Opis obserwacji towarzyszących przeprowadzonemu doświadczeniu z udziałem acetonu, etanalu i kwasu octowego
W trzech probówkach strącono wodorotlenek miedzi(II), a następnie w każdej z nich, w sposób losowy umieszczono wodne roztwory acetonu, etanalu oraz kwasu octowego. Każdym z naczyń energicznie wstrząśnięto i ogrzewano na łaźni wodnej o temperaturze około 90 ⁰C. Tylko w drugiej probówce zaobserwowano zmiany przed rozpoczęciem ogrzewania. W pierwszym i trzecim naczyniu po zakończeniu doświadczenia odnotowano zmianę barwy znajdującego się w nich osadu – odpowiednio na kolor czarny oraz ceglasty.
Określ, co zaobserwowano w drugiej probówce przed rozpoczęciem ogrzewania jej zawartości? Odpowiedź uzasadnij równaniem reakcji chemicznej, której przebiegowi towarzyszyły takie, a nie inne podane przez Ciebie obserwacje. Rozwiązanie tego zadania dostępne jest nieodpłatnie pod poniższym linkiem: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zapis równania reakcji chemicznej na podstawie przeprowadzonego eksperymentu z utworzeniem czarnej substancji
W trzech probówkach strącono wodorotlenek miedzi(II), a następnie w każdej z nich, w sposób losowy umieszczono wodne roztwory acetonu, etanalu oraz kwasu octowego. Każdym z naczyń energicznie wstrząśnięto i ogrzewano na łaźni wodnej o temperaturze około 90 ⁰C. Tylko w drugiej probówce zaobserwowano zmiany przed rozpoczęciem ogrzewania. W pierwszym i trzecim naczyniu po zakończeniu doświadczenia odnotowano zmianę barwy znajdującego się w nich osadu – odpowiednio na kolor czarny oraz ceglasty.
Napisz równanie reakcji chemicznej, jaka doprowadziła do powstania czarnej substancji i podaj wzór sumaryczny związku chemicznego wchodzącego w skład ceglastego osadu. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Bilansowanie równania reakcji kwasu szczawiowego z zakwaszonym roztworem manganianu(VII) potasu
Plamy pozostałe po manganianie(VII) potasu można wywabić roztworem kwasu szczawiowego z dodatkiem rozcieńczonego kwasu siarkowego(VI).
Napisz w formie jonowej skróconej równanie przebiegającej reakcji chemicznej, jaka prowadzi do usunięcia plam. Współczynniki uzgodnij metodą bilansu jonowo-elektronowego. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określanie wzorów półstrukturalnych izomerów geometrycznych kwasu karboksylowego (izomeria geometryczna)
W celu całkowitego przereagowania 1 g pewnego jednonienasyconego, monokarboksylowego kwasu alifatycznego zużyto 4 g 10% roztworu wodorotlenku sodu.
Podaj nazwę systematyczną tego kwasu oraz wzory półstrukturalne jego izomerów geometrycznych, jeśli wiadomo, że wszystkie atomy węgla w cząsteczkach tego związku chemicznego leżą na tej samej płaszczyźnie. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone

