Uzasadnienie poprawności narysowanej struktury cząsteczki na podstawie teorii VSEPR. Zadanie 6.2. Informator CKE chemia 2023 rozszerzony (1 punkt)
Atom siarki tworzy z atomami fluoru m.in. cząsteczki o wzorze SF2 i SF6. Poniżej zamieszczono model ilustrujący kształt cząsteczki SF6.
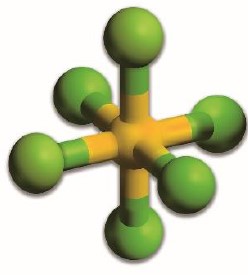
Wykaż na podstawie teorii VSEPR (odpychanie par elektronowych powłoki walencyjnej), że przedstawiony model jest poprawną ilustracją kształtu cząsteczki SF6.
Wybór właściwego procesu z uzasadnieniem na podstawie danych pomiarowych. Zadanie 7. Informator CKE chemia 2023 rozszerzony (2 punkty)
Zbadano wpływ zmian temperatury (doświadczenie I) i zmian ciśnienia (doświadczenie II) w układzie na wydajność otrzymywania produktu X w reakcji opisanej schematem:
a A (g) + b B (g) ⇄ x X (g)
Wyniki pomiarów zamieszczono w poniższych tabelach. Zawartość produktu X w mieszaninie równowagowej wyrażono w procentach objętościowych.
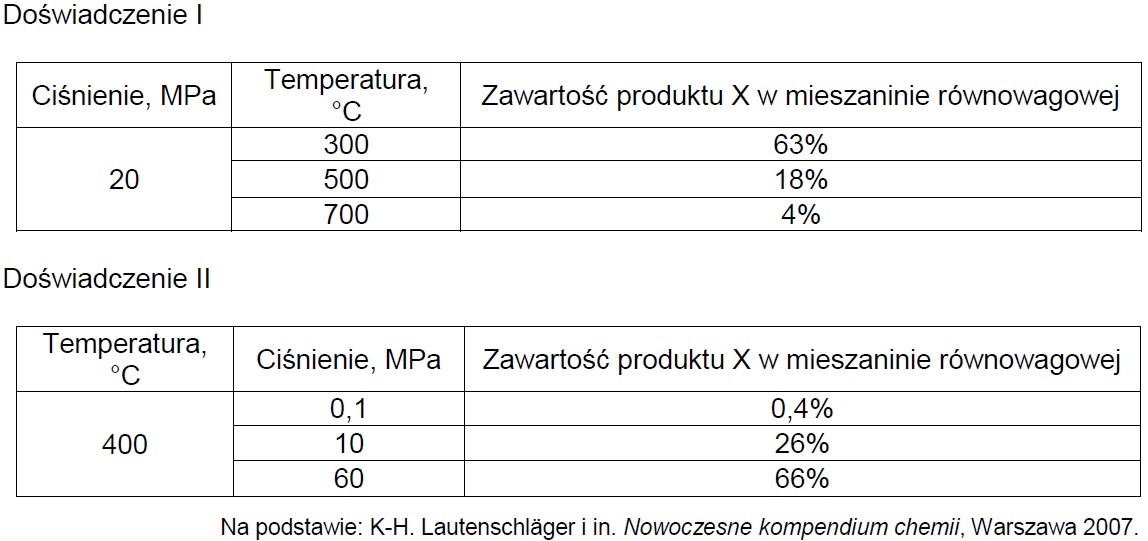
Na podstawie przedstawionych wyników pomiarów wybierz spośród wymienionych poniżej proces, który zachodził w badanym układzie. Napisz numer wybranego procesu. Odpowiedź uzasadnij. Numer procesu: Uzasadnienie:
Wybór poprawnych określeń dotyczących doświadczenia ze zmianą objętości układu. Zadanie 8. Informator CKE chemia 2023 rozszerzony (1 punkt)
Przeprowadzono doświadczenie, którego celem była obserwacja zmian energii wewnętrznej badanego układu w wyniku przemiany chemicznej. W procesie przeprowadzonym w warunkach izotermiczno-izobarycznych wprowadzono do cylindra gazowy tlen oraz sproszkowane żelazo i zamknięto ten cylinder ruchomym tłokiem. Schemat doświadczenia przedstawiono na poniższym rysunku.
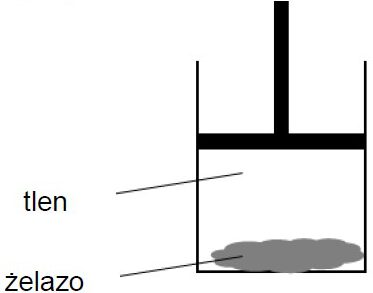
W warunkach doświadczenia reakcja zachodziła z niewielką szybkością. Ścianki cylindra umożliwiały wymianę ciepła z otoczeniem.
Uzupełnij poniższe zdania. Wybierz i zaznacz jedną odpowiedź spośród podanych w każdym nawiasie. W wyniku przebiegu opisanego procesu tlen się zużywa, a tłok przesuwa się (w dół / w górę), wykonując pracę nad układem. Przemianie żelaza w tlenek żelaza(III) towarzyszyło odprowadzenie ciepła do otoczenia, co oznacza, że ta reakcja jest procesem (endoenergetycznym / egzoenergetycznym).
Obliczanie ilości energii jaką należy dostarczyć w celu przeprowadzenia reakcji rozkładu. Zadanie 9. Informator CKE chemia 2023 rozszerzony (2 punkty)
Reakcja rozkładu azotanu(V) ołowiu(II) jest procesem endoenergetycznym i przebiega zgodnie z równaniem:
2Pb(NO3)2 → 2PbO + 4NO2↑ + O2↑
Wartości standardowych entalpii tworzenia związków biorących udział w opisanej reakcji podano w poniższej tabeli.

Oblicz, ile energii na sposób ciepła należy dostarczyć, aby całkowicie rozłożyć 3,31 g Pb(NO3)2.
Wybór właściwego wykresu ilustrującego zmiany stężenia reagenta. Zadanie 10. Informator CKE chemia 2023 rozszerzony (1 punkt)
Do reaktora o stałej pojemności, z którego usunięto powietrze, wprowadzono próbkę gazowego związku A i zainicjowano reakcję. W zamkniętym reaktorze ustaliła się równowaga opisana równaniem:
A (g) ⇄ 2B (g)
Mierzono stężenie związku A w czasie trwania reakcji. Tę zależność przedstawiono na poniższym wykresie:
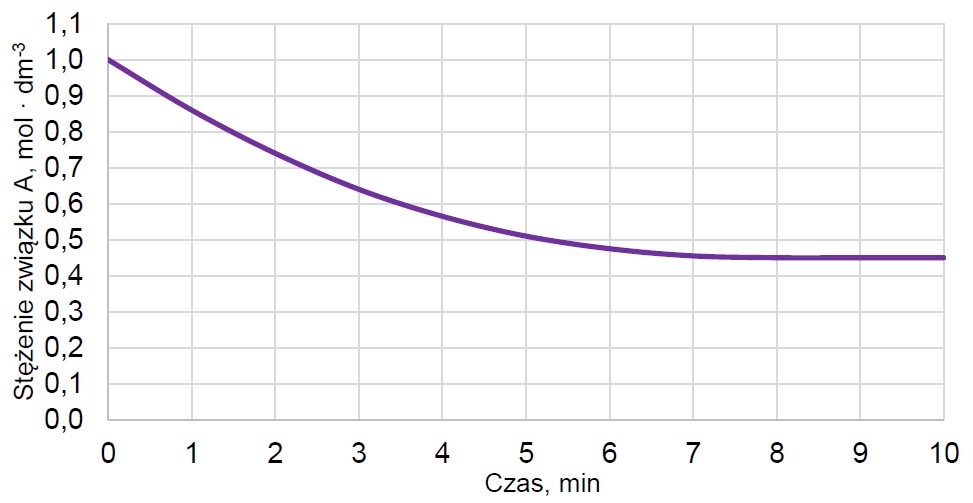
Z poniższych wykresów wybierz ten, który jest ilustracją zależność stężenia związku B od czasu trwania reakcji. Zaznacz wykres A, B, C albo D i uzasadnij swój wybór. Uzasadnienie: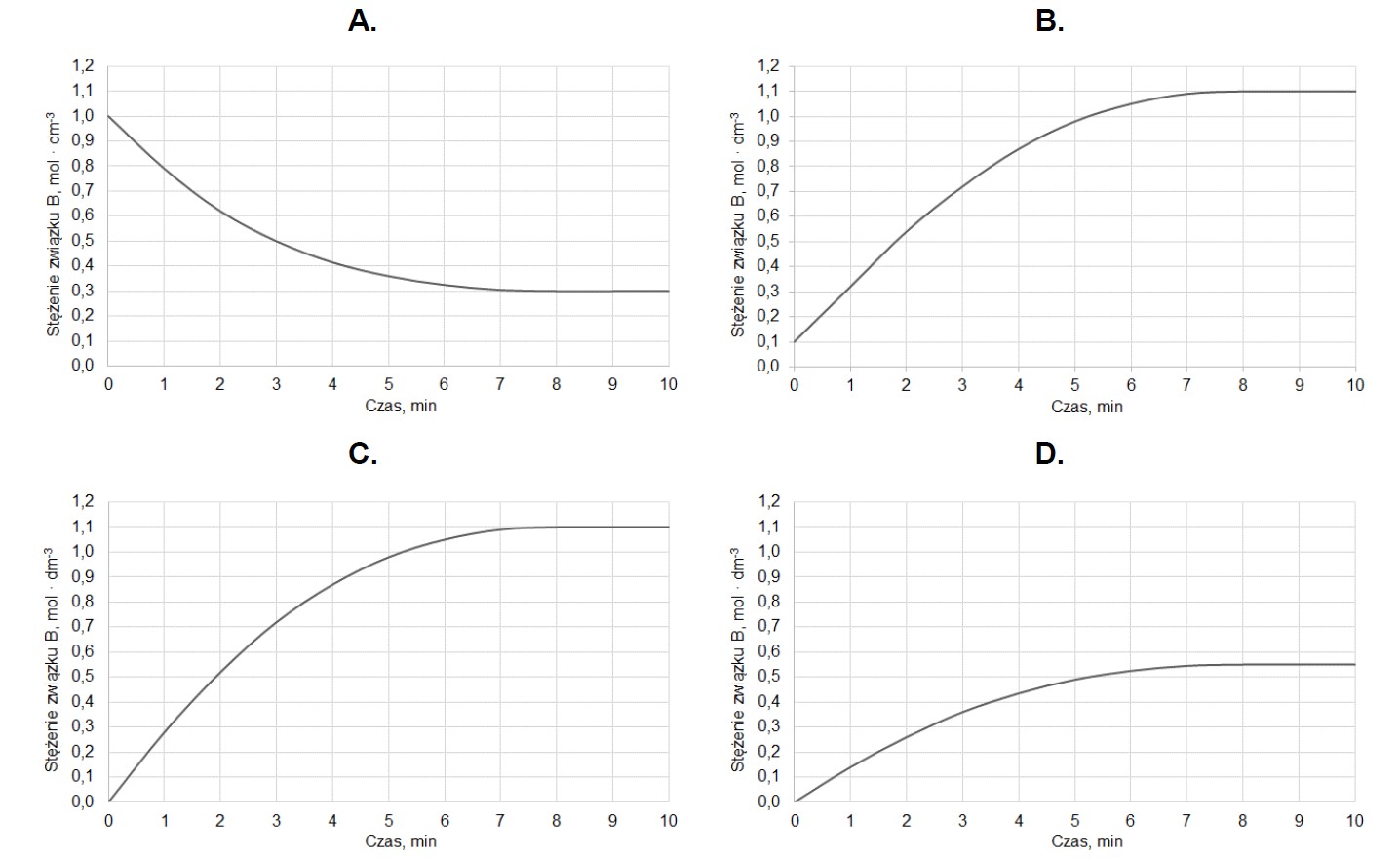
Obliczanie wartości stężeniowej stałej równowagi. Zadanie 11. Informator CKE chemia 2023 rozszerzony (2 punkty)
Skład mieszaniny można wyrazić za pomocą ułamków molowych. Ułamek molowy składnika A, 𝑥n(A), to iloraz liczby moli tego składnika, 𝑛A, i sumy liczb moli wszystkich składników mieszaniny. Np. dla mieszaniny trójskładnikowej A, B, C:
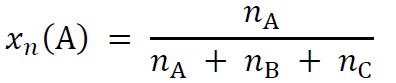
W pewnych warunkach ciśnienia i temperatury sporządzono mieszaninę dwóch gazowych substancji: wodoru i jodu, w zamkniętym reaktorze o objętości V = 20,0 dm3.
Po zainicjowaniu procesu opisanego równaniem:
![]()
uzyskano w stanie równowagi mieszaninę o składzie: 𝑚(I2) = 381 g, 𝑛(HI) = 1,50 mol oraz pewną ilość wodoru. Sumaryczna liczba moli wszystkich składników uzyskanej mieszaniny równowagowej wynosiła 6,00 moli.
Oblicz wartość stężeniowej stałej równowagi reakcji syntezy jodowodoru w warunkach temperatury i ciśnienia, w których wykonano pomiar, oraz oblicz skład początkowej mieszaniny substratów reakcji w ułamkach molowych.
Rysowanie wykresu ilustrującego zmiany stężeń reagentów w czasie trwania reakcji. Zadanie 12. Informator CKE chemia 2023 rozszerzony (1 punkt)
Skład mieszaniny można wyrazić za pomocą ułamków molowych. Ułamek molowy składnika A, 𝑥n(A), to iloraz liczby moli tego składnika, 𝑛A, i sumy liczb moli wszystkich składników mieszaniny. Np. dla mieszaniny trójskładnikowej A, B, C:
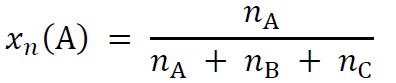
W pewnych warunkach ciśnienia i temperatury sporządzono mieszaninę dwóch gazowych substancji: wodoru i jodu, w zamkniętym reaktorze o objętości V = 20,0 dm3.
Po zainicjowaniu procesu opisanego równaniem:
![]()
uzyskano w stanie równowagi mieszaninę o składzie: 𝑚(I2) = 381 g, 𝑛(HI) = 1,50 mol oraz pewną ilość wodoru. Sumaryczna liczba moli wszystkich składników uzyskanej mieszaniny równowagowej wynosiła 6,00 moli.
Narysuj wykres przedstawiający zmiany liczby moli wszystkich reagentów w czasie trwania reakcji: od momentu rozpoczęcia eksperymentu – P, przez moment, w którym układ osiągnął stan równowagi – R, do momentu zakończenia eksperymentu – Z. W tym celu narysuj trzy krzywe obrazujące zmiany liczb moli reagentów i wprowadź oznaczenia tych krzywych: n(H2), n(I2) oraz n(HI).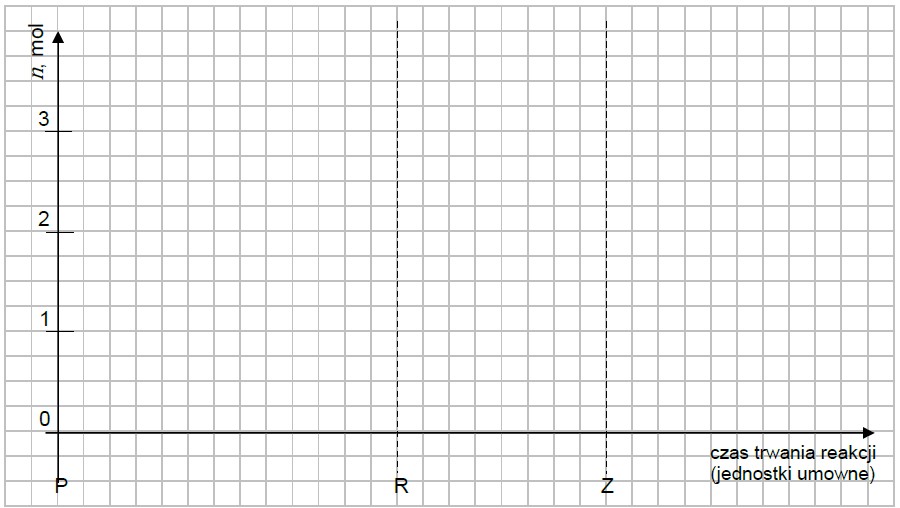
Termograwimetryczne ustalanie przebiegu procesu rozkładu hydratu węglanu kobaltu(II). Zadanie 14. Informator CKE chemia 2023 rozszerzony (3 punkty)
Termograwimetria to technika badania związków chemicznych pozwalająca m.in. na rejestrację zmian masy próbki w trakcie jej rozkładu termicznego. Wynikiem takiego badania jest krzywa zwana termogramem, ilustrująca zmianę masy próbki w funkcji wzrastającej ze stałą szybkością temperatury.
Próbkę zawierającą 3∙10–4 mola uwodnionego węglanu kobaltu(II), CoCO3∙xH2O, ogrzewano w atmosferze argonu. Rejestrowano zmiany masy próbki wraz z rosnącą temperaturą w przedziale od 0 °C do 550 °C. Badanie prowadzono do chwili, w której masa próbki nie ulegała już dalszym zmianom. Stwierdzono, że rozkład termiczny zachodzi w dwóch etapach. Analiza gazowych produktów rozkładu powstających w trakcie eksperymentu w obu etapach wykazała, że w każdym z nich wydziela się tylko jeden rodzaj gazu, w każdym z etapów – inny. Uzyskany termogram przedstawiono na schemacie.
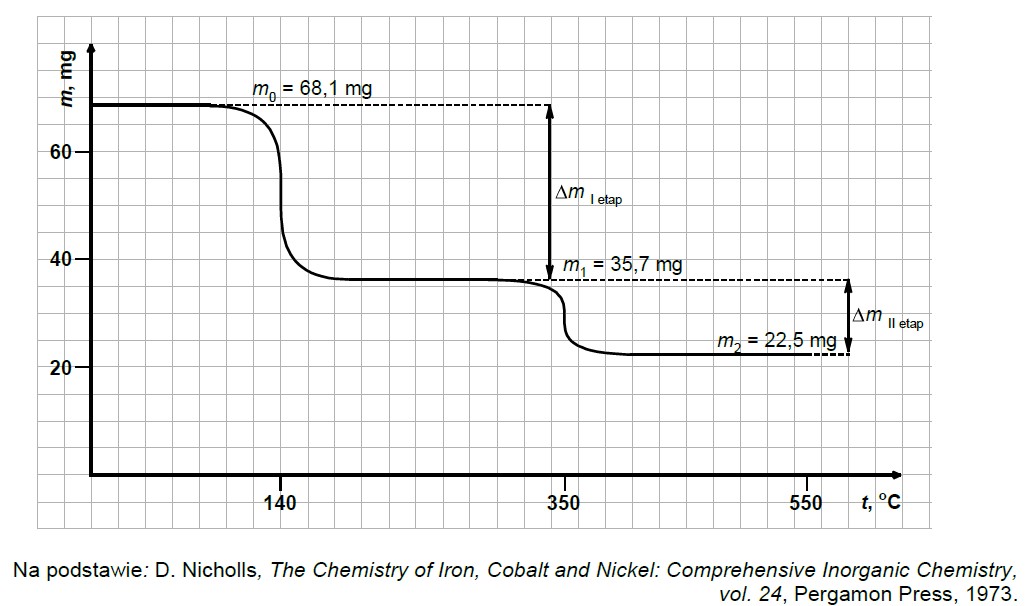
Na podstawie obliczeń ustal przebieg rozkładu hydratu węglanu kobaltu(II) – napisz równania reakcji przebiegających w I i II etapie rozkładu. Równanie reakcji rozkładu w I etapie: Równanie reakcji rozkładu w II etapie:
Wybór poprawnych odczynników do przeprowadzenia doświadczenia. Zadanie 15.1. Informator CKE chemia 2023 rozszerzony (1 punkt)
Przeprowadzono doświadczenie, w którym na podstawie zachodzącej reakcji chemicznej można stwierdzić, że wolny chlor jest silniejszym utleniaczem niż wolny brom.
Uzupełnij schemat przeprowadzonego doświadczenia – zaznacz po jednym wzorze odczynnika w zestawach I i II.
Wskazanie właściwej fotografii ilustrującej mieszaninę poreakcyjną. Zadanie 15.2. Informator CKE chemia 2023 rozszerzony (1 punkt)
Przeprowadzono doświadczenie, w którym na podstawie zachodzącej reakcji chemicznej można stwierdzić, że wolny chlor jest silniejszym utleniaczem niż wolny brom.

Do probówki zawierającej kilka cm3 bezbarwnego rozpuszczalnika CCl4 wlano podobną objętość odczynnika, który został wybrany z zestawu I, a następnie zawartość probówki energicznie wstrząsano. Zaobserwowano rozdzielenie się cieczy na dwie warstwy (etap 1.). Następnie do probówki dodano odczynnik wybrany z zestawu II, ponownie wstrząsano zawartość probówki i zaobserwowano rozdzielenie się cieczy na dwie warstwy (etap 2.).
Zaznacz numer zdjęcia, na którym zilustrowany jest wynik po etapie 1., oraz numer zdjęcia przedstawiającego wynik po etapie 2. doświadczenia.
Zapis równania reakcji chemicznej przebiegającej podczas doświadczenia. Zadanie 15.3. Informator CKE chemia 2023 rozszerzony (1 punkt)
Przeprowadzono doświadczenie, w którym na podstawie zachodzącej reakcji chemicznej można stwierdzić, że wolny chlor jest silniejszym utleniaczem niż wolny brom.

Napisz w formie jonowej skróconej równanie reakcji zachodzącej podczas przeprowadzonego doświadczenia.
Obliczanie masy jodu znajdującego się w 100 g wody jodowej. Zadanie 16. Informator CKE chemia 2023 rozszerzony (2 punkty)
Jod bardzo słabo rozpuszcza się w wodzie i jego nasycony roztwór, nazywany wodą jodową, w temperaturze 25 oC ma stężenie ok. 1,3·10–3 mol·dm–3. Dużo lepiej jod rozpuszcza się (roztwarza) w roztworze zawierającym jony jodkowe, gdyż przebiega tam reakcja opisana równaniem:
I2 + I– ⇄ I3–
Stężeniowa stała tej równowagi w temperaturze 25 oC jest równa 700.
W niektórych schorzeniach tarczycy stosuje się tzw. płyn Lugola, który można przyrządzić, jeśli wymiesza się 1 g jodu i 2 g jodku potasu z 97 g wody.
Oblicz masę jodu rozpuszczonego w 100 g nasyconego wodnego roztworu w temperaturze 25 oC. Oblicz, ile razy masa jodu, który rozpuszczono, aby przygotować 100 g płynu Lugola, jest większa niż masa jodu w 100 g wody jodowej. Przyjmij, że gęstość wody jodowej jest równa 1,0 g·cm–3.
Obliczanie stężenia równowagowego jonów jodkowych w płynie Lugola. Zadanie 17. Informator CKE chemia 2023 rozszerzony (2 punkty)
Jod bardzo słabo rozpuszcza się w wodzie i jego nasycony roztwór, nazywany wodą jodową, w temperaturze 25 oC ma stężenie ok. 1,3·10–3 mol·dm–3. Dużo lepiej jod rozpuszcza się (roztwarza) w roztworze zawierającym jony jodkowe, gdyż przebiega tam reakcja opisana równaniem:
I2 + I– ⇄ I3–
Stężeniowa stała tej równowagi w temperaturze 25 oC jest równa 700.
W niektórych schorzeniach tarczycy stosuje się tzw. płyn Lugola, który można przyrządzić, jeśli wymiesza się 1 g jodu i 2 g jodku potasu z 97 g wody.
Oblicz równowagowe stężenie jonów jodkowych (I–) w płynie Lugola w temperaturze 25 oC. Przyjmij, że gęstość tego roztworu w temperaturze pokojowej jest równa 1,05 g·cm–3.
Rysowanie wzoru elektronowego jonu trijodkowego. Zadanie 18. Informator CKE chemia 2023 rozszerzony (1 punkt)
Jod bardzo słabo rozpuszcza się w wodzie i jego nasycony roztwór, nazywany wodą jodową, w temperaturze 25 oC ma stężenie ok. 1,3·10–3 mol·dm–3. Dużo lepiej jod rozpuszcza się (roztwarza) w roztworze zawierającym jony jodkowe, gdyż przebiega tam reakcja opisana równaniem:
I2 + I– ⇄ I3–
Stężeniowa stała tej równowagi w temperaturze 25 oC jest równa 700.
W niektórych schorzeniach tarczycy stosuje się tzw. płyn Lugola, który można przyrządzić, jeśli wymiesza się 1 g jodu i 2 g jodku potasu z 97 g wody.
Jon trijodkowy I3– ma budowę liniową.
Narysuj wzór elektronowy jonu trijodkowego. Zaznacz kreskami wszystkie wspólne i wolne pary elektronowe atomów.

