Ocena jak rozcieńczenie wodą wpłynie na pH buforu amonowego. Zadanie 20. Arkusz CKE chemia maj 2012 rozszerzony (1 punkt)
Bufory pH to roztwory zawierające sprzężoną parę kwas–zasada Brønsteda w podobnych stężeniach. Roztwory te mają zdolność do utrzymywania stałej wartości pH po dodaniu do nich niewielkich ilości mocnych kwasów lub zasad. Działanie buforu pH polega na tym, że po dodaniu mocnego kwasu zasada Brønsteda reaguje z jonami H3O+, a po dodaniu mocnej zasady kwas Brønsteda reaguje z jonami OH–. Przykładem roztworu buforowego jest bufor amonowy, który otrzymuje się przez rozpuszczenie w wodzie amoniaku NH3 i chlorku amonu NH4Cl. Sprzężoną parę kwas–zasada stanowią obecne w nim kationy amonowe i cząsteczki amoniaku.
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, t. 1, Warszawa 2005
O pH roztworu buforowego decyduje rodzaj zawartej w nim sprzężonej pary kwas–zasada oraz stosunek stężenia kwasu i sprzężonej z nim zasady.
Oceń, jak wpłynie na pH buforu amonowego rozcieńczenie go wodą destylowaną. Uzupełnij poniższe zdanie, wpisując określenie wzrośnie, zmaleje lub nie zmieni się. Po rozcieńczeniu buforu amonowego jego pH:
Zapis równań reakcji chemicznych z udziałem związków chromu. Zadanie 21a. Arkusz CKE chemia maj 2012 rozszerzony (2 punkty)
Do wodnego roztworu chromianu(VI) potasu dodano kilka kropli rozcieńczonego kwasu siarkowego(VI) i stwierdzono, że roztwór zmienił barwę z żółtej na pomarańczową. Świadczyło to o powstaniu anionów dichromianowych(VI) (reakcja I). Następnie do otrzymanego roztworu wprowadzono kilka kropli roztworu wodorotlenku potasu i roztwór z powrotem stał się żółty (reakcja II).
Napisz w formie jonowej skróconej równania reakcji I i II. I: II:
Wybór właściwych zdań dotyczących reakcji związków chromu. Zadanie 21b. Arkusz CKE chemia maj 2012 rozszerzony (1 punkt)
Do wodnego roztworu chromianu(VI) potasu dodano kilka kropli rozcieńczonego kwasu siarkowego(VI) i stwierdzono, że roztwór zmienił barwę z żółtej na pomarańczową. Świadczyło to o powstaniu anionów dichromianowych(VI) (reakcja I). Następnie do otrzymanego roztworu wprowadzono kilka kropli roztworu wodorotlenku potasu i roztwór z powrotem stał się żółty (reakcja II).
Spośród poniższych zdań wybierz wszystkie, które są wnioskami wynikającymi z opisanego doświadczenia. I Chromiany(VI) są silnymi utleniaczami, a ich właściwości utleniające zależą od pH środowiska reakcji. II Przemiana anionów chromianowych(VI) w aniony dichromianowe(VI) jest reakcją odwracalną. III W środowisku zasadowym trwałe są aniony chromianowe(VI), a w środowisku kwasowym – aniony dichromianowe(VI). IV W środowisku zasadowym trwałe są aniony dichromianowe(VI), a w środowisku kwasowym – aniony chromianowe(VI). Numery wybranych zdań:
Wskazanie kolejności pierwiastków chemicznych wydzielanych na katodzie. Zadanie 22a. Arkusz CKE chemia maj 2012 rozszerzony (1 punkt)
W 1 dm3 wody rozpuszczono azotan(V) srebra(I) AgNO3, azotan(V) miedzi(II) Cu(NO3)2 oraz azotan(V) sodu NaNO3, otrzymując roztwór o jednakowych stężeniach molowych kationów. Przez otrzymany roztwór przepuszczono ładunek elektryczny w warunkach umożliwiających wydzielenie na katodzie kolejno trzech pierwiastków.
Uzupełnij poniższą tabelę, wpisując nazwy lub symbole pierwiastków w kolejności ich wydzielania na katodzie.
Wskazanie pierwiastka wydzielonego na anodzie oraz zapis równania reakcji elektrodowej. Zadanie 22b. Arkusz CKE chemia maj 2012 rozszerzony (1 punkt)
W 1 dm3 wody rozpuszczono azotan(V) srebra(I) AgNO3, azotan(V) miedzi(II) Cu(NO3)2 oraz azotan(V) sodu NaNO3, otrzymując roztwór o jednakowych stężeniach molowych kationów. Przez otrzymany roztwór przepuszczono ładunek elektryczny w warunkach umożliwiających wydzielenie na katodzie kolejno trzech pierwiastków.
Wiedząc, że w doświadczeniu użyto elektrod grafitowych, określ, jaki pierwiastek wydzielił się na anodzie. Odpowiedź uzasadnij, pisząc równanie reakcji anodowej. Nazwa lub symbol pierwiastka: Równanie reakcji:
Uzupełnienie schematu ogniwa oraz zapis obserwowanych zmian podczas jego pracy. Zadanie 23ab. Arkusz CKE chemia maj 2012 rozszerzony (2 punkty)
Zaprojektuj ogniwo galwaniczne, w którym półogniwo Ni│Ni2+ będzie pełnić funkcję anody.
a) Uzupełnij poniższy schemat, wpisując symbole lub wzory odczynników wybranych spośród następujących: Ni Ni(NO3)2 (aq) Pb Pb(NO3)2 (aq) Zn Zn(NO3)2 (aq) b) Opisz zmiany, jakie będzie można zaobserwować w półogniwach podczas pracy ogniwa. Anoda: Katoda: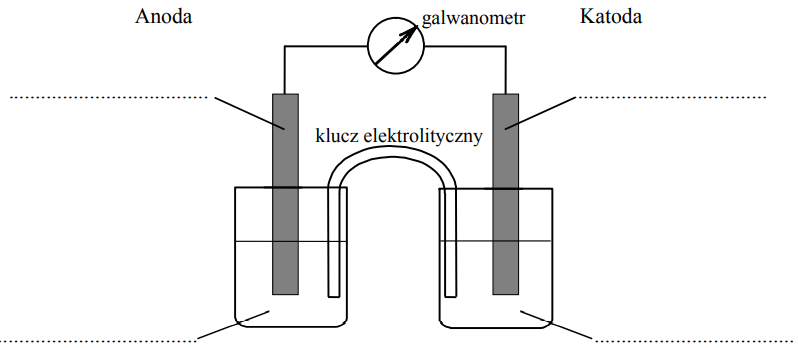
Wskazanie stopni utlenienia atomów węgla oraz liczby elektronów wymienianych podczas reakcji redoks. Zadanie 24. Arkusz CKE chemia maj 2012 rozszerzony (2 punkty)
W reakcji z wodnym roztworem manganianu(VII) potasu eten utlenia się do etano-1,2-diolu (glikolu etylenowego).
Wyznacz stopnie utlenienia atomów węgla w cząsteczce etenu i cząsteczce etano-1,2-diolu oraz określ liczbę moli elektronów oddawanych przez 1 mol etenu w opisanej reakcji. Stopnie utlenienia atomów węgla w cząsteczce etenu: Stopnie utlenienia atomów węgla w cząsteczce etano-1,2-diolu: Liczba moli elektronów:
Wybór poprawnych określeń dotyczących reakcji chlorowania etanu oraz benzenu. Zadanie 25. Arkusz CKE chemia maj 2012 rozszerzony (2 punkty)
Na przykładzie reakcji chloru z etanem i chloru z benzenem porównaj mechanizm reakcji substytucji, którym ulegają węglowodory nasycone i aromatyczne.
Uzupełnij poniższe zdania, wybierając nazwy spośród podanych w nawiasach (wybrane nazwy podkreśl). 1. Etan ulega reakcji substytucji ( elektrofilowej / nukleofilowej / wolnorodnikowej ). Drobiny, które reagują bezpośrednio z cząsteczkami etanu, to (atomy chloru Cl· / cząsteczki chloru Cl2 / aniony chlorkowe Cl–). Są one (rodnikami / elektrofilami / nukleofilami), które powstają z cząsteczek chloru pod wpływem (światła / FeCl3 jako katalizatora / rozpuszczalnika). 2. Benzen ulega reakcji substytucji (elektrofilowej / nukleofilowej / wolnorodnikowej). Drobiny, które reagują bezpośrednio z cząsteczkami benzenu, są (rodnikami / elektrofilami / nukleofilami ). Powstają one z cząsteczek chloru pod wpływem (światła / FeCl3 jako katalizatora / rozpuszczalnika).
Zapis równań reakcji chemicznych prowadzących do utworzenia odczynnika Tollensa. Zadanie 26a. Arkusz CKE chemia maj 2012 rozszerzony (1 punkt)
Odczynnik Tollensa, potocznie nazywany amoniakalnym roztworem tlenku srebra, otrzymuje się przez dodanie wody amoniakalnej do wodnego roztworu AgNO3. Potoczna nazwa odczynnika nie jest poprawna, ponieważ jon O2– nie występuje w roztworach wodnych. Początkowo wytrąca się czarnobrunatny osad tlenku srebra(I). W miarę dodawania kolejnych porcji wody amoniakalnej osad ten ulega roztworzeniu, ponieważ jony srebra(I) tworzą z cząsteczkami amoniaku jony kompleksowe o wzorze [Ag(NH3)2]+ . W wyniku tej reakcji powstaje bezbarwny roztwór, który jest odczynnikiem Tollensa.
Uzupełnij poniższe zapisy, tak aby otrzymać równania (w formie jonowej) opisanych reakcji. Wpisz wzory produktów oraz brakujące współczynniki stechiometryczne.
Określenie odczynu roztworu odczynnika Tollensa. Zadanie 26b. Arkusz CKE chemia maj 2012 rozszerzony (1 punkt)
Odczynnik Tollensa, potocznie nazywany amoniakalnym roztworem tlenku srebra, otrzymuje się przez dodanie wody amoniakalnej do wodnego roztworu AgNO3. Potoczna nazwa odczynnika nie jest poprawna, ponieważ jon O2– nie występuje w roztworach wodnych. Początkowo wytrąca się czarnobrunatny osad tlenku srebra(I). W miarę dodawania kolejnych porcji wody amoniakalnej osad ten ulega roztworzeniu, ponieważ jony srebra(I) tworzą z cząsteczkami amoniaku jony kompleksowe o wzorze [Ag(NH3)2]+ . W wyniku tej reakcji powstaje bezbarwny roztwór, który jest odczynnikiem Tollensa.
Określ odczyn roztworu będącego odczynnikiem Tollensa.
Ocena, czy wykorzystując próbę Tollensa możliwe jest odróżnienie glukozy od fruktozy. Zadanie 27. Arkusz CKE chemia maj 2012 rozszerzony (1 punkt)
W roztworze o odczynie zasadowym ketony, których cząsteczki zawierają grupę hydroksylową –OH przy atomie węgla połączonym z atomem węgla grupy karbonylowej (α-hydroksyketony), ulegają izomeryzacji. Przemianę tę ilustruje poniższy schemat.
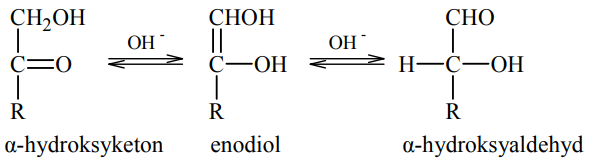
Oceń, czy za pomocą próby Tollensa można odróżnić glukozę od fruktozy. Odpowiedź uzasadnij.
Wskazanie cukrów dających pozytywny wynik próby Tollensa. Zadanie 28. Arkusz CKE chemia maj 2012 rozszerzony (1 punkt)
Poniżej przedstawiono wzory (w projekcji Hawortha) ilustrujące budowę wybranych mono i disacharydów.
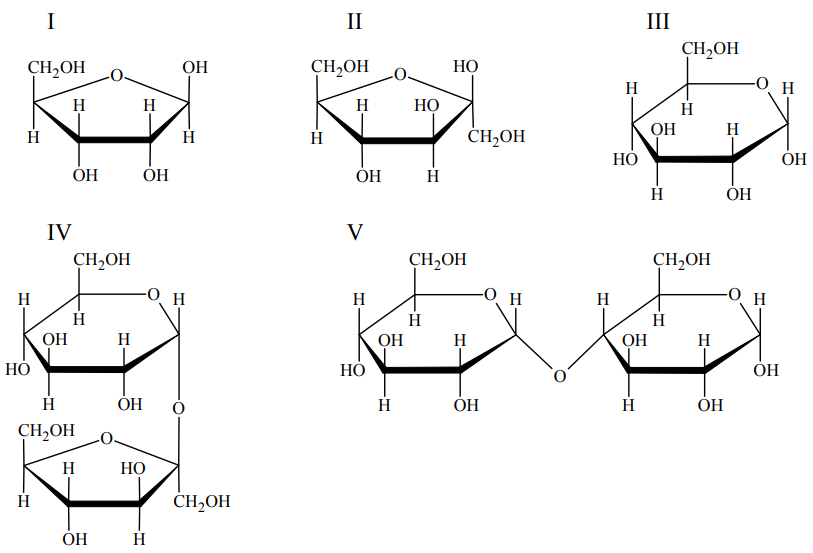
Wskaż wszystkie sacharydy, które dają pozytywny wynik próby Tollensa. Numery wzorów wybranych sacharydów:
Bilans jonowo-elektronowy reakcji glukozy z odczynnikiem Tollensa. Zadanie 29ab. Arkusz CKE chemia maj 2012 rozszerzony (3 punkty)
Reakcja glukozy z odczynnikiem Tollensa przebiega zgodnie z poniższym schematem:
CH2OH–(CHOH)4–CHO + Ag(NH3)2+ + OH– → CH2OH–(CHOH)4–COO– + Ag + NH3 + H2O
a) Napisz w formie jonowej z uwzględnieniem pobranych lub oddanych elektronów (zapis jonowo-elektronowy) równania procesów redukcji i utleniania. Równanie procesu redukcji: Równanie procesu utleniania: b) Dobierz i uzupełnij współczynniki stechiometryczne w poniższym schemacie.![]()
Zapis wzoru sumarycznego alkanu oraz wzorów grupowych i nazw jego dwóch monochloropochodnych. Zadanie 30ab. Arkusz CKE chemia maj 2012 rozszerzony (3 punkty)
Pewien alkan o rozgałęzionym łańcuchu węglowym poddano chlorowaniu, otrzymując dwie izomeryczne monochloropochodne o masie molowej M = 92,5 g·mol–1.
a) Napisz wzór sumaryczny alkanu poddanego chlorowaniu. b) Napisz wzory półstrukturalne (grupowe) obu otrzymanych monochloropochodnych tego alkanu oraz podaj ich nazwy systematyczne.