Obliczanie masy atomowej galu. Zadanie 4. Arkusz CKE chemia maj 2014 rozszerzony (1 punkt)
W poniższej tabeli przedstawiono masy atomowe i zawartość procentową trwałych izotopów galu występujących w przyrodzie.
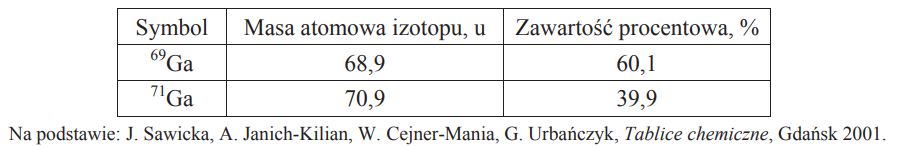
Oblicz masę atomową galu. Wynik zaokrąglij do pierwszego miejsca po przecinku.
Zapis równania reakcji jądrowej. Zadanie 5. Arkusz CKE chemia maj 2014 rozszerzony (1 punkt)
Radioaktywny izotop galu o liczbie masowej równej 67 jest stosowany w medycynie nuklearnej. Otrzymuje się go w reakcji zachodzącej podczas bombardowania protonami jąder izotopu cynku o liczbie masowej równej 68.
Napisz równanie opisanego procesu, uzupełniając poniższy schemat.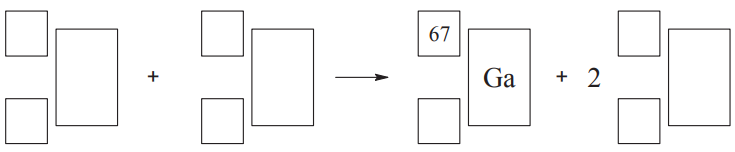
Wybór poprawnych określeń dotyczących niesparowanego elektronu w atomie galu. Zadanie 6. Arkusz CKE chemia maj 2014 rozszerzony (1 punkt)
W stanie podstawowym atom galu ma jeden niesparowany elektron.
Uzupełnij zdania. Wybierz i podkreśl symbol typu podpowłoki oraz wartość głównej i pobocznej liczby kwantowej spośród podanych w nawiasach. Niesparowany elektron atomu galu w stanie podstawowym należy do podpowłoki typu (s / p / d). Główna liczba kwantowa n opisująca stan tego elektronu wynosi (2 / 3 / 4), a poboczna liczba kwantowa l jest równa (0 / 1 / 2 / 3).
Zapis równań reakcji galu z roztworem kwasu i roztworem zasady. Zadanie 7. Arkusz CKE chemia maj 2014 rozszerzony (2 punkty)
Gal jest metalem, który roztwarza się w mocnych kwasach oraz mocnych zasadach. W reakcjach tych tworzy sole, przechodząc na stopień utlenienia III. Drugi produkt tych reakcji jest taki sam jak w reakcjach glinu z mocnymi kwasami i zasadami. Poniżej przedstawiono schemat reakcji galu z mocnymi kwasami i zasadami.
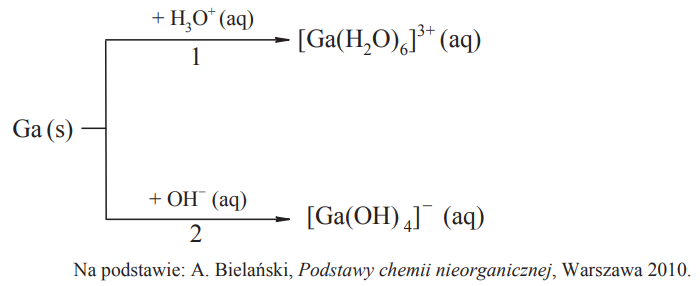
Napisz w formie jonowej skróconej równania reakcji oznaczonych numerami 1 i 2. 1: 2:
Obliczanie stężenia molowego kwasu w określonym momencie reakcji. Zadanie 8. Arkusz CKE chemia maj 2014 rozszerzony (2 punkty)
Po wrzuceniu 0,720 g magnezu do 0,150 dm3 kwasu solnego o stężeniu 0,120 mol·dm–3 zaszła reakcja opisana równaniem:
Mg + 2H3O+ → Mg2+ + H2 + 2H2O
Oblicz stężenie molowe kwasu solnego w momencie, gdy przereagowało 20% masy magnezu. W obliczeniach przyjmij, że objętość roztworu się nie zmienia. Wynik podaj z dokładnością do dwóch miejsc po przecinku.
Rysowanie kreskowego wzoru elektronowego kwasu borowego oraz wyjaśnienie, dlaczego jest akceptorem jonów wodorotlenkowych. Zadanie 9. Arkusz CKE chemia maj 2014 rozszerzony (2 punkty)
Kwas ortoborowy H3BO3 jest bardzo słabym wieloprotonowym kwasem, który w roztworach wodnych działa nie jako donor protonów, lecz jako akceptor jonów wodorotlenkowych, reagując z wodą zgodnie z równaniem:
H3BO3 + 2H2O ⇄ H3O+ + [B(OH)4]–
Stała równowagi tej reakcji jest równa 5,8·10–10 . W obecności środków odciągających wodę, np. stężonego H2SO4, kwas ortoborowy tworzy z alkoholami estry.
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2010.
Narysuj wzór elektronowy cząsteczki kwasu ortoborowego, oznaczając kreskami wiązania oraz wolne pary elektronowe. Wyjaśnij, dlaczego kwas borowy jest akceptorem jonów wodorotlenkowych.
Wskazanie nazwy tworzącego się wiązania chemicznego. Zadanie 10. Arkusz CKE chemia maj 2014 rozszerzony (1 punkt)
Kwas ortoborowy H3BO3 jest bardzo słabym wieloprotonowym kwasem, który w roztworach wodnych działa nie jako donor protonów, lecz jako akceptor jonów wodorotlenkowych, reagując z wodą zgodnie z równaniem:
H3BO3 + 2H2O ⇄ H3O+ + [B(OH)4]–
Stała równowagi tej reakcji jest równa 5,8·10–10 . W obecności środków odciągających wodę, np. stężonego H2SO4, kwas ortoborowy tworzy z alkoholami estry.
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2010.
Nazwij typ wiązania (ze względu na sposób jego powstawania), jakie tworzy się między atomem boru w cząsteczce kwasu ortoborowego i anionem wodorotlenkowym.
Zapis równania reakcji kwasu ortoborowego z metanolem. Zadanie 12. Arkusz CKE chemia maj 2014 rozszerzony (1 punkt)
Kwas ortoborowy H3BO3 jest bardzo słabym wieloprotonowym kwasem, który w roztworach wodnych działa nie jako donor protonów, lecz jako akceptor jonów wodorotlenkowych, reagując z wodą zgodnie z równaniem:
H3BO3 + 2H2O ⇄ H3O+ + [B(OH)4]–
Stała równowagi tej reakcji jest równa 5,8·10–10 . W obecności środków odciągających wodę, np. stężonego H2SO4, kwas ortoborowy tworzy z alkoholami estry.
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2010.
Napisz, posługując się wzorami półstrukturalnymi (grupowymi) związków organicznych, równanie reakcji kwasu ortoborowego z metanolem, w której stosunek molowy kwasu do alkoholu jest równy 1 : 3.
Obliczanie standardowej entalpii uwodornienia etenu. Zadanie 13. Arkusz CKE chemia maj 2014 rozszerzony (2 punkty)
W tabeli podano wartości standardowej molowej entalpii trzech reakcji.
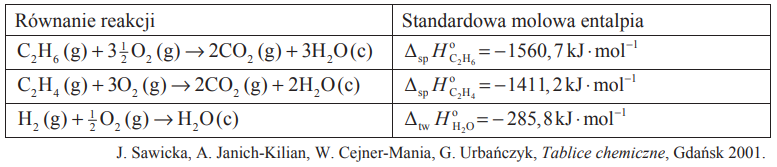
Na podstawie powyższych danych oblicz standardową molową entalpię reakcji uwodornienia etenu ΔHox, która zachodzi zgodnie z równaniem: C2H4(g) + H2(g) → C2H6(g) Wynik podaj z dokładnością do pierwszego miejsca po przecinku.
Wskazanie nazwy systematycznej kwasu izocytrynowego. Zadanie 14. Arkusz CKE chemia maj 2014 rozszerzony (1 punkt)
Kwas cytrynowy (kwas 2-hydroksypropano-1,2,3-trikarboksylowy) o składzie C6H8O7 spełnia ważną funkcję w metabolizmie organizmów jako produkt przejściowy cyklu Krebsa, w którym ulega izomeryzacji do kwasu izocytrynowego o następującym wzorze:
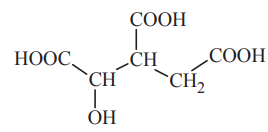
Podaj nazwę systematyczną kwasu izocytrynowego.
Rysowanie wzoru grupowego kwasu cytrynowego. Zadanie 15. Arkusz CKE chemia maj 2014 rozszerzony (1 punkt)
Kwas cytrynowy (kwas 2-hydroksypropano-1,2,3-trikarboksylowy) o składzie C6H8O7 spełnia ważną funkcję w metabolizmie organizmów jako produkt przejściowy cyklu Krebsa, w którym ulega izomeryzacji do kwasu izocytrynowego o następującym wzorze:

Napisz wzór półstrukturalny (grupowy) kwasu cytrynowego.
Wskazanie liczb asymetrycznych atomów węgla oraz enancjomerów dotyczących kwasu cytrynowego oraz izocytrynowego. Zadanie 16. Arkusz CKE chemia maj 2014 rozszerzony (2 punkty)
Kwas cytrynowy (kwas 2-hydroksypropano-1,2,3-trikarboksylowy) o składzie C6H8O7 spełnia ważną funkcję w metabolizmie organizmów jako produkt przejściowy cyklu Krebsa, w którym ulega izomeryzacji do kwasu izocytrynowego o następującym wzorze:

Przeanalizuj budowę cząsteczek kwasu cytrynowego i izocytrynowego ze względu na możliwość wystąpienia enancjomerii (izomerii optycznej). Wpisz w tabeli liczbę asymetrycznych atomów węgla w cząsteczkach tych kwasów oraz liczbę enancjomerów (izomerów optycznych) lub zaznacz ich brak.
Wskazanie właściwego wyrażenia z entalpią reakcji. Zadanie 17a. Arkusz CKE chemia maj 2014 rozszerzony (1 punkt)
Do wodnego roztworu kwasu cytrynowego dodano nadmiar wodnego roztworu wodorowęglanu sodu NaHCO3. Stwierdzono, że temperatura mieszaniny poreakcyjnej jest znacznie niższa niż temperatura roztworów przed ich zmieszaniem. Zaobserwowano także wydzielanie bezbarwnego gazu.
Spośród podanych zależności wybierz i podkreśl tę, która jest prawdziwa dla entalpii procesu dokonującego się w opisanym doświadczeniu. ΔH < 0 ΔH = 0 ΔH > 0
Zapis równania reakcji kwasu cytrynowego z wodorowęglanem sodu w wodnym roztworze. Zadanie 17b. Arkusz CKE chemia maj 2014 rozszerzony (1 punkt)
Do wodnego roztworu kwasu cytrynowego dodano nadmiar wodnego roztworu wodorowęglanu sodu NaHCO3. Stwierdzono, że temperatura mieszaniny poreakcyjnej jest znacznie niższa niż temperatura roztworów przed ich zmieszaniem. Zaobserwowano także wydzielanie bezbarwnego gazu.
Napisz w formie cząsteczkowej równanie reakcji, która zaszła w czasie doświadczenia. Przyjmij, że kwas cytrynowy przereagował z wodorowęglanem sodu w stosunku molowym 1 : 3. Zastosuj następujący wzór kwasu cytrynowego: C3H4(OH)(COOH)3.

