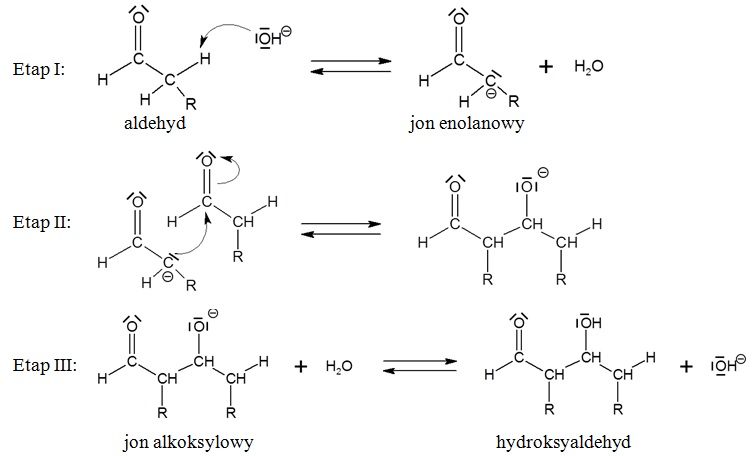
Zadanie 33. Arkusz Palladium kwiecień 2019 (1 punkt)
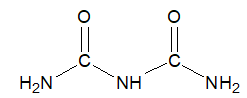
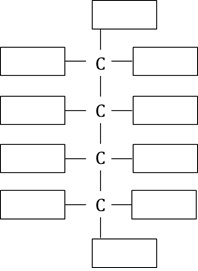
Ftalimidek potasu jest pochodną kwasu ftalowego (kwasu benzeno-1,2-dikarboksylowego). Wzór chemiczny tego związku chemicznego można przedstawić w postaci:
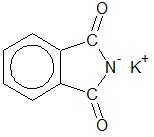
Określ liczbę wiązań σ w kryształach ftalimidku potasu zawierających 0,02 mola jonów. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 36. Arkusz Palladium kwiecień 2019 (1 punkt)
W czterech zlewkach znajdowały się wodne roztwory o takim samym stężeniu molowym następujących związków chemicznych: octanu sodu, chlorku etanoamoniowego, fenolanu potasu oraz siarczanu(VI) sodu.
Stosując półstrukturalne (grupowe) wzory związków organicznych uszereguj podane roztwory zgodnie ze wzrostem wartości ich pH. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wybór związków chemicznych, których wodne roztwory dobrze przewodzą prąd elektryczny (elektroliza)
Aby wodny roztwór związku chemicznego mógł przewodzić prąd elektryczny, w układzie muszą znajdować się swobodnie poruszające się nośniki ładunku elektrycznego.
Spośród wymienionych związków chemicznych podkreśl wzory (lub nazwy) tych, których wodne roztwory po umieszczeniu w nich elektrod i zamknięciu obwodu elektrycznego będą dobrze przewodzić prąd elektryczny. CH3COOH, sacharoza, Ba(OH)2, CH3NH2, glukoza, etanol, HClO3, Na2CO3, CuSO4, NH3. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wybór substancji, której kryształy przewodzą prąd elektryczny (elektroliza)
W stałym stanie skupienia kryształy niektórych substancji chemicznych dobrze przewodzą prąd elektryczny.
Wśród niżej wymienionych podkreśl nazwy tych substancji chemicznych, których kryształy wykazują opisaną wyżej własność. Diament, miedź, siarka, chlorek sodu, grafit, sacharoza, glukoza, wodorotlenek potasu. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zapis równań połówkowych procesów elektrodowych przebiegających podczas elektrolizy wodnych roztworów kwasu solnego oraz wodorotlenku sodu (elektroliza)
W kilku różnych elektrolizerach przeprowadzono (niezależnie) elektrolizę wodnych roztworów związków chemicznych: kwasu solnego, wodorotlenku sodu, siarczanu(VI) miedzi(II), bromku potasu oraz chlorku żelaza(II). Każdorazowo zastosowano elektrody platynowe.
Napisz równania połówkowe głównych procesów utleniania i redukcji, jakie przebiegły w przestrzeni katodowej oraz anodowej podczas opisanego doświadczenia z udziałem wodnych roztworów: kwasu solnego oraz wodorotlenku sodu. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zapis równań połówkowych procesów elektrodowych przebiegających podczas elektrolizy wodnych roztworów siarczanu(VI) miedzi(II), bromku potasu oraz chlorku kobaltu(II) (elektroliza)
W kilku różnych elektrolizerach przeprowadzono (niezależnie) elektrolizę wodnych roztworów związków chemicznych: kwasu solnego, wodorotlenku sodu, siarczanu(VI) miedzi(II), bromku potasu oraz chlorku kobaltu(II). Każdorazowo zastosowano elektrody platynowe.
Napisz równania połówkowe głównych procesów utleniania i redukcji, jakie przebiegły w przestrzeni katodowej oraz anodowej podczas opisanego doświadczenia z udziałem wodnych roztworów: siarczanu(VI) miedzi(II), bromku potasu oraz chlorku kobaltu(II). © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone