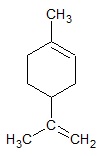
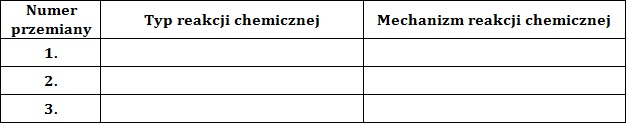
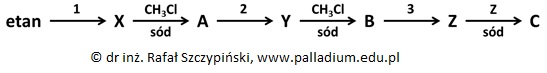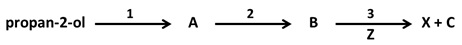Ocena, czy masa manganowej blaszki uległa zwiększeniu, czy zmniejszeniu (blaszki)
W wodnym roztworze chlorku kobaltu(II) zanurzono blaszkę wykonaną z manganu. Po zakończeniu reakcji chemicznej stwierdzono, że jej masa uległa zmianie.
Oceń, czy masa blaszki uległa zwiększeniu, czy zmniejszeniu? Odpowiedź uzasadnij odpowiednimi obliczeniami. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określanie wzoru półstrukturalnego oraz nazwy związku organicznego (izomeria optyczna)
Pewien występujący w postaci enancjomerów nasycony, alifatyczny keton łańcuchowy A poddano redukcji wodorem. Produkt B tej reakcji odwodniono w obecności tlenku glinu i uzyskano równomolową mieszaninę alkenów C i D. Związek C występuje jako para izomerów geometrycznych, natomiast związek D – enancjomerów. Centrum chiralności związku D jest ten sam atom węgla, co w wyjściowym ketonie A. Głównymi produktami addycji wody do związków chemicznych C i D są alkohole o najwyższej rzędowości.
Wiedząc, że produktem addycji wodoru do alkenów jest 2,4-dimetyloheksan, podaj wzór półstrukturalny oraz nazwę systematyczną związku chemicznego A. Zapisz numer lokantu, którym opisany jest asymetryczny atom węgla w jego cząsteczce. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Procent wagowy jonów węglanowych w musującej tabletce suplementującej magnez
Niedobory jonów Mg2+ powstałe w wyniku ciężkiego wysiłku fizycznego mogą być uzupełniane w wyniku ich suplementacji za pomocą musujących tabletek zawierających węglan magnezu, kwas cytrynowy, kwas jabłkowy oraz inne substancje pomocnicze.
Wiedząc, że opakowanie zawiera 20 tabletek, a ich sumaryczna masa wynosi 80 g, oblicz, jaki procent wagowy w musującej tabletce stanowią jony węglanowe pochodzące z węglanu magnezu, jeśli jony Mg2+ ważą 200 mg w przeliczeniu na jedną tabletkę? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określanie liczby wiązań sigma oraz typu hybrydyzacji orbitali walencyjnych atomu węgla w karbokationie
W pierwszym etapie reakcji alkenu z wodą w obecności rozcieńczonego kwasu siarkowego(VI) powstaje karbokation. Ogólny schemat budowy takiej drobiny przedstawia rysunek:
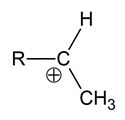
Określ liczbę wiązań σ jakie tworzy atom węgla na którym zlokalizowany jest ładunek dodatni oraz typ hybrydyzacji (sp, sp2, sp3) jego orbitali walencyjnych. Liczba wiązań σ: Typ hybrydyzacji: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wyjaśnienie dużej różnicy w temperaturach wrzenia alkoholu oraz izomerycznego z nim nadtlenku organicznego
W wodnym 10,3-procentowym roztworze pewnego nasyconego alkoholu na jedną jego cząsteczkę przypada trzydzieści cząsteczek wody. Związek ten roztwarza świeżo strącony osad wodorotlenku miedzi(II) z utworzeniem szafirowego klarownego roztworu. Temperatura wrzenia opisanego alkoholu pod ciśnieniem normalnym wynosi 470 K. Przy identycznej wartości ciśnienia, jeden z jego izomerów wrze w temperaturze 287 K i należy do szeregu homologicznego tzw. nadtlenków organicznych, czyli związków chemicznych o wzorze ogólnym w postaci R1–O–O–R2. We wzorze tym R1 oraz R2 stanowią reszty cząsteczek tego samego, bądź różnych węglowodorów.
Na podstawie: www.pubchem.com oraz W. Mizerski, Tablice chemiczne, Warszawa 2013.
Wyjaśnij, czym spowodowana jest tak duża różnica w wartościach temperatur wrzenia wymienionych izomerycznych związków chemicznych? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Rysowanie wzoru półstrukturalnego trans-1,2-difenyloetylenu na podstawie jego nazwy (izomeria geometryczna)
Difenyloacetylen można otrzymać w dwuetapowym procesie:
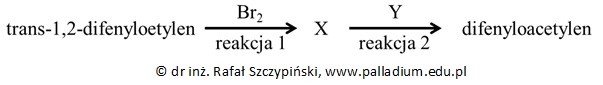
Narysuj wzór półstrukturalny (grupowy) trans-1,2-difenyloetylenu. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Bilansowanie równania reakcji nadtlenku wodoru z manganianem(VII) potasu w środowisku obojętnym
Do wodnego roztworu manganianu(VII) potasu dodano roztwór zawierający stechiometryczną względem KMnO4 ilość nadtlenku wodoru. Zaobserwowano dwie zmiany świadczące o przebiegu reakcji chemicznej. Ponadto roztwór tylko nieznaczenie uległ odbarwieniu.
Napisz, jakie dwie zmiany (poza nieznacznym odbarwieniem roztworu) odnotowano? Odpowiedź uzasadnij równaniem reakcji chemicznej zapisanym w formie jonowej skróconej. Współczynniki uzgodnij metodą bilansu jonowo-elektronowego. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Przypisywanie modelu hybrydyzacji atomom węgla w cząsteczce difenyloacetylenu oraz określanie liczby wiązań σ oraz π w cząsteczce węglowodoru
Difenyloacetylen można otrzymać w dwuetapowym procesie:
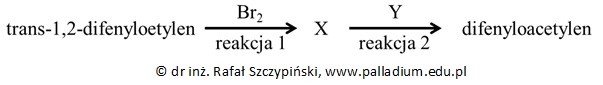
Określ typ hybrydyzacji (sp, sp2, sp3) jaką można przypisać orbitalom walencyjnym alifatycznych atomów węgla w cząsteczce difenyloacetylenu. Podaj liczbę wiązań σ oraz liczbę wiązań π znajdujących się w cząsteczce tego węglowodoru. Typ hybrydyzacji: ……….. Liczba wiązań σ: ……….. Liczba wiązań π: ……….. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone