Uzasadnienie, czy przeprowadzone doświadczenie jest wystarczające, aby określić charakter chemiczny wodorotlenku galu. Podręcznik 7.2 zad. 4
Na świeżo strącony osad wodorotlenku galu podziałano nadmiarem roztworu wodorotlenku potasu. Po wstrząśnięciu zawartością naczynia reakcyjnego stwierdzono, że cały osad uległ roztworzeniu.
Oceń, czy przeprowadzone doświadczenie było wystarczające, aby stwierdzić amfoteryczny charakter tlenku galu? Odpowiedź uzasadnij. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
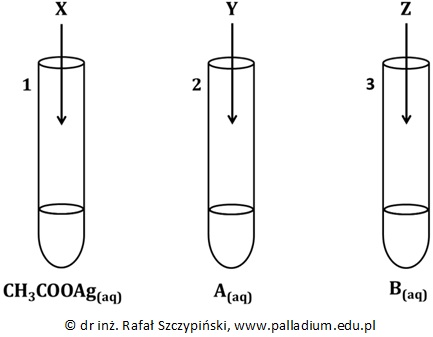
Odróżnianie wodnych roztworów siarczanu(VI) cynku oraz siarczanu(VI) magnezu. Podręcznik 7.2 zad. 5
W dwóch nieopisanych probówkach znajdują się wodne roztwory – siarczanu(VI) cynku oraz siarczanu(VI) magnezu.
Zaproponuj doświadczenie, którego celem będzie odróżnienie od siebie zawartości obu naczyń. W tym celu wybierz jeden z podanych odczynników, a następnie opisz tok postępowania, w którym przedstawisz stosowne obserwacje oraz wnioski. Dostępne odczynniki: HCl(aq), KOH(aq), BaCl2(aq), fenoloftaleina. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obserwacje na podstawie przeprowadzonego eksperymentu z udziałem tlenków metali oraz wodorotlenków. Podręcznik 7.2 zad. 6
Rozpuszczalność wodorotlenku potasu w temperaturze 20 ⁰C wynosi 85 g/100 g wody. Przeprowadzono doświadczenie chemiczne, opisane poniższym rysunkiem:
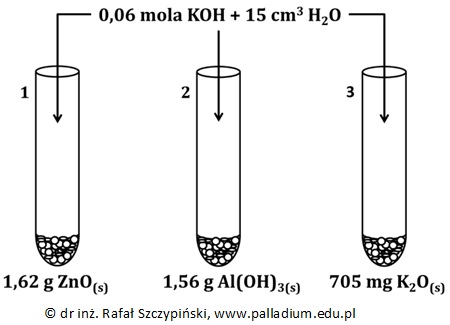
Napisz, co zaobserwowano w każdej z probówek podczas przebiegu tego eksperymentu? Odpowiedź uzasadnij stosownymi obliczeniami. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wskazanie równania reakcji redoks oraz wzoru utleniacza i reduktora. Podręcznik 8.1 zad. 1
Poniżej zapisano równania kilku reakcji chemicznych.
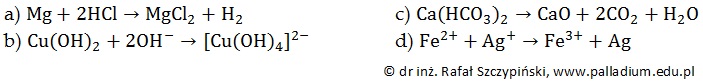
Określ, które z opisanych wyżej przemian należą do reakcji redoks? Następnie wskaż drobinę pełniącą wówczas rolę utleniacza oraz drobinę będącą reduktorem. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wskazanie kationu, który w danej parze jest silniejszym utleniaczem. Podręcznik 8.1 zad. 2
Poniżej podano pary kilku wybranych kationów metali.

Korzystając z szeregu napięciowego metali oraz półogniw redoks wskaż (wstawiając znak „<” lub „>”), który jon w danej parze kationów jest silniejszym utleniaczem? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Przygotowanie roztworu zawierającego jony Zn2+ o określonym stężeniu molowym (blaszki). Podręcznik 8.2 zad. 5
Cynk jest metalem aktywniejszym od miedzi.
Wykonując stosowne obliczenia oraz dysponując wodą destylowaną, niezbędnym szkłem laboratoryjnym, blaszką cynkową o masie 5 g oraz 80 cm³ wodnego roztworu siarczanu(VI) miedzi(II) o stężeniu 0,25 mol∙dm–3, zaprojektuj doświadczenie, którego celem będzie uzyskanie roztworu o stężeniu jonów Zn2+ równym 0,2 mol∙dm–3. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Odróżnianie wodnych roztworów azotanu(V) srebra różniących się stężeniem molowym (blaszki). Podręcznik 8.2 zad. 6
W dwóch nieopisanych kolbach miarowych o pojemności 250 cm3 każda, znajdowały się jednakowe objętości wodnych roztworów azotanu(V) srebra o stężeniach 0,1 mol∙dm–3 oraz 0,5 mol∙dm–3.
Zaproponuj doświadczenie, którego celem będzie odróżnienie zawartości wymienionych naczyń, jeśli dysponujesz identycznymi blaszkami cynkowymi, wagą laboratoryjną, cylindrem miarowym oraz dwiema zlewkami. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wybór metalu spełniającego odpowiednie warunki w reakcji z kwasem. Podręcznik 8.2 zad. 7
Dany jest zbiór metali: Zn, Cu, Ca, Cr, Al, Fe, Na, Mg.
Podaj symbole tych spośród wymienionych pierwiastków chemicznych, które spełniają niżej wymienione warunki. a) Reagują z rozcieńczonym roztworem H2SO4 „na gorąco”. b) W temperaturze pokojowej reagują ze stężonym roztworem HNO3. c) W podwyższonej temperaturze roztwarzają się w stężonym kwasie solnym. d) Nie reagują z rozcieńczonym roztworem kwasu ortofosforowego(V). © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wybór odpowiedniego metalu spełniającego rolę powłoki zabezpieczającej stal przed korozją (korozja). Podręcznik 8.2 zad. 8
Podczas działania czynników atmosferycznych na elementy stalowe dochodzi do ich korozji elektrochemicznej.
Który metal spośród Cu, Ca, Zn, Pb zostałby przez Ciebie wykorzystany, w celu zabezpieczenia przed korozją stalowej blachy służącej do budowy dachu? Odpowiedź uzasadnij. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Odróżnianie roztworu kwasu siarkowego(VI) od roztworu wodorotlenku sodu. Podręcznik 8.3 zad. 1
W dwóch probówkach znajdowały się wodne roztwory – kwasu siarkowego(VI) oraz zasady sodowej.
Zaprojektuj doświadczenie, którego celem będzie odróżnienie zawartości wymienionych naczyń. W tym celu wybierz dwa spośród dostępnych odczynników: NaClO3(aq), KMnO4(aq), HNO3(aq), H2O2(aq), H3PO4(aq). Następnie podaj obserwacje oraz wnioski, wraz z zapisanymi w formie jonowej skróconej równaniami przebiegających reakcji chemicznych. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Opis obserwacji towarzyszących przeprowadzonemu doświadczeniu odróżniania rozcieńczonych roztworów wodorotlenków. Podręcznik 8.4 zad. 1
Przeprowadzono doświadczenie chemiczne, którego celem było odróżnienie rozcieńczonych, wodnych roztworów wodorotlenków – baru oraz potasu. W tym celu rozkładowi termicznemu poddano próbkę węglanu wapnia, a wydzielający się gazowy produkt wprowadzano do każdego z naczyń zawierających identyfikowane roztwory. Ogrzewanie węglanu przerwano, gdy w jednym z naczyń zarejestrowano objaw świadczący o przebiegającej w nim reakcji chemicznej.
Napisz, o jakim objawie przebiegu reakcji mowa jest w tekście wprowadzającym? Swoją odpowiedź uzasadnij równaniem reakcji chemicznej, zapisanym w formie jonowej skróconej. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone