Zapis równania reakcji nadtlenku sodu z wodą. Zadanie 6.2. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
Produktem spalania metalicznego sodu w tlenie jest nadtlenek sodu o wzorze Na2O2. W wyniku reakcji tego związku z sodem w podwyższonej temperaturze można otrzymać tlenek sodu Na2O. Każdy z opisanych związków sodu z tlenem ma budowę jonową i tworzy sieć krystaliczną zbudowaną z kationów i anionów. Nadtlenek sodu reaguje gwałtownie z wodą. Jednym z produktów tej reakcji, zachodzącej bez zmiany stopni utlenienia, jest nadtlenek wodoru H2O2.
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2006.
Napisz w formie cząsteczkowej równanie reakcji nadtlenku sodu z wodą.
Zapis równania reakcji przebiegającej po zmieszaniu wodnych roztworów jodku potasu i siarczanu(VI) miedzi(II). Zadanie 7. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
Przeprowadzono doświadczenie zilustrowane schematem.
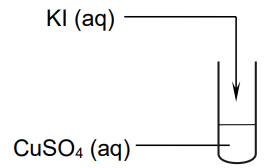
Po zmieszaniu obu roztworów zaszła reakcja utleniania i redukcji, w wyniku której wytrącił się biały osad jodku miedzi(I) i wydzielił się wolny jod.
Napisz w formie jonowej skróconej równanie reakcji, która zaszła po zmieszaniu roztworów KI i CuSO4.
Rozstrzygnięcie wraz z uzasadnieniem, czy kwas solny przereaguje z miedzią. Zadanie 8.1. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
Poniższy schemat przedstawia przemiany, jakim ulegają miedź i jej związki.
![]()
Rozstrzygnij, czy substancją A może być kwas solny o stężeniu 10 % masowych. Uzasadnij swoją odpowiedź. W uzasadnieniu odwołaj się do właściwości miedzi i kwasu solnego. Rozstrzygnięcie: Uzasadnienie:
Zapis wzoru wybranej substancji chemicznej oraz równania reakcji. Zadanie 8.2. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
Poniższy schemat przedstawia przemiany, jakim ulegają miedź i jej związki.
![]()
Napisz wzór sumaryczny substancji B, jeśli wiadomo, że po zajściu reakcji i odsączeniu osadu w roztworze obecne były kationy sodu i aniony chlorkowe. Napisz w formie jonowej równanie reakcji 3., której produktem jest m.in. jon kompleksowy o wzorze [Cu(NH3)4]2+. Wzór substancji B: Równanie reakcji 3.:
Wybór związków chemicznych roztwarzających wodorotlenek miedzi(II). Zadanie 8.3. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
Poniższy schemat przedstawia przemiany, jakim ulegają miedź i jej związki.
![]()
Spośród podanych poniżej wzorów wybierz wzory wszystkich substancji, w których wodnych roztworach na zimno roztwarza się wodorotlenek miedzi(II). Napisz numery wybranych wzorów. Wybrane wzory: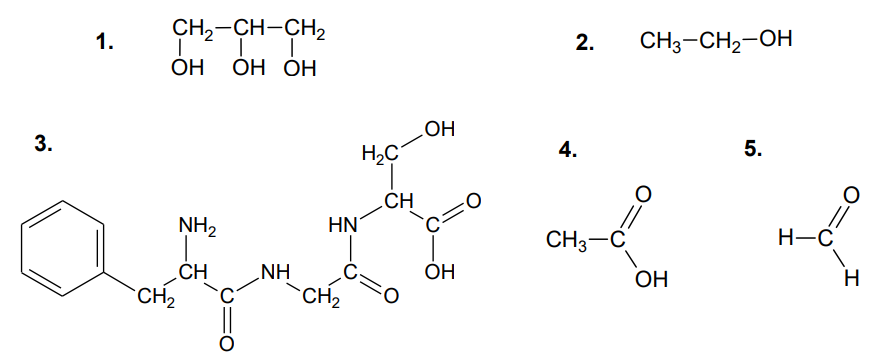
Zapis równania reakcji chemicznej w formie jonowej skróconej oraz wybór właściwej probówki. Zadanie 9.1. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
W dwóch probówkach oznaczonych numerami I i II umieszczono jednakową ilość wiórków magnezowych o tym samym stopniu rozdrobnienia. Następnie do probówek wprowadzono jednakowe objętości roztworów o tej samej temperaturze:
– do probówki I – kwas solny o pH = 1
– do probówki II – wodny roztwór kwasu siarkowego(VI) o stężeniu 0,1 mol·dm–3 .
Przebieg doświadczenia zilustrowano poniższym rysunkiem.
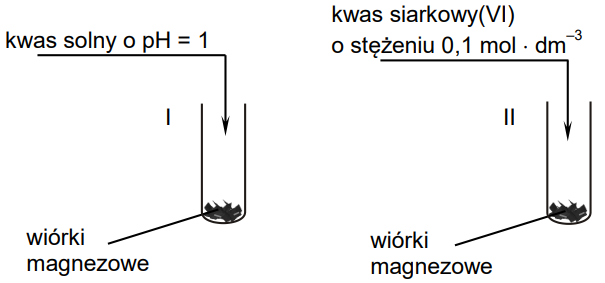
Podczas opisanego doświadczenia w każdej probówce wiórki magnezowe uległy całkowitemu roztworzeniu i powstały klarowne, bezbarwne roztwory, ale w jednej z probówek reakcja przebiegła szybciej.
Napisz w formie jonowej skróconej równanie reakcji, która zaszła podczas opisanego doświadczenia w obu probówkach. Wskaż numer probówki (I albo II), w której wiórki magnezowe roztworzyły się szybciej. Równanie reakcji: Wiórki magnezowe roztworzyły się szybciej w probówce numer
Wybór właściwych określeń dotyczących przebiegu doświadczenia chemicznego. Zadanie 9.2. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
W dwóch probówkach oznaczonych numerami I i II umieszczono jednakową ilość wiórków magnezowych o tym samym stopniu rozdrobnienia. Następnie do probówek wprowadzono jednakowe objętości roztworów o tej samej temperaturze:
– do probówki I – kwas solny o pH = 1
– do probówki II – wodny roztwór kwasu siarkowego(VI) o stężeniu 0,1 mol·dm–3 .
Przebieg doświadczenia zilustrowano poniższym rysunkiem.

Podczas opisanego doświadczenia w każdej probówce wiórki magnezowe uległy całkowitemu roztworzeniu i powstały klarowne, bezbarwne roztwory, ale w jednej z probówek reakcja przebiegła szybciej.
Uzupełnij poniższe zdanie – wybierz i zaznacz jedną odpowiedź spośród podanych w każdym nawiasie. Stężenie molowe roztworów obu kwasów było (równe / różne), a stężenie jonów H+ w tych roztworach było (równe / różne), dlatego opisane doświadczenie pozwoliło określić wpływ (stężenia molowego / pH) roztworów użytych kwasów na szybkość reakcji.
Wybór czynności pozwalającej na wyodrębnienie składnika z mieszaniny. Zadanie 10. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
W dwóch probówkach oznaczonych numerami I i II umieszczono jednakową ilość wiórków magnezowych o tym samym stopniu rozdrobnienia. Następnie do probówek wprowadzono jednakowe objętości roztworów o tej samej temperaturze:
– do probówki I – kwas solny o pH = 1
– do probówki II – wodny roztwór kwasu siarkowego(VI) o stężeniu 0,1 mol·dm–3 .
Przebieg doświadczenia zilustrowano poniższym rysunkiem.

Podczas opisanego doświadczenia w każdej probówce wiórki magnezowe uległy całkowitemu roztworzeniu i powstały klarowne, bezbarwne roztwory, ale w jednej z probówek reakcja przebiegła szybciej.
Którą czynność należy wykonać w celu wyodrębnienia z mieszaniny poreakcyjnej jonowego produktu otrzymanego w probówce I? Zaznacz właściwą odpowiedź spośród podanych. A. Sączenie B. Dekantacja C. Odwirowanie D. Odparowanie pod wyciągiem
Zapis w formie jonowej skróconej równania reakcji chemicznej oraz wybór właściwego odczynnika. Zadanie 12.1. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
W trzech probówkach (I–III) umieszczono wodne roztwory soli potasu zawierających chrom na VI stopniu utlenienia. Zawartość probówki III zakwaszono. Następnie do każdej probówki dodano jeden odczynnik wybrany z poniższej listy:
– wodny roztwór wodorotlenku potasu
– wodny roztwór azotanu(V) sodu
– wodny roztwór azotanu(V) srebra(I)
– wodny roztwór siarczanu(IV) potasu.
Schemat doświadczenia i opis wyglądu zawartości probówek I–III przed reakcją i po jej zakończeniu przedstawiono w poniższej tabeli.
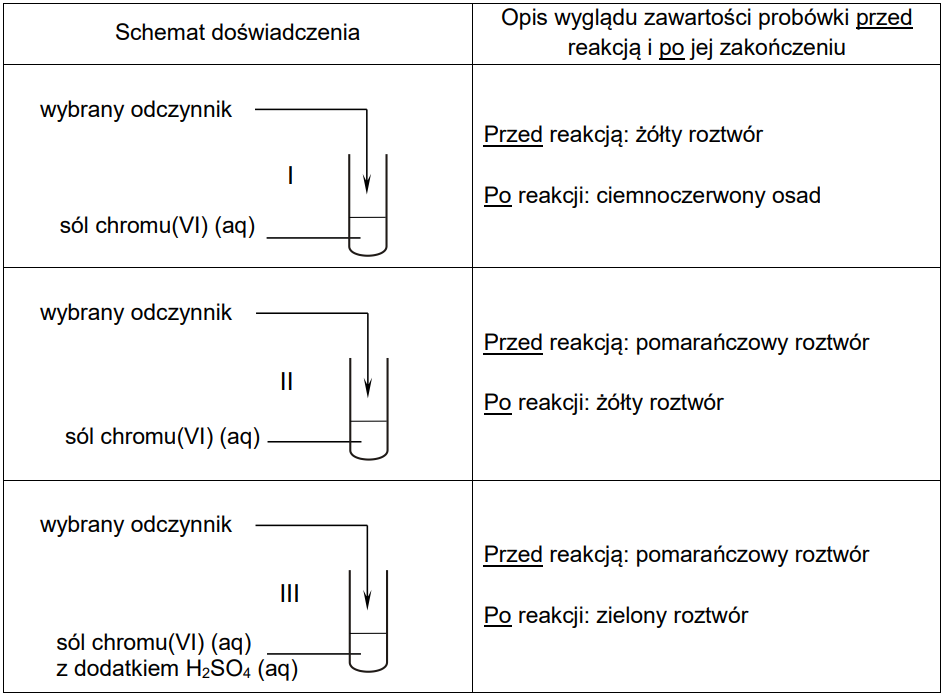
Napisz w formie jonowej skróconej równanie reakcji zachodzącej w probówce I po dodaniu wybranego odczynnika do roztworu soli chromu(VI) oraz napisz nazwę lub wzór odczynnika, który dodano do probówki II w opisanym doświadczeniu. Równanie reakcji zachodzącej w probówce I: Nazwa lub wzór odczynnika dodanego do probówki II:
Zapis w formie jonowej skróconej równania reakcji chemicznej. Zadanie 12.2. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
W trzech probówkach (I–III) umieszczono wodne roztwory soli potasu zawierających chrom na VI stopniu utlenienia. Zawartość probówki III zakwaszono. Następnie do każdej probówki dodano jeden odczynnik wybrany z poniższej listy:
– wodny roztwór wodorotlenku potasu
– wodny roztwór azotanu(V) sodu
– wodny roztwór azotanu(V) srebra(I)
– wodny roztwór siarczanu(IV) potasu.
Schemat doświadczenia i opis wyglądu zawartości probówek I–III przed reakcją i po jej zakończeniu przedstawiono w poniższej tabeli.

Napisz w formie jonowej skróconej równanie reakcji zachodzącej w probówce III po dodaniu wybranego odczynnika do roztworu soli chromu(VI) z dodatkiem H2SO4.
Wybór właściwych odpowiedzi dotyczących przeprowadzonego doświadczenia. Zadanie 12.3. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
W trzech probówkach (I–III) umieszczono wodne roztwory soli potasu zawierających chrom na VI stopniu utlenienia. Zawartość probówki III zakwaszono. Następnie do każdej probówki dodano jeden odczynnik wybrany z poniższej listy:
– wodny roztwór wodorotlenku potasu
– wodny roztwór azotanu(V) sodu
– wodny roztwór azotanu(V) srebra(I)
– wodny roztwór siarczanu(IV) potasu.
Schemat doświadczenia i opis wyglądu zawartości probówek I–III przed reakcją i po jej zakończeniu przedstawiono w poniższej tabeli.

Uzupełnij poniższe zdania – wybierz i zaznacz jedną odpowiedź spośród podanych w każdym nawiasie. Reakcja redoks przebiegła w probówce (I / II / III). Sól chromu(VI) pełni w tej przemianie funkcję (reduktora / utleniacza).
Zapis równań reakcji utleniania oraz redukcji z udziałem związków manganu. Zadanie 13. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
Wykonano doświadczenie zilustrowane poniższym schematem.
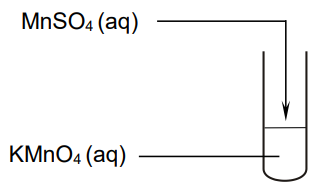
Po zakończeniu reakcji w probówce widoczne były bezbarwny roztwór i brunatny osad.
Napisz w formie jonowej skróconej, z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy), równania procesów redukcji i utleniania zachodzących podczas opisanej przemiany. Uwzględnij, że reakcja zachodzi w środowisku obojętnym. Równanie procesu redukcji: Równanie procesu utleniania:
Wskazanie najsłabszego oraz najsilniejszego reduktora na podstawie doświadczenia z blaszkami metali. Zadanie 14.1. Arkusz CKE chemia maj 2022 rozszerzony (1 punkt)
O trzech metalach umownie oznaczonych symbolami A, X i Z wiadomo, że tworzą wyłącznie kationy o wzorach X+, A2+, Z3+. Stwierdzono, że właściwości utleniające kationów tych metali maleją w szeregu: X+, A2+, Z3+.
Przeprowadzono doświadczenie z udziałem metali Z i X oraz wodnych roztworów soli, w których były obecne jony X+ i A2+. Schemat doświadczenia przedstawiono poniżej.
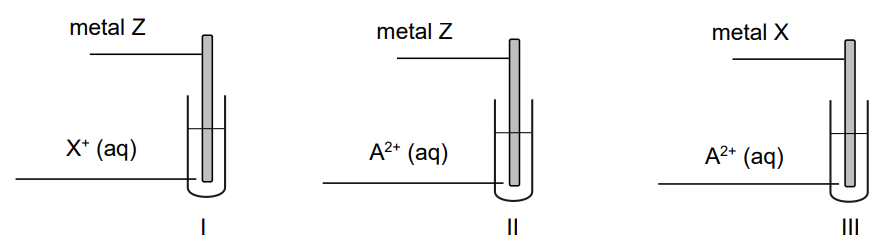
Wskaż metal, który jest najsłabszym reduktorem, oraz metal, który jest najsilniejszym reduktorem. Użyj symboli A, X albo Z. Najsłabszy reduktor: Najsilniejszy reduktor:
Wybór właściwej probówki oraz zapis równań reakcji chemicznych. Zadanie 14.2. Arkusz CKE chemia maj 2022 rozszerzony (2 punkty)
O trzech metalach umownie oznaczonych symbolami A, X i Z wiadomo, że tworzą wyłącznie kationy o wzorach X+, A2+, Z3+. Stwierdzono, że właściwości utleniające kationów tych metali maleją w szeregu: X+, A2+, Z3+.
Przeprowadzono doświadczenie z udziałem metali Z i X oraz wodnych roztworów soli, w których były obecne jony X+ i A2+. Schemat doświadczenia przedstawiono poniżej.

W jednej probówce nie zaobserwowano objawów reakcji.
Napisz numer probówki, w której nie zaobserwowano objawów reakcji. Napisz w formie jonowej skróconej równania dwóch reakcji, które przebiegły podczas przeprowadzonego doświadczenia. Użyj symboli A, X, Z. Numer probówki: Równania reakcji:

