Wybór wzoru soli oraz zapis równań reakcji chemicznych. Zadanie 9. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (2 punkty)
Przeprowadzono doświadczenie, w którym do probówki z wodnym roztworem soli pewnego metalu M (zdjęcie 1.), wprowadzono wodny roztwór wodorotlenku potasu o niewielkim stężeniu (etap I) i stwierdzono, że wytrącony osad nie roztwarza się w nadmiarze odczynnika (zdjęcie 2.). Do otrzymanej mieszaniny wkroplono stężony wodny roztwór amoniaku (etap II). W wyniku reakcji powstały jony o wzorze [M(NH3)4]2+. Wygląd zawartości probówki po zakończeniu doświadczenia przedstawiono na zdjęciu 3.

Spośród soli, których wzory wymieniono poniżej, zaznacz tę, której roztwór mógł znajdować się w probówce na początku doświadczenia. AgNO3 CrCl3 CuSO4 FeCl3 MnSO4 Napisz w formie jonowej skróconej równanie reakcji, która zaszła w etapie I opisanego doświadczenia: Napisz w formie jonowej równanie reakcji, która zaszła w etapie II opisanego doświadczenia:
Ustalanie wzoru tlenku żelaza. Zadanie 10.1. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (2 punkty)
Wodorotlenki metali ciężkich są nietrwałe i łatwo ulegają rozkładowi. W celu zbadania jednej z takich reakcji przeprowadzono następujące doświadczenie: w warunkach beztlenowych z roztworu FeCl2 wytrącono wodorotlenek żelaza(II). Po pewnym czasie stwierdzono, że z mieszaniny poreakcyjnej wydziela się bezbarwny gaz, który zapala się wybuchowo. Po ustaniu objawów reakcji jej stały produkt odsączono i całkowicie usunięto z niego wodę. Badanie składu tego związku wykazało, że jest to tlenek, zawierający 72,36 % masowych żelaza.
Na podstawie: M. Ma, Y. Zhang, Z. Gou i N. Gu, Nanoscale Research Letters, 8 (2013) 16.
Na podstawie obliczeń ustal wzór otrzymanego tlenku żelaza.
Zapis równania reakcji rozkładu wodorotlenku żelaza(II) w podanych warunkach. Zadanie 10.2. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (1 punkt)
Wodorotlenki metali ciężkich są nietrwałe i łatwo ulegają rozkładowi. W celu zbadania jednej z takich reakcji przeprowadzono następujące doświadczenie: w warunkach beztlenowych z roztworu FeCl2 wytrącono wodorotlenek żelaza(II). Po pewnym czasie stwierdzono, że z mieszaniny poreakcyjnej wydziela się bezbarwny gaz, który zapala się wybuchowo. Po ustaniu objawów reakcji jej stały produkt odsączono i całkowicie usunięto z niego wodę. Badanie składu tego związku wykazało, że jest to tlenek, zawierający 72,36 % masowych żelaza.
Na podstawie: M. Ma, Y. Zhang, Z. Gou i N. Gu, Nanoscale Research Letters, 8 (2013) 16.
Napisz w formie cząsteczkowej równanie reakcji rozkładu wodorotlenku żelaza(II), której produktem jest opisany tlenek.
Zapis równania reakcji całkowitego spalania butan-1-olu. Zadanie 11.1. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (1 punkt)
Molową entalpię spalania butan-1-olu można wyznaczyć doświadczalnie. W tym celu szklany palnik napełnia się butan-1-olem, a następnie waży. Za pomocą tak przygotowanego palnika ogrzewa się kolbę zawierającą wodę o znanej masie. Proces spalania alkoholu prowadzi się przez pewien czas, przy czym stale kontroluje się za pomocą termometru temperaturę wody w kolbie. Na zakończenie doświadczenia palnik waży się powtórnie.
Przeprowadzono opisane doświadczenie i na podstawie zmiany temperatury wody określono, że w tym doświadczeniu woda pobrała 𝑄=50 400 J energii cieplnej pochodzącej ze spalania butan-1-olu.
W tabeli poniżej zestawiono dane z pomiaru masy palnika podczas doświadczenia.

Napisz równanie reakcji spalania całkowitego butan-1-olu. Zastosuj wzory sumaryczne substratów i produktów.
Obliczanie molowej entalpii spalania butan-1-olu. Zadanie 11.2. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (2 punkty)
Molową entalpię spalania butan-1-olu można wyznaczyć doświadczalnie. W tym celu szklany palnik napełnia się butan-1-olem, a następnie waży. Za pomocą tak przygotowanego palnika ogrzewa się kolbę zawierającą wodę o znanej masie. Proces spalania alkoholu prowadzi się przez pewien czas, przy czym stale kontroluje się za pomocą termometru temperaturę wody w kolbie. Na zakończenie doświadczenia palnik waży się powtórnie.
Przeprowadzono opisane doświadczenie i na podstawie zmiany temperatury wody określono, że w tym doświadczeniu woda pobrała 𝑄=50 400 J energii cieplnej pochodzącej ze spalania butan-1-olu.
W tabeli poniżej zestawiono dane z pomiaru masy palnika podczas doświadczenia.

Na podstawie efektu cieplnego reakcji (𝑄) można obliczyć entalpię reakcji (Δ𝐻).
Oblicz molową entalpię spalania butan-1-olu. Pomiń straty ciepła. Wynik zapisz w zaokrągleniu do liczb całkowitych oraz z jednostką kJ·mol‒1. Uwzględnij odpowiedni znak entalpii reakcji.
Zapis równania reakcji usuwania przemijającej twardości wody. Zadanie 12. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (1 punkt)
W wyniku kontaktu ze skałami i z glebą woda wzbogaca się m.in. w związki wapnia. Obecność tych związków w wodzie jest przyczyną zwiększonej twardości. Twardość węglanową (przemijającą) można usunąć przez gotowanie, co prowadzi do przechodzenia wodorowęglanu wapnia w osad węglanu.
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2018.
Napisz w formie jonowej równanie reakcji, która zachodzi podczas gotowania twardej wody zawierającej wodorowęglan wapnia.
Wybór właściwych słów dotyczących kalcytu oraz aragonitu. Zadanie 13. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (1 punkt)
W wyniku kontaktu ze skałami i z glebą woda wzbogaca się m.in. w związki wapnia. Obecność tych związków w wodzie jest przyczyną zwiększonej twardości. Twardość węglanową (przemijającą) można usunąć przez gotowanie, co prowadzi do przechodzenia wodorowęglanu wapnia w osad węglanu.
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2018.
Głównym składnikiem skał wapiennych jest związek chemiczny, występujący w dwóch odmianach krystalicznych, znanych jako kalcyt i aragonit. Na poniższym wykresie przedstawiono zależność iloczynu rozpuszczalności (𝐾s) kalcytu i aragonitu od temperatury. Iloczyn rozpuszczalności jest wyrażony jako p𝐾s (p𝐾s = –log 𝐾s).
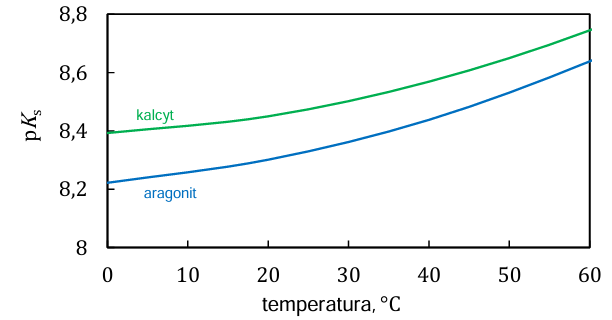
Na podstawie: L.N. Plummer, E. Busenberg, Geochimica et Cosmochimica Acta, 46 (1982) 6.
Uzupełnij poniższe zdania. Zaznacz jedną odpowiedź spośród podanych w każdym nawiasie. Wraz ze wzrostem temperatury rozpuszczalność kalcytu i aragonitu w wodzie (rośnie / maleje). W danej temperaturze rozpuszczalność aragonitu jest (większa / mniejsza) niż rozpuszczalność kalcytu.
Obliczanie pH roztworu uzyskanego w wyniku reakcji chemicznej. Zadanie 14. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (2 punkty)
Do 400 cm3 roztworu kwasu azotowego(V) o pH = 2,5 wprowadzono 120,0 mg tlenku wapnia, który po chwili roztworzył się całkowicie. Doświadczenie wykonano w temperaturze t = 25 oC .
Oblicz pH otrzymanego roztworu. Załóż, że dodatek tlenku wapnia nie zmienił objętości roztworu. Wynik zapisz w zaokrągleniu do jednego miejsca po przecinku.
Zapis równania procesu decydującego o odczynie roztworu w teorii Brønsteda. Zadanie 15.2. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (1 punkt)
W czterech zlewkach znajdowały się – w losowej kolejności – bezbarwne wodne roztwory różnych soli: węglanu sodu, azotanu(V) ołowiu(II), jodku potasu i siarczanu(VI) cynku. W każdej zlewce był roztwór innej soli. Roztwory tych soli oznaczono numerami I–IV. W celu identyfikacji zawartości każdej zlewki przeprowadzono dwuetapowe doświadczenie.
Etap 1. Roztwór I wprowadzono do trzech probówek, a następnie do każdej z nich dodano po około 2 cm3 roztworu II, III i IV. Analogicznie postąpiono z pozostałymi roztworami:
– do roztworu II dodano roztwory I, III i IV,
– do roztworu III dodano roztwory I, II i IV,
– do roztworu IV dodano roztwory I, II i III. Wyniki doświadczenia przedstawiono w tabeli.

Etap 2. Niewielkie objętości roztworów I–IV przelano do czterech probówek i zbadano ich odczyn przy użyciu alkoholowego roztworu błękitu bromotymolowego. Poniżej przedstawiono wyniki przeprowadzonego doświadczenia.

Napisz równanie reakcji decydującej o odczynie roztworu IV. Wpisz do schematu wzory odpowiednich drobin. Zastosuj definicję kwasu i zasady Brønsteda.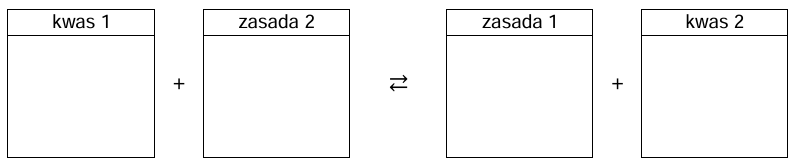
Obliczanie masy płytki po zakończeniu doświadczenia. Zadanie 16.1. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (2 punkty)
Poniższe równanie opisuje reakcję kationów miedzi(II) z metalicznym niklem.
Cu2+(aq) + Ni (s) → Ni2+(aq) + Cu (s)
Ta przemiana może zachodzić w różnych układach, np.:
– w roztworze soli miedzi(II) po zanurzeniu w nim blaszki niklowej,
– w ogniwie złożonym z odpowiednich półogniw metalicznych.
Przygotowano wodny roztwór CuSO4 o stężeniu 0,50 mol∙dm–3 i objętości 20,0 cm3. W tym roztworze zanurzono niklową płytkę o masie 5,820 g. Po pewnym czasie płytkę wyjęto i osuszono. Stwierdzono, że:
– po zakończeniu doświadczenia stężenie jonów Cu2+ w roztworze wynosiło 0,040 mol∙dm–3,
– w warunkach doświadczenia cały wydzielony metal osadził się na płytce.
Oblicz masę płytki po wyjęciu jej z roztworu i osuszeniu. Załóż, że objętość roztworu nie uległa zmianie. W obliczeniach przyjmij następujące wartości mas molowych: MCu = 63,55 g∙mol–1 i MNi = 58,69 g∙mol–1.
Ocena poprawności zdań dotyczących ogniwa chemicznego. Zadanie 16.2. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (1 punkt)
Poniższe równanie opisuje reakcję kationów miedzi(II) z metalicznym niklem.
Cu2+(aq) + Ni (s) → Ni2+(aq) + Cu (s)
Ta przemiana może zachodzić w różnych układach, np.:
– w roztworze soli miedzi(II) po zanurzeniu w nim blaszki niklowej,
– w ogniwie złożonym z odpowiednich półogniw metalicznych.
Skonstruowano ogniwo elektrochemiczne złożone ze standardowego półogniwa miedziowego oraz standardowego półogniwa niklowego. Półogniwa połączono kluczem elektrolitycznym w formie U-rurki wypełnionej nasyconym roztworem azotanu(V) potasu.
Oceń prawdziwość poniższych zdań. Zaznacz P, jeśli zdanie jest prawdziwe, albo F – jeśli jest fałszywe. 1. Siła elektromotoryczna opisanego ogniwa w warunkach standardowych jest równa 0,216 V. 2. W trakcie pracy opisanego ogniwa kationy potasu przemieszczają się z klucza elektrolitycznego w kierunku półogniwa miedziowego, a aniony azotanowe(V) – w kierunku półogniwa niklowego.
Wskazanie z uzasadnieniem półogniwa o wyższym potencjale redukcji. Zadanie 17. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (1 punkt)
Roztwarzanie tlenków wanadu (VO, V2O3, VO2, V2O5) w kwasach nie zawsze prowadzi do powstania prostych kationów wanadu, takich jak V2+ lub V3+, gdyż ten pierwiastek na wyższych stopniach utlenienia tworzy jony oksowanadowe, takie jak VO2+ lub VO2+. Po zmieszaniu roztworu zawierającego kationy VO2+ z roztworem zawierającym kationy V2+ w środowisku kwasowym zachodzi reakcja, którą można opisać równaniem:
VO2+ (aq) + V2+ (aq) + 2H3O+ (aq) → VO2+ (aq) + V3+ (aq) + 3H2O (c)
Na podstawie: C. Blanc, A. Rufer, Paths to Sustainable Energy, Lozanna 2010.
W poniższej tabeli podano równania dwóch reakcji:
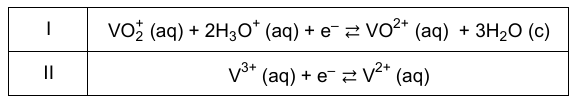
Rozstrzygnij, która reakcja – I czy II – charakteryzuje się wyższą wartością standardowego potencjału redukcji. Odpowiedź uzasadnij. Rozstrzygnięcie: Uzasadnienie:
Zapis nazwy systematycznej węglowodoru na podstawie rysunku modelu jego cząsteczki. Zadanie 18.1. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (1 punkt)
Poniżej przedstawiono model przestrzenny cząsteczki pewnego węglowodoru X.
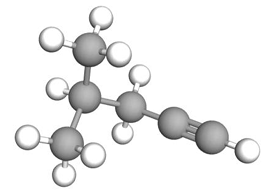
Napisz nazwę systematyczną węglowodoru X.
Wskazanie liczby atomów węgla o hybrydyzacji sp3 oraz liczby wiązań pi w cząsteczce węglowodoru. Zadanie 18.2. Arkusz CKE chemia próbny grudzień 2024 rozszerzony (1 punkt)
Poniżej przedstawiono model przestrzenny cząsteczki pewnego węglowodoru X.

Uzupełnij tabelę. Wpisz liczbę atomów węgla o hybrydyzacji orbitali walencyjnych typu sp3 oraz liczbę wiązań typu 𝝅 w cząsteczce węglowodoru X.

