Zadanie 10.1. Wskazanie numeru alkoholu oraz zapis jego nazwy systematycznej. Doświadczenia chemiczne w zadaniach część 1. Rozdział 5 (1 punkt)
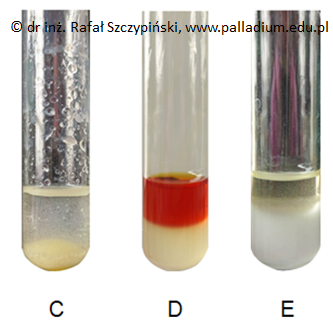
W temperaturze 21 oC próbkę pewnego związku chemicznego poddano działaniu alkalicznego roztworu manganianu(VII) potasu i uzyskano mieszaninę, którą przedstawia zamieszczona fotografia.

Jeden ze związków chemicznych, których wzory 1.–3. wymieniono poniżej nie daje w opisanych warunkach widocznego na fotografii efektu.
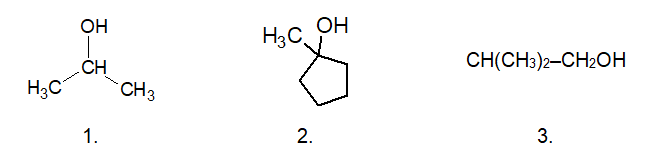
Spośród podanych wzorów wybierz ten, który przedstawia związek chemiczny jaki nie mógł przereagować w opisanych warunkach, a następnie napisz jego nazwę systematyczną. Numer alkoholu: Nazwa systematyczna: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 10.2. Wskazanie przyczyny braku reakcji wybranego alkoholu. Doświadczenia chemiczne w zadaniach część 1. Rozdział 5 (1 punkt)
W temperaturze 21 oC próbkę pewnego związku chemicznego poddano działaniu alkalicznego roztworu manganianu(VII) potasu i uzyskano mieszaninę, którą przedstawia zamieszczona fotografia.

Jeden ze związków chemicznych, których wzory 1.–3. wymieniono poniżej nie daje w opisanych warunkach widocznego na fotografii efektu.

Określ, dlaczego jeden wskazany spośród wymienionych związków chemicznych nie przereagował w opisanych warunkach? Odnieś się do jego rzędowości. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 12.1. Wskazanie właściwego urządzenia pomiarowego oraz zapis nazwy mierzonej wielkości. Doświadczenia chemiczne w zadaniach część 1. Rozdział 5 (1 punkt)
Rysunki poniżej przedstawiają wzory chemiczne kilku substancji o stałym stanie skupienia.
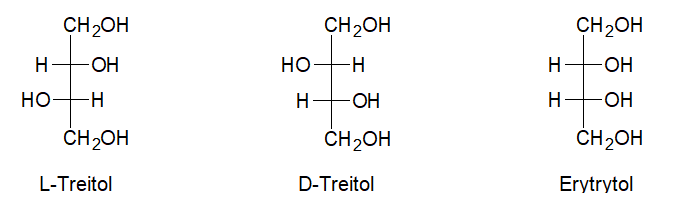
Opisane tetraole mogą zostać odróżnione podczas doświadczenia z wykorzystaniem jednego z urządzeń przedstawionych na fotografiach 1.–3. W tym celu próbkę każdej z wymienionych substancji stanowiącej etanolowy roztwór o takim samym stężeniu poddaje się badaniu, w trakcie którego wykorzystywane są własności optyczne związku chemicznego.

W wyniku przeprowadzonych pomiarów wartości pewnej wielkości fizycznej (α) z wykorzystaniem źródła światła linii D sodu w temperaturze 20 oC uzyskano następujące wyniki (www.sigmaaldrich.com):
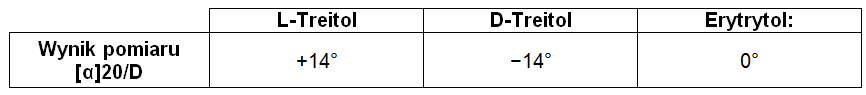
Wskaż numer fotografii przedstawiającej aparaturę wykorzystaną do wykonania pomiarów oraz określ nazwę wielkości fizycznej α, której wartości wyznaczono dla każdej z próbek. Numer fotografii: Nazwa wielkości fizycznej α: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 12.2. Wyjaśnienie przyczyny wartości alfa równej zero w przypadku erytrytolu. Doświadczenia chemiczne w zadaniach część 1. Rozdział 5 (1 punkt)
Rysunki poniżej przedstawiają wzory chemiczne kilku substancji o stałym stanie skupienia.

Opisane tetraole mogą zostać odróżnione podczas doświadczenia z wykorzystaniem jednego z urządzeń przedstawionych na fotografiach 1.–3. W tym celu próbkę każdej z wymienionych substancji stanowiącej etanolowy roztwór o takim samym stężeniu poddaje się badaniu, w trakcie którego wykorzystywane są własności optyczne związku chemicznego.

W wyniku przeprowadzonych pomiarów wartości pewnej wielkości fizycznej (α) z wykorzystaniem źródła światła linii D sodu w temperaturze 20 oC uzyskano następujące wyniki (www.sigmaaldrich.com):

Wyjaśnij, dlaczego w przypadku Erytrytolu wartość α = 0°. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 13. Rysowanie wzorów zidentyfikowanych w danym naczyniu związków chemicznych. Doświadczenia chemiczne w zadaniach część 1. Rozdział 5 (1 punkt)
W celu odróżnienia wodnych roztworów – etanolu oraz fenolu, próbkę każdej z badanych substancji wprowadzono do probówek zawierających wodny roztwór FeCl3. Zamieszczone fotografie ilustrują zawartość probówek po wykonaniu opisanego doświadczenia.

Narysuj wzory grupowe lub uproszczone zidentyfikowanych związków chemicznych przypisując je do odpowiednich probówek. 1.: 2.: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 14. Wskazanie emulsji oraz roztworu rzeczywistego z uzasadnieniem. Doświadczenia chemiczne w zadaniach część 1. Rozdział 5 (2 punkty)
W probówce umieszczono próbkę tymolu:
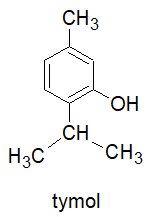
do której wprowadzono wodę destylowaną (22 oC) i energicznie wstrząśnięto zawartością naczynia (fotografia 1.). Następnie przeprowadzono doświadczenie chemiczne według poniższego schematu.

Po dodaniu stałego wodorotlenku potasu probówką energicznie wstrząśnięto uzyskując mieszaninę przedstawioną na 3. fotografii. Podczas chłodzenia powstałego roztworu do wyjściowej temperatury nie zaobserwowano żadnych zmian.
Wskaż numer tej probówki, której zawartość stanowi emulsję oraz numer probówki zawierającej roztwór rzeczywisty. Uzasadnij swój wybór. Emulsja: Uzasadnienie: Roztwór rzeczywisty: Uzasadnienie: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 15. Rysowanie wzoru produktu reakcji. Doświadczenia chemiczne w zadaniach część 1. Rozdział 5 (1 punkt)
W probówce umieszczono próbkę tymolu:

do której wprowadzono wodę destylowaną (22 oC) i energicznie wstrząśnięto zawartością naczynia (fotografia 1.). Następnie przeprowadzono doświadczenie chemiczne według poniższego schematu.

Po dodaniu stałego wodorotlenku potasu probówką energicznie wstrząśnięto uzyskując mieszaninę przedstawioną na 3. fotografii. Podczas chłodzenia powstałego roztworu do wyjściowej temperatury nie zaobserwowano żadnych zmian.
Narysuj wzór grupowy związku chemicznego powstałego w 3. probówce. Określ rodzaj kryształów (kowalencyjne, molekularne, jonowe) w postaci których substancja ta występuje w warunkach normalnych. Uzupełnij tabelę. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 16.1. Rysowanie wzoru grupowego związku nadającego zabarwienie. Doświadczenia chemiczne w zadaniach część 1. Rozdział 5 (1 punkt)
W probówce umieszczono próbkę tymolu:

do której wprowadzono wodę destylowaną (22 oC) i energicznie wstrząśnięto zawartością naczynia (fotografia 1.). Następnie przeprowadzono doświadczenie chemiczne według poniższego schematu.

Po dodaniu stałego wodorotlenku potasu probówką energicznie wstrząśnięto uzyskując mieszaninę przedstawioną na 3. fotografii. Podczas chłodzenia powstałego roztworu do wyjściowej temperatury nie zaobserwowano żadnych zmian.
Fenole ulegają nitrowaniu bez udziału katalizatora. Powstałe nitropochodne mają inne zabarwienie, niż wyjściowy substrat organiczny. Opisana cecha odnosi się również do barw roztworów związków organicznych, która zależy od rodzaju obecnych w cząsteczkach substancji rozpuszczonej ugrupowań atomów oraz od związku chemicznego stanowiącego rozpuszczalnik. Na fotografii A przedstawiono benzenowy roztwór tymolu o temperaturze 22 oC. Fotografia B w tych samych warunkach ilustruje wodną zawiesinę pochodnej tymolu o nazwie 5-metylo-4-nitro-2-(propan-2-ylo)fenol.

Narysuj wzór grupowy związku chemicznego, którego obecność w probówce B nadaje jej zawartości widoczne zabarwienie. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 17.1. Zapis równań reakcji chemicznych. Doświadczenia chemiczne w zadaniach część 1. Rozdział 5 (2 punkty)
W dwóch niepodpisanych butelkach znajdowały się acetaldehyd oraz propanon. W celu identyfikacji zawartości naczyń, próbki badanych substancji wprowadzono do probówek zawierających alkaliczne zawiesiny wodorotlenku miedzi(II) i energicznie wstrząśnięto. W każdym z naczyń uzyskano zawartość widoczną na fotografii 1. Następnie każdą z probówek ogrzano, co doprowadziło do zmian, jakie przedstawiają fotografie 2. oraz 3.

Napisz w formie jonowej skróconej, stosując wzory grupowe odpowiednich drobin równania reakcji chemicznych, których przebieg doprowadził do powstania zawartości przedstawionych na 2. oraz 3. fotografii. Fotografia 2.: Fotografia 3.: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 17.2. Wskazanie właściwej probówki. Doświadczenia chemiczne w zadaniach część 1. Rozdział 5 (1 punkt)
W dwóch niepodpisanych butelkach znajdowały się acetaldehyd oraz propanon. W celu identyfikacji zawartości naczyń, próbki badanych substancji wprowadzono do probówek zawierających alkaliczne zawiesiny wodorotlenku miedzi(II) i energicznie wstrząśnięto. W każdym z naczyń uzyskano zawartość widoczną na fotografii 1. Następnie każdą z probówek ogrzano, co doprowadziło do zmian, jakie przedstawiają fotografie 2. oraz 3.

Wskaż numer tej probówki, w której nastąpiła zmiana wartości stopni utlenienia atomów podczas opisanego doświadczenia. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zadanie 18. Ocena, czy uzyskano pozytywny wynik próby Tollensa. Doświadczenia chemiczne w zadaniach część 1. Rozdział 5 (1 punkt)
Wodne roztwory stosunkowo dobrze rozpuszczalnych w wodzie aldehydów można odróżnić od wielu innych substancji chemicznych przeprowadzając próbę Tollensa.
Poniższy rysunek ilustruje wzór cząsteczki 4-metoksybenzaldehydu (aldehydu anyżowego). Na fotografii A przedstawiono zachowanie się tego związku chemicznego wobec wody destylowanej, natomiast fotografia B obrazuje wynik próby Tollensa z jego udziałem.
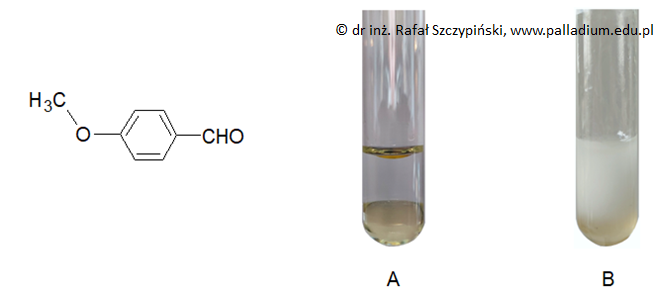
Oceń, czy uzyskano pozytywny wynik przeprowadzonej z udziałem aldehydu anyżowego próby Tollensa. Odpowiedź uzasadnij odnosząc się do wyglądu zawartości naczynia. Ocena: Uzasadnienie: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone