Rysowanie wzoru elektronowego cząsteczki ditlenku triwęgla oraz wskazanie liczby wiązań sigma oraz atomów węgla o hybrydyzacji sp. Zadanie 5. Arkusz CKE chemia maj 2023 rozszerzony formuła 2015 (2 punkty)
Ze względu na zdolność atomów węgla do łączenia się w łańcuchy ten pierwiastek tworzy z tlenem nie tylko związki takie jak CO i CO2, lecz także mniej typowe połączenia. Jednym z nich jest ditlenek triwęgla o wzorze sumarycznym C3O2. Cząsteczka tego związku ma budowę liniową, atomami wewnętrznymi są w niej atomy węgla, a skrajnymi – atomy tlenu. Ditlenek triwęgla reaguje z wodą. W tej reakcji powstaje jeden produkt – kwas dikarboksylowy.
Na podstawie: J.E. House, Inorganic Chemistry, Elsevier, 2008.
Narysuj wzór elektronowy cząsteczki C3O2 (zaznacz kreskami wiązania chemiczne i wolne pary elektronowe). Uzupełnij poniższe zdania. Wybierz i zaznacz jedną odpowiedź spośród podanych w każdym nawiasie. Wzór elektronowy: Aby wyjaśnić budowę cząsteczki C3O2, hybrydyzację typu sp przypisuje się orbitalom walencyjnym (trzech atomów / dwóch atomów / jednego atomu) węgla. Liczba wiązań sigma w cząsteczce C3O2 wynosi (2 / 4 / 6 / 8).
Rysowanie wzoru półstrukturalnego produktu reakcji ditlenku triwęgla z wodą. Zadanie 6. Arkusz CKE chemia maj 2023 rozszerzony formuła 2015 (1 punkt)
Ze względu na zdolność atomów węgla do łączenia się w łańcuchy ten pierwiastek tworzy z tlenem nie tylko związki takie jak CO i CO2, lecz także mniej typowe połączenia. Jednym z nich jest ditlenek triwęgla o wzorze sumarycznym C3O2. Cząsteczka tego związku ma budowę liniową, atomami wewnętrznymi są w niej atomy węgla, a skrajnymi – atomy tlenu. Ditlenek triwęgla reaguje z wodą. W tej reakcji powstaje jeden produkt – kwas dikarboksylowy.
Na podstawie: J.E. House, Inorganic Chemistry, Elsevier, 2008.
Narysuj wzór półstrukturalny (grupowy) produktu reakcji ditlenku triwęgla z wodą.
Wybór bardziej lotnego związku z wyjaśnieniem. Zadanie 7. Arkusz CKE chemia maj 2023 rozszerzony formuła 2015 (1 punkt)
W poniższej tabeli podano wzory dwóch związków organicznych: alkoholu benzylowego i etylobenzenu, a także wartości masy molowej oraz temperatury wrzenia tych związków.

Na podstawie: T. Mizerski, Tablice chemiczne, Warszawa 2013.
Rozstrzygnij, który związek – alkohol benzylowy czy etylobenzen – jest substancją bardziej lotną. Wyjaśnij, dlaczego alkohol benzylowy i etylobenzen znacznie różnią się wartościami temperatury wrzenia. Odnieś się do wpływu różnicy w budowie cząsteczek obu związków na ich właściwości fizykochemiczne. Rozstrzygnięcie: Wyjaśnienie:
Obliczanie stałej równowagi reakcji syntezy BrCl. Zadanie 8. Arkusz CKE chemia maj 2023 rozszerzony formuła 2015 (1 punkt)
Reakcja rozkładu chlorku bromu(I) przebiega w fazie gazowej zgodnie z równaniem:
2BrCl (g) ⇄ Br2 (g) + Cl2 (g)
Wartość stężeniowej stałej równowagi reakcji rozkładu chlorku bromu(I) w temperaturze 500 K jest równa 32.
Na podstawie: L. Jones, P. Atkins, Chemia ogólna, Warszawa 2009.
Reakcja syntezy chlorku bromu(I) przebiega w fazie gazowej zgodnie z równaniem:
Br2 (g) + Cl2 (g) ⇄ 2BrCl (g)
Oblicz wartość stężeniowej stałej równowagi reakcji syntezy chlorku bromu(I) w temperaturze 𝟓𝟎𝟎 𝐊.
Wybór mocniejszego kwasu z uzasadnieniem wyboru. Zadanie 9. Arkusz CKE chemia maj 2023 rozszerzony formuła 2015 (1 punkt)
W wodnych roztworach słabych kwasów jednoprotonowych zachodzi dysocjacja. Dla danej wartości stężenia molowego roztworu i w danej temperaturze ustala się stan równowagi między cząsteczkami i jonami obecnymi w roztworze. Na poniższym wykresie przedstawiono zależność stopnia dysocjacji (a) dwóch kwasów jednoprotonowych HX i HQ od stężenia molowego roztworu w temperaturze 20 °C.
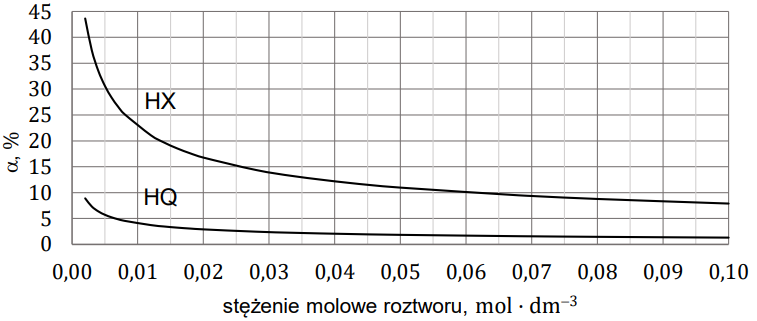
Wartości stopnia dysocjacji kwasu HX dla wybranych stężeń molowych (𝑐0) zebrano w tabeli (𝑡 = 20 °C).
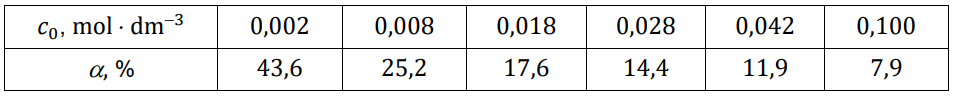
Rozstrzygnij, na podstawie analizy danych zamieszczonych na wykresie, który kwas (HX czy HQ) jest mocniejszy. Zaznacz jego wzór. Odpowiedź uzasadnij. HX HQ Uzasadnienie:
Wybór odczynników oraz jonowy zapis równań reakcji chemicznych. Zadanie 10.1. Arkusz CKE chemia maj 2023 rozszerzony formuła 2015 (3 punkty)
Sole można otrzymać m.in. w reakcjach:
1. soli kwasu I z kwasem II mocniejszym od kwasu I
2. wodorotlenku z tlenkiem kwasowym.
Uzupełnij schemat doświadczenia, w którym można otrzymać: KOH (aq) HCl (aq) C6H5OH Ba(OH)2 (aq) Na2CO3 (aq) (NH4)3PO4 (aq) Następnie napisz w formie jonowej równania reakcji, które zaszły w kolbie oraz w probówce podczas tego doświadczenia. Równanie reakcji zachodzącej w kolbie: Równanie reakcji zachodzącej w probówce:
– w kolbie rozpuszczalną w wodzie sól metodą 1.
– w probówce nierozpuszczalną sól metodą 2.
Wzory użytych odczynników wybierz spośród następujących: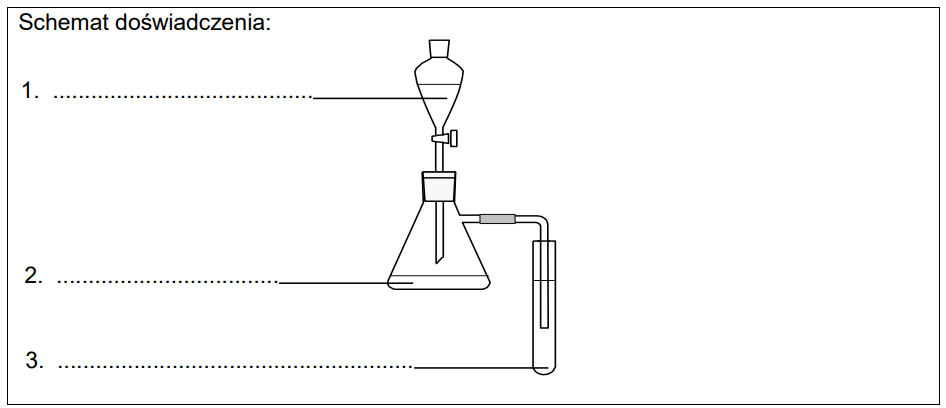
Wybór odpowiedniej czynności. Zadanie 10.2. Arkusz CKE chemia maj 2023 rozszerzony formuła 2015 (1 punkt)
Sole można otrzymać m.in. w reakcjach:
1. soli kwasu I z kwasem II mocniejszym od kwasu I
2. wodorotlenku z tlenkiem kwasowym.
Podczas opisanego doświadczenia dodano z wkraplacza do kolby stechiometryczną ilość reagenta.
Spośród czynności, których nazwy podano poniżej, wybierz tę, którą należy wykonać w celu wyodrębnienia jonowego produktu reakcji z mieszaniny poreakcyjnej, powstałej w kolbie. Zaznacz jej nazwę. odparowanie pod wyciągiem odwirowanie sączenie
Wybór par drobin które nie tworzą sprzężonej pary kwas-zasada Brønsteda. Zadanie 11. Arkusz CKE chemia maj 2023 rozszerzony formuła 2015 (1 punkt)
Spośród wymienionych par drobin wybierz i zaznacz wszystkie te, które nie tworzą sprzężonej pary Brønsteda kwas – zasada.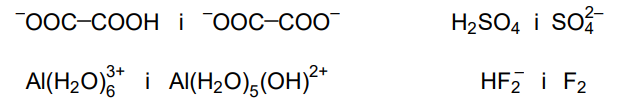
Zapis równania procesu zgodnie z teorią Brønsteda i wskazaniem sprzężonych par kwasów oraz zasad. Zadanie 12.1. Arkusz CKE chemia maj 2023 rozszerzony formuła 2015 (1 punkt)
Przeprowadzono doświadczenie, w którym do dwóch probówek z wodnym roztworem Na2SO3 dodano:
– do probówki 1. – kilka kropel roztworu fenoloftaleiny
– do probówki 2. – nadmiar stężonego HCl (aq).
Zawartość probówki 1., po dodaniu do niej roztworu fenoloftaleiny, zabarwiła się na kolor czerwonoróżowy (malinowy).
Wpisz do schematu wzory odpowiednich drobin tak, aby powstało równanie procesu decydującego o odczynie roztworu w probówce 1. Zastosuj definicję kwasu i zasady Brønsteda.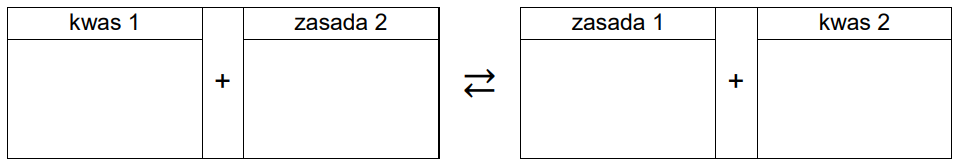
Zapis obserwacji oraz równania reakcji chemicznej w formie jonowej skróconej. Zadanie 12.2. Arkusz CKE chemia maj 2023 rozszerzony formuła 2015 (1 punkt)
Przeprowadzono doświadczenie, w którym do dwóch probówek z wodnym roztworem Na2SO3 dodano:
– do probówki 1. – kilka kropel roztworu fenoloftaleiny
– do probówki 2. – nadmiar stężonego HCl (aq).
Napisz, co zaobserwowano podczas doświadczenia w probówce 2. po dodaniu odczynnika. Napisz w formie jonowej skróconej równanie reakcji, która była przyczyną zaobserwowanych zmian. Obserwacje: Równanie reakcji:
Rozstrzygnięcie czy miareczkowany kwas jest mocny czy słaby z dwoma uzasadnieniami. Zadanie 13. Arkusz CKE chemia maj 2023 rozszerzony formuła 2015 (2 punkty)
Badano reakcje mocnego kwasu HA i słabego kwasu HX z mocną zasadą. W tym celu wykonano miareczkowanie wodnych roztworów tych kwasów za pomocą wodnego roztworu wodorotlenku potasu – zgodnie z poniższym opisem. Umieszczono w zlewce 20,0 cm3 roztworu wybranego kwasu o stężeniu 0,10 mol ∙ dm−3 i zmierzono pH tego roztworu. Następnie do zlewki z roztworem kwasu dodawano porcjami wodny roztwór KOH o stężeniu 0,10 mol ∙ dm−3 . Po dodaniu każdej porcji roztworu wodorotlenku mierzono pH mieszaniny reakcyjnej. Punkt równoważnikowy (PR) został osiągnięty po dodaniu takiej objętości roztworu KOH, w jakiej liczba moli zasady jest równa liczbie moli kwasu. Uzyskane wyniki przedstawiono w formie wykresu zależności mierzonego pH od objętości roztworu KOH – naniesione punkty połączono, w wyniku czego otrzymano krzywą miareczkowania. Poniżej przedstawiono krzywą miareczkowania wodnego roztworu jednego z tych kwasów (HA albo HX) wodnym roztworem wodorotlenku potasu.
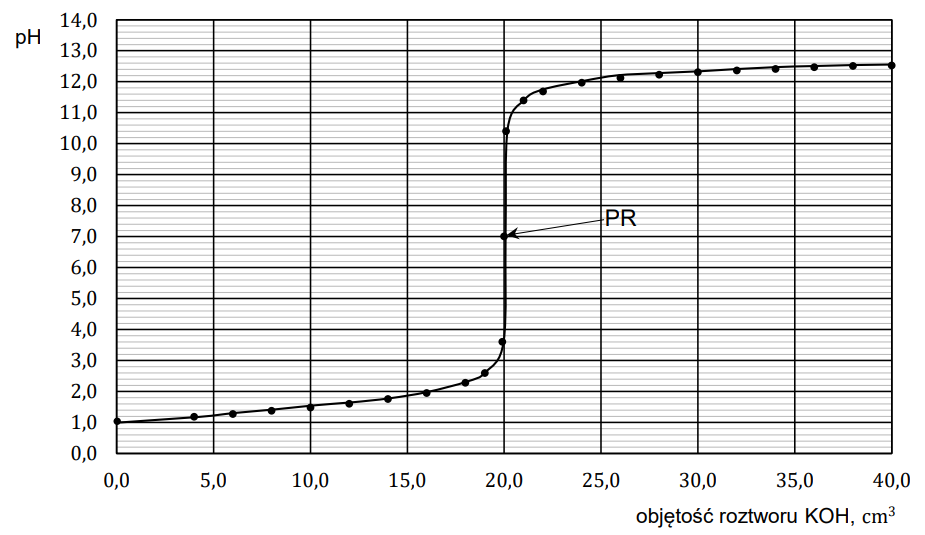
Rozstrzygnij, czy przedstawiony wykres ilustruje wyniki miareczkowania wodnego roztworu słabego kwasu HX wodnym roztworem KOH w opisanym doświadczeniu. Odpowiedź uzasadnij – przytocz dwa różne argumenty. Uzasadnienie: 1. 2.
Obliczanie wartości pH nasyconego roztworu wody amoniakalnej. Zadanie 14. Arkusz CKE chemia maj 2023 rozszerzony formuła 2015 (2 punkty)
W temperaturze 25 °C rozpuszczalność amoniaku w wodzie jest równa 46 g w 100 g wody.
Na podstawie: K. H. Lautenschläger i in., Nowoczesne kompendium chemii, Warszawa 2007.
Oblicz pH wodnego roztworu amoniaku nasyconego w tej temperaturze, jeżeli jego gęstość jest równa 0,91 g∙cm–𝟑 . Wynik końcowy zaokrąglij do pierwszego miejsca po przecinku.
Określanie odczynu wodnych roztworów soli. Zadanie 15. Arkusz CKE chemia maj 2023 rozszerzony formuła 2015 (1 punkt)
Wymieszano po dwa wodne roztwory różnych soli o stężeniu ok. 0,5 mol ∙ dm−3 . W ten sposób otrzymano roztwory A i B, których skład podany jest w poniższej tabeli.

Określ odczyn roztworów A i B. Odczyn roztworu A: Odczyn roztworu B:
Wybór właściwych wyrazów w nawiasach. Zadanie 16. Arkusz CKE chemia maj 2023 rozszerzony formuła 2015 (1 punkt)
Przygotowano wodne roztwory następujących substancji:
1. kwasu azotowego(V) o stężeniu 0,5 mol ∙ dm−3
2. kwasu octowego (etanowego) o stężeniu 0,5 mol ∙ dm−3
3. wodorotlenku baru o pH = 11 4. wodorotlenku potasu o pH = 11.
Uzupełnij poniższe zdania. Wybierz i zaznacz jedną odpowiedź spośród podanych w każdym nawiasie. Wartość pH roztworu kwasu azotowego(V) jest (większa niż / mniejsza niż / taka sama jak) wartość pH roztworu kwasu octowego. Spośród roztworów o odczynie zasadowym mniejsze stężenie molowe ma roztwór numer (3 / 4).
Zapis równań przebiegających reakcji chemicznych w dwuetapowym procesie. Zadanie 17.1. Arkusz CKE chemia maj 2023 rozszerzony formuła 2015 (1 punkt)
Czysty tlenek wapnia można otrzymać w laboratorium w wyniku prażenia szczawianu wapnia o wzorze CaC2O4. Podczas ogrzewania szczawian wapnia najpierw rozkłada się na węglan wapnia i tlenek węgla(II) (reakcja 1.). Dalsze ogrzewanie, w wyższej temperaturze, prowadzi do rozkładu węglanu wapnia na tlenek wapnia i tlenek węgla(IV) (reakcja 2.). Tlenek wapnia jest ciałem stałym o temperaturze topnienia równej 2858 K. Energicznie reaguje z wodą, a przemianie tej towarzyszy wydzielanie się znacznej ilości ciepła.
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2010.
Napisz równanie reakcji, która zachodzi w pierwszym etapie rozkładu termicznego szczawianu wapnia (reakcja 1.), i równanie reakcji, która zachodzi w drugim etapie tego procesu (reakcja 2.). Równanie reakcji 1.: Równanie reakcji 2.:

