Identyfikacja roztworów soli na podstawie ich zachowania się wobec wody chlorowej. Zadanie 17.1. Arkusz CKE chemia maj 2021 rozszerzony (1 punkt)
W dwóch probówkach znajdowały się wodne roztwory soli X i Z, otrzymane przez rozpuszczenie stałych soli, z których jedną był siarczek potasu, a drugą – bromek potasu. Przeprowadzono doświadczenie zgodnie z poniższym schematem. W doświadczeniu użyto świeżo otrzymanej wody chlorowej.
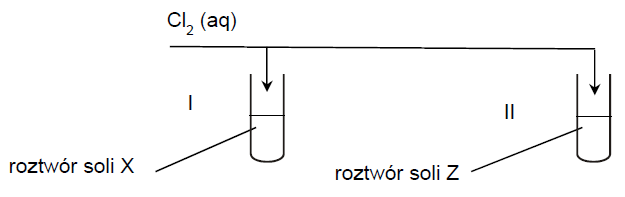
Po dodaniu wody chlorowej do probówek zauważono, że w probówce I roztwór zmienił barwę, ale pozostał klarowny, natomiast w probówce II pojawiło się zmętnienie.
Zidentyfikuj sole X i Z i wpisz ich wzory do tabeli.
Zapis równania reakcji pomiędzy chlorem a bromkiem potasu oraz pomiędzy chlorem a siarczkiem potasu. Zadanie 17.2. Arkusz CKE chemia maj 2021 rozszerzony (1 punkt)
W dwóch probówkach znajdowały się wodne roztwory soli X i Z, otrzymane przez rozpuszczenie stałych soli, z których jedną był siarczek potasu, a drugą – bromek potasu. Przeprowadzono doświadczenie zgodnie z poniższym schematem. W doświadczeniu użyto świeżo otrzymanej wody chlorowej.

Po dodaniu wody chlorowej do probówek zauważono, że w probówce I roztwór zmienił barwę, ale pozostał klarowny, natomiast w probówce II pojawiło się zmętnienie.
Napisz w formie jonowej skróconej równania reakcji pomiędzy chlorem a bromkiem potasu oraz pomiędzy chlorem a siarczkiem potasu.
Wybór właściwego związku chemicznego, którego roztwór użyto do wykonania doświadczenia. Zadanie 18.1. Arkusz CKE chemia maj 2021 rozszerzony (1 punkt)
W kolbach oznaczonych numerami I i II znajdowały się dwa różne klarowne roztwory o żółtej barwie. Każdy z roztworów otrzymano przez rozpuszczenie w wodzie jednej substancji wybranej spośród:
FeCl3 K2CrO4 KMnO4 MnSO4 (NH4)2CrO4 (NH4)2Cr2O7
Do roztworu w kolbie I dodano wodny roztwór wodorotlenku sodu i zaobserwowano wydzielanie się bezbarwnego gazu o charakterystycznym zapachu. Stwierdzono także, że w mieszaninie nie wytrącił się żaden osad i że roztwór pozostał żółty.
Do roztworu w kolbie II dodano wodny roztwór kwasu siarkowego(VI) i stwierdzono, że roztwór pozostał klarowny, ale zmienił barwę z żółtej na pomarańczową. Kiedy do uzyskanej mieszaniny dodano nadmiar wodnego roztworu wodorotlenku sodu, roztwór z powrotem stał się żółty i nie zaobserwowano wydzielania gazu.
Spośród wymienionych powyżej związków chemicznych wybierz i napisz wzór związku, którego roztwór znajdował się w kolbie I na początku doświadczenia.
Zapis równań reakcji chemicznych przebiegających po dodaniu roztworu kwasu siarkowego(VI) i nadmiaru roztworu zasady sodowej. Zadanie 18.2. Arkusz CKE chemia maj 2021 rozszerzony (2 punkty)
W kolbach oznaczonych numerami I i II znajdowały się dwa różne klarowne roztwory o żółtej barwie. Każdy z roztworów otrzymano przez rozpuszczenie w wodzie jednej substancji wybranej spośród:
FeCl3 K2CrO4 KMnO4 MnSO4 (NH4)2CrO4 (NH4)2Cr2O7
Do roztworu w kolbie I dodano wodny roztwór wodorotlenku sodu i zaobserwowano wydzielanie się bezbarwnego gazu o charakterystycznym zapachu. Stwierdzono także, że w mieszaninie nie wytrącił się żaden osad i że roztwór pozostał żółty.
Do roztworu w kolbie II dodano wodny roztwór kwasu siarkowego(VI) i stwierdzono, że roztwór pozostał klarowny, ale zmienił barwę z żółtej na pomarańczową. Kiedy do uzyskanej mieszaniny dodano nadmiar wodnego roztworu wodorotlenku sodu, roztwór z powrotem stał się żółty i nie zaobserwowano wydzielania gazu.
Napisz w formie jonowej skróconej równanie reakcji, która zaszła w kolbie II: • po dodaniu wodnego roztworu H2SO4 do zawartości kolby: • po dodaniu nadmiaru wodnego roztworu NaOH:
Zapis równania reakcji przebiegającej między antymonem i stężonym kwasem siarkowym(VI) z zastosowaniem bilansu jonowo-elektronowego. Zadanie 19.1. Arkusz CKE chemia maj 2021 rozszerzony (2 punkty)
Antymon roztwarza się na gorąco w stężonym kwasie siarkowym(VI). W tej przemianie tworzy się m.in. zdysocjowany w wodnym roztworze siarczan(VI) antymonu(III) oraz wydziela się bezbarwny gaz o charakterystycznym ostrym zapachu, w którym siarka stanowi 50% masowych.
Antymon reaguje także na gorąco ze stężonym kwasem azotowym(V). W tej przemianie wydziela się bezbarwny gaz, który w kontakcie z powietrzem zabarwia się na kolor czerwonobrunatny, i powstaje trudno rozpuszczalny jednoprotonowy kwas antymonowy(V). W cząsteczce tego kwasu stosunek liczby atomów wodoru do liczby atomów tlenu jest równy 1 : 3.
Na podstawie: J. Minczewski, Z. Marczenko, Chemia analityczna, Warszawa 2004.
Napisz w formie jonowej z uwzględnieniem liczby oddawanych lub pobieranych elektronów (zapis jonowo-elektronowy) równania reakcji redukcji i utleniania zachodzących podczas opisanego procesu roztwarzania antymonu na gorąco w stężonym kwasie siarkowym(VI). Napisz w formie cząsteczkowej sumaryczne równanie opisanej przemiany. Równanie reakcji redukcji: Równanie reakcji utleniania: Sumaryczne równanie reakcji:
Zapis równania reakcji roztwarzania antymonu w stężonym kwasie azotowym(V). Zadanie 19.2. Arkusz CKE chemia maj 2021 rozszerzony (1 punkt)
Antymon roztwarza się na gorąco w stężonym kwasie siarkowym(VI). W tej przemianie tworzy się m.in. zdysocjowany w wodnym roztworze siarczan(VI) antymonu(III) oraz wydziela się bezbarwny gaz o charakterystycznym ostrym zapachu, w którym siarka stanowi 50% masowych.
Antymon reaguje także na gorąco ze stężonym kwasem azotowym(V). W tej przemianie wydziela się bezbarwny gaz, który w kontakcie z powietrzem zabarwia się na kolor czerwonobrunatny, i powstaje trudno rozpuszczalny jednoprotonowy kwas antymonowy(V). W cząsteczce tego kwasu stosunek liczby atomów wodoru do liczby atomów tlenu jest równy 1 : 3.
Na podstawie: J. Minczewski, Z. Marczenko, Chemia analityczna, Warszawa 2004.
Napisz w formie jonowej sumaryczne równanie opisanego procesu roztwarzania antymonu na gorąco w stężonym kwasie azotowym(V).
Wybór poprawnych określeń dotyczących rozpuszczalności dwóch soli oraz stężeń ich roztworów. Zadanie 20. Arkusz CKE chemia maj 2021 rozszerzony (1 punkt)
Na wykresie przedstawiono zależność rozpuszczalności w wodzie dwóch soli – K2CrO4 i Pb(NO3)2 – od temperatury.
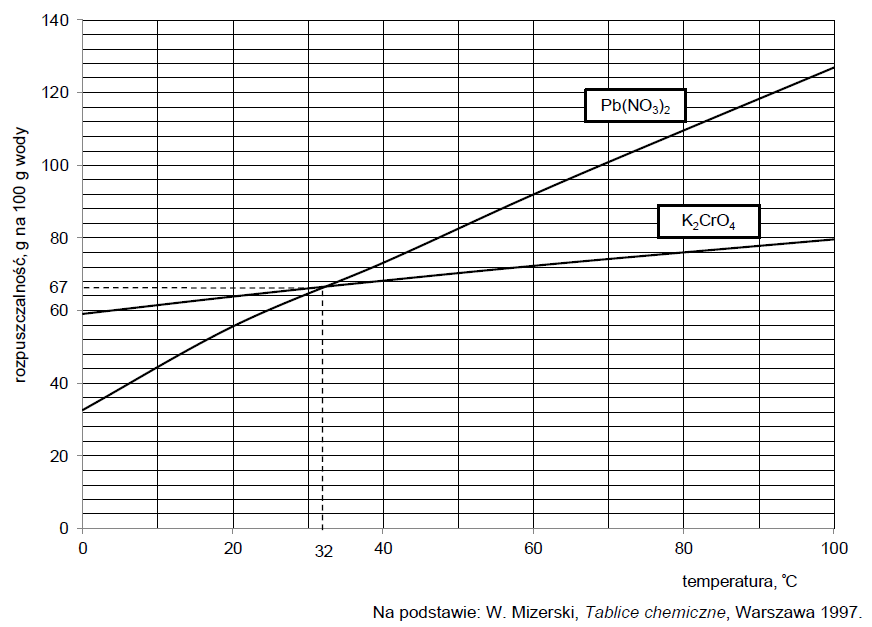
Przeprowadzono doświadczenie zilustrowane na poniższym schemacie.
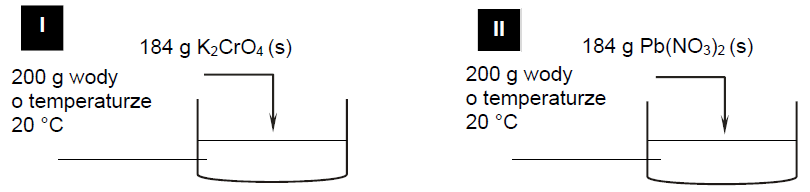
Następnie zawartość zlewek ogrzano do temperatury 𝑡, w której w zlewce II cały azotan(V) ołowiu(II) uległ rozpuszczeniu, a otrzymany roztwór był nasycony.
Napisz wartość temperatury 𝒕, a następnie uzupełnij poniższe zdanie dotyczące mieszanin otrzymanych w obu zlewkach po ogrzaniu ich zawartości do temperatury 𝒕. Wybierz i podkreśl jedną odpowiedź spośród podanych w każdym nawiasie. 𝑡 = Roztwór w zlewce I jest (nienasycony / nasycony), a jego stężenie wyrażone w procentach masowych jest (mniejsze niż / takie samo jak / większe niż) stężenie roztworu wyrażone w procentach masowych w zlewce II.
Obliczanie masy osadu na podstawie znajomości rozpuszczalności reagujących ze sobą soli. Zadanie 21. Arkusz CKE chemia maj 2021 rozszerzony (2 punkty)
Na wykresie przedstawiono zależność rozpuszczalności w wodzie dwóch soli – K2CrO4 i Pb(NO3)2 – od temperatury.

Do 100 gramów nasyconego roztworu azotanu(V) ołowiu(II) o temperaturze 32 °C dodano 100 gramów nasyconego roztworu chromianu(VI) potasu o temperaturze 32 °C. W wyniku przemiany zilustrowanej poniższym równaniem wytrącił się osad.
Pb2+ + CrO42– → PbCrO4
Oblicz masę otrzymanego osadu. Wskaż substancję użytą w nadmiarze – podaj jej wzór lub nazwę. Przyjmij, że opisana przemiana przebiegła z wydajnością równą 100%. Masy molowe są równe: M K2CrO4 = 194 g∙mol–1, M Pb(NO3)2 = 331 g∙mol–1, M PbCrO4 = 323 g∙mol–1. Masa osadu: W nadmiarze użyto:
Wybór poprawnych określeń dotyczących doświadczenia z użyciem miedzi i kwasu azotowego(V) oraz siarkowego(VI). Obliczanie masy osadu na podstawie znajomości rozpuszczalności reagujących ze sobą soli. Zadanie 22. Arkusz CKE chemia maj 2021 rozszerzony (2 punkty)
W dwóch nieoznaczonych probówkach znajdowały się oddzielnie: rozcieńczony wodny roztwór kwasu azotowego(V) i rozcieńczony wodny roztwór kwasu siarkowego(VI). W tych roztworach zanurzono blaszki miedziane, a zawartość probówek lekko ogrzano.
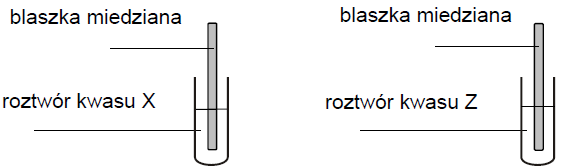
Po zanurzeniu blaszki miedzianej w roztworze kwasu X i ogrzaniu zawartości probówki wydzielał się bezbarwny gaz, który w kontakcie z powietrzem zabarwiał się na kolor czerwonobrunatny.
Uzupełnij poniższe zdania. Wybierz i podkreśl jedną odpowiedź spośród podanych w każdym nawiasie. W rozcieńczonym roztworze kwasu azotowego(V) miedź (reaguje z wydzieleniem gazowego tlenku / reaguje z wydzieleniem wodoru / nie reaguje) i roztwór (przyjmuje barwę niebieską / pozostaje bezbarwny). W rozcieńczonym roztworze kwasu siarkowego(VI) miedź (reaguje z wydzieleniem gazowego tlenku / reaguje z wydzieleniem wodoru / nie reaguje) i roztwór (przyjmuje barwę niebieską / pozostaje bezbarwny). Kwasem X jest (HNO3 / H2SO4).
Zapis wzoru półstrukturalnego oraz nazwy systematycznej jodku alkilu użytego w reakcji Wurtza. Zadanie 23. Arkusz CKE chemia maj 2021 rozszerzony (1 punkt)
Alkany można otrzymać z halogenków alkilów o ogólnym wzorze R–X, w którym R oznacza grupę alkilową, a X – atom halogenu (chloru, bromu lub jodu). Halogenki alkilów reagują z sodem zgodnie z poniższym schematem:
![]()
Reakcję przeprowadza się w środowisku bezwodnym w podwyższonej temperaturze. Jeżeli do reakcji zastosuje się jeden halogenek alkilu, R–X, otrzymuje się jeden alkan, a przy zastosowaniu różnych halogenków alkilów, np. R1–X i R2–X, powstaje mieszanina alkanów.
Na podstawie: R.T. Morrison, R.N. Boyd, Chemia organiczna, Warszawa 2008.
Pewien jodek alkilu poddano działaniu sodu i otrzymano alkan o wzorze:
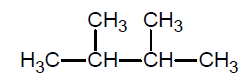
Napisz wzór półstrukturalny (grupowy) i nazwę systematyczną jodku alkilu, który poddano działaniu sodu w opisanej reakcji. Wzór półstrukturalny (grupowy): Nazwa systematyczna:
Ocena poprawności zdań dotyczących reakcji Wurtza. Zadanie 24. Arkusz CKE chemia maj 2021 rozszerzony (1 punkt)
Alkany można otrzymać z halogenków alkilów o ogólnym wzorze R–X, w którym R oznacza grupę alkilową, a X – atom halogenu (chloru, bromu lub jodu). Halogenki alkilów reagują z sodem zgodnie z poniższym schematem:
![]()
Reakcję przeprowadza się w środowisku bezwodnym w podwyższonej temperaturze. Jeżeli do reakcji zastosuje się jeden halogenek alkilu, R–X, otrzymuje się jeden alkan, a przy zastosowaniu różnych halogenków alkilów, np. R1–X i R2–X, powstaje mieszanina alkanów.
Na podstawie: R.T. Morrison, R.N. Boyd, Chemia organiczna, Warszawa 2008.
Mieszaninę 2-jodobutanu i jodku metylu poddano działaniu sodu i otrzymano różne alkany.
Oceń prawdziwość poniższych zdań. Zaznacz P, jeżeli zdanie jest prawdziwe, albo F – jeśli jest fałszywe. 1. W opisanej reakcji otrzymano cztery różne alkany. 2. Otrzymanym w opisanej reakcji alkanem o najmniejszej masie cząsteczkowej był metan. 3. Alkanem o największej masie cząsteczkowej – otrzymanym w opisanej reakcji – był 3,4-dimetyloheksan.
Uzupełnienie ciągu przemian z udziałem 2-jodobutanu oraz powstałego z niego alkoholu. Zadanie 25.1. Arkusz CKE chemia maj 2021 rozszerzony (1 punkt)
W wyniku zasadowej hydrolizy 2-jodobutanu otrzymano alkohol, który następnie utleniono tlenkiem miedzi(II).
Uzupełnij schemat opisanych przemian. Wpisz wzory półstrukturalne (grupowe): 2-jodobutanu, alkoholu otrzymanego w wyniku zasadowej hydrolizy 2-jodobutanu i organicznego produktu utlenienia tlenkiem miedzi(II) tego alkoholu.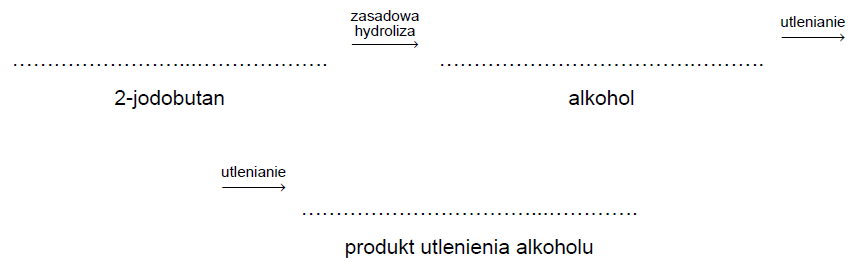
Wybór poprawnych określeń dotyczących reakcji jodku alkilu. Zadanie 25.2. Arkusz CKE chemia maj 2021 rozszerzony (1 punkt)
W wyniku zasadowej hydrolizy 2-jodobutanu otrzymano alkohol, który następnie utleniono tlenkiem miedzi(II).
Uzupełnij poniższe zdania. Wybierz i podkreśl jedną odpowiedź spośród podanych w każdym nawiasie. Hydroliza zasadowa jodku alkilu jest reakcją (addycji / substytucji / eliminacji) zachodzącą zgodnie z mechanizmem nukleofilowym. Przykładem obojętnego elektrycznie nukleofilu jest cząsteczka (CH4 / H2 / NH3), a nukleofilu jonowego – jon (CN– / Cu2+ / H3O+).
Zapis wzoru grupowego oraz nazwy alkoholu będącego substratem reakcji dehydratacji. Zadanie 26.1. Arkusz CKE chemia maj 2021 rozszerzony (1 punkt)
Alkeny można otrzymać m.in. w wyniku reakcji eliminacji wody z alkoholi (tzw. reakcja dehydratacji alkoholi).
Poddano dehydratacji 3-metylobutan-2-ol i otrzymano mieszaninę alkenów A i B, przy czym alken A jest produktem głównym (atom wodoru jest odrywany w tym przypadku od tego atomu węgla, który jest połączony z mniejszą liczbą atomów wodoru), a alken B – produktem ubocznym przemiany.
Produkt A można także otrzymać w wyniku dehydratacji innego alkoholu.
Podaj wzór półstrukturalny (grupowy) i nazwę systematyczną tego alkoholu. Wzór: Nazwa systematyczna:
Zapis równania reakcji alkenu z HBr prowadzącej do głównego produktu organicznego. Zadanie 26.2. Arkusz CKE chemia maj 2021 rozszerzony (1 punkt)
Alkeny można otrzymać m.in. w wyniku reakcji eliminacji wody z alkoholi (tzw. reakcja dehydratacji alkoholi).
Poddano dehydratacji 3-metylobutan-2-ol i otrzymano mieszaninę alkenów A i B, przy czym alken A jest produktem głównym (atom wodoru jest odrywany w tym przypadku od tego atomu węgla, który jest połączony z mniejszą liczbą atomów wodoru), a alken B – produktem ubocznym przemiany.
Napisz równanie reakcji alkenu A z bromowodorem (HBr) prowadzącej do powstania produktu głównego tej przemiany. Zastosuj wzory półstrukturalne (grupowe) związków organicznych.

