Przypisanie mechanizmów reakcji dla procesów addycji oraz substytucji. Zadanie 26. Arkusz CKE chemia maj 2015 rozszerzony (1 punkt)
Przeprowadzono doświadczenie z udziałem dwóch różnych węglowodorów. W wyniku dwóch odrębnych reakcji − jednej addycji, a drugiej substytucji − i przy użyciu odpowiednich reagentów jako główny produkt każdej reakcji otrzymano 2-bromo-2-metylobutan.
Określ, według jakiego mechanizmu (nukleofilowego, rodnikowego, elektrofilowego) przebiega każda z opisanych reakcji. Reakcja addycji przebiega według mechanizm: Reakcja substytucji przebiega według mechanizmu:
Wyjaśnienie, dlaczego głównym produktem reakcji addycji i substytucji jest 2-bromo-2-metylobutan. Zadanie 27. Arkusz CKE chemia maj 2015 rozszerzony (1 punkt)
Przeprowadzono doświadczenie z udziałem dwóch różnych węglowodorów. W wyniku dwóch odrębnych reakcji − jednej addycji, a drugiej substytucji − i przy użyciu odpowiednich reagentów jako główny produkt każdej reakcji otrzymano 2-bromo-2-metylobutan.
Wyjaśnij, dlaczego głównym produktem opisanych reakcji addycji i substytucji jest ta sama monobromopochodna 2-metylobutanu (2-bromo-2-metylobutan).
Zapis wzoru grupowego alkoholu na podstawie opisu struktury jego cząsteczki oraz reakcji jakiej ulega. Zadanie 28. Arkusz CKE chemia maj 2015 rozszerzony (2 punkty)
W cząsteczce pewnego optycznie czynnego nasyconego łańcuchowego alkoholu monohydroksylowego o nierozgałęzionym łańcuchu jest pięć atomów węgla. W wyniku utlenienia tego alkoholu powstaje keton.
Narysuj wzór półstrukturalny (grupowy), podaj nazwę systematyczną oraz określ rzędowość opisanego alkoholu. Wzór: Nazwa: Rzędowość:
Wskazanie poprawnych nazw systematycznych dwóch związków organicznych. Zadanie 29. Arkusz CKE chemia maj 2015 rozszerzony (1 punkt)
Poniżej przedstawiono wzory dwóch związków organicznych.
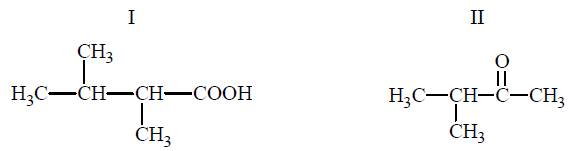
Zaznacz odpowiedź, w której podano poprawne nazwy systematyczne związków I i II.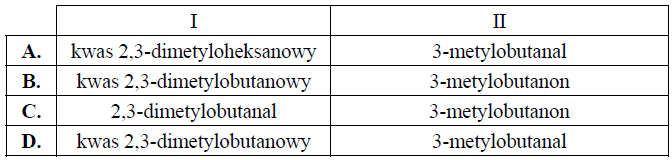
Wybór poprawnych zdań opisujących narysowany związek chemiczny. Zadanie 30. Arkusz CKE chemia maj 2015 rozszerzony (1 punkt)
Poniżej przedstawiono wzory dwóch związków organicznych.
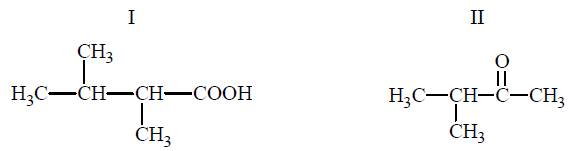
Z podanych niżej informacji wybierz i zaznacz te, które są prawdziwe dla związku II. 1. W wyniku redukcji tego związku wodorem powstaje 3-metylobutan-2-ol. 2. Po dodaniu tego związku do świeżo strąconego wodorotlenku miedzi(II) i ogrzaniu obserwuje się zmianę zabarwienia zawartości probówki z niebieskiej na ceglastą. 3. Związek ten powstaje w wyniku utleniania alkoholu II-rzędowego. 4. Związek ten reaguje bezpośrednio z sodem, w wyniku czego tworzy sól.
Obliczanie pH roztworu kwasu etanowego o stężeniu 6% masowych. Zadanie 31. Arkusz CKE chemia maj 2015 rozszerzony (2 punkty)
Oblicz pH wodnego roztworu kwasu etanowego o stężeniu 6,0% masowych i gęstości 1,00 g·cm−3 (t = 25 °C), dla którego stopień dysocjacji α ˂ 5%. Wynik końcowy zaokrąglij do pierwszego miejsca po przecinku.
Rysowanie alkoholu furfurylowego stanowiącego produkt reakcji redukcji furfuralu. Zadanie 32.1. Arkusz CKE chemia maj 2015 rozszerzony (1 punkt)
Furfural jest pochodną furanu. W cząsteczce furfuralu występuje grupa funkcyjna, która łatwo redukuje się w obecności wodoru, co prowadzi do powstania alkoholu furfurylowego. Na gorąco, pod wpływem wodorotlenku miedzi(II), grupa ta się utlenia, w wyniku czego powstaje kwas pirośluzowy.
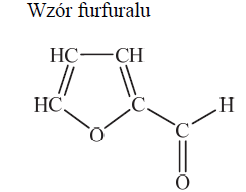
Na podstawie: K.-H. Lautenschläger, W. Schröter, A. Wanninger, Nowoczesne kompendium chemii, Warszawa 2007.
Narysuj wzór półstrukturalny (grupowy) lub uproszczony alkoholu furfurylowego, otrzymanego na drodze redukcji furfuralu.
Zapis równania reakcji prowadzącej do powstania kwasu pirośluzowego. Zadanie 32.2. Arkusz CKE chemia maj 2015 rozszerzony (1 punkt)
Furfural jest pochodną furanu. W cząsteczce furfuralu występuje grupa funkcyjna, która łatwo redukuje się w obecności wodoru, co prowadzi do powstania alkoholu furfurylowego. Na gorąco, pod wpływem wodorotlenku miedzi(II), grupa ta się utlenia, w wyniku czego powstaje kwas pirośluzowy.

Na podstawie: K.-H. Lautenschläger, W. Schröter, A. Wanninger, Nowoczesne kompendium chemii, Warszawa 2007.
Uzupełnij poniższy schemat, tak aby otrzymać równanie opisanej reakcji otrzymywania kwasu pirośluzowego. Zastosuj wzory półstrukturalne (grupowe) lub uproszczone związków organicznych.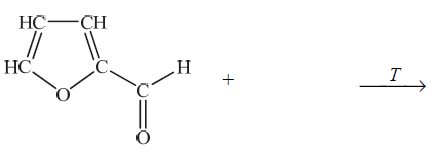
Wybór poprawnych odczynników w celu porównania mocy kwasów pirogronowego i octowego. Zadanie 33.1. Arkusz CKE chemia maj 2015 rozszerzony (1 punkt)
Moc kwasów można porównać na podstawie analizy ich stałych dysocjacji albo metodą doświadczalną. Stała dysocjacji kwasu pirogronowego jest równa Ka = 4,1·10−3 w t = 25 °C.
Na podstawie: J. Sawicka i inni, Tablice chemiczne, Gdańsk 2004.
Porównaj wartości stałych dysocjacji kwasu pirogronowego i kwasu etanowego, a następnie zaprojektuj doświadczenie, w którym zajdzie reakcja potwierdzająca, że jeden z nich jest mocniejszy.
Uzupełnij poniższy schemat doświadczenia, wpisując wzory użytych odczynników wybranych spośród: Schemat doświadczenia:
– CH3COCOOH (aq)
– CH3COCOONa (aq)
– CH3COOH (aq)
– CH3COONa (aq)
– NaOH (aq)
Opis zmian towarzyszących przeprowadzonemu doświadczeniu porównania mocy kwasów pirogronowego i octowego. Zadanie 33.2. Arkusz CKE chemia maj 2015 rozszerzony (1 punkt)
Moc kwasów można porównać na podstawie analizy ich stałych dysocjacji albo metodą doświadczalną. Stała dysocjacji kwasu pirogronowego jest równa Ka = 4,1·10−3 w t = 25 °C.
Na podstawie: J. Sawicka i inni, Tablice chemiczne, Gdańsk 2004.
Porównaj wartości stałych dysocjacji kwasu pirogronowego i kwasu etanowego, a następnie zaprojektuj doświadczenie, w którym zajdzie reakcja potwierdzająca, że jeden z nich jest mocniejszy.
Opisz zmiany, które potwierdzają, że wybrany kwas jest mocniejszy od drugiego.
Wybór odczynnika pozwalającego odróżnić parafinę od stearyny. Zadanie 34. Arkusz CKE chemia maj 2015 rozszerzony (1 punkt)
W dwóch nieoznakowanych probówkach znajdują się parafina i stearyna.
Zaznacz poprawne dokończenie zdania. W celu zidentyfikowania tych substancji należy A. porównać ich rozpuszczalność w wodzie. B. zbadać ich zachowanie wobec wody bromowej. C. zbadać ich zachowanie wobec wodorotlenku sodu. D. zbadać ich zachowanie wobec stężonego kwasu azotowego(V).
Rysowanie wzoru Hawortha α-D-mannopiranozy na podstawie jej projekcji Fischera. Zadanie 35. Arkusz CKE chemia maj 2015 rozszerzony (1 punkt)
Wzory monosacharydów można przedstawiać, posługując się projekcją Fischera (wzory liniowe) lub projekcją Hawortha (wzory taflowe). Poniżej przedstawiono wzór D-glukozy w projekcji Fischera oraz wzór α-D-glukopiranozy w projekcji Hawortha.
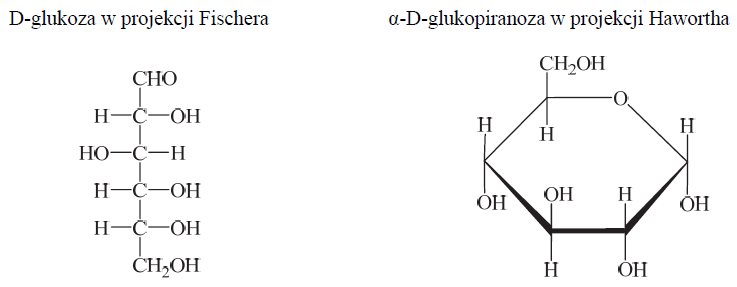
Przeanalizuj wzór D-mannozy w projekcji Fischera i uzupełnij schemat, tak aby przedstawiał on wzór α-D-mannopiranozy w projekcji Hawortha.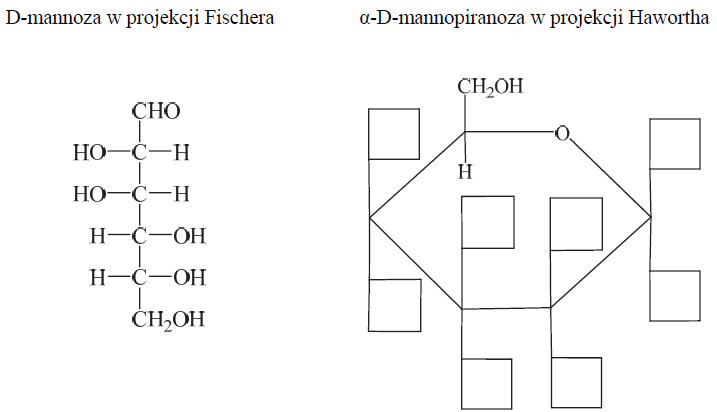
Uszeregowanie tłuszczy zgodnie ze wzrastającą liczbą jodową. Zadanie 36. Arkusz CKE chemia maj 2015 rozszerzony (1 punkt)
Liczba jodowa jest miarą liczby wiązań nienasyconych, np. w tłuszczach. Określa ona liczbę gramów jodu, który może przyłączyć w warunkach standardowych 100 gramów tłuszczu.
Na podstawie: Encyklopedia szkolna. Chemia, Kraków 2005.
Poniżej podano wzory trzech tłuszczów.
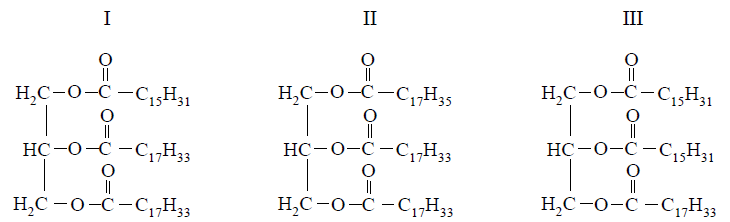
Uszereguj tłuszcze o podanych wzorach zgodnie ze wzrastającą liczbą jodową − zapisz w kolejności numery, którymi je oznaczono.
Zapis nazw zidentyfikowanych związków chemicznych. Zadanie 37. Arkusz CKE chemia maj 2015 rozszerzony (1 punkt)
W czterech naczyniach (I–IV) znajdowały się wodne roztwory: glukozy, fenolu (benzenolu), glicerolu (propano-1,2,3-triolu) i glicyloalanyloglicyny. W celu ich identyfikacji przeprowadzono trzy serie doświadczeń. W pierwszej serii doświadczeń, po dodaniu wodnego roztworu chlorku żelaza(III) do próbek pobranych z czterech naczyń, próbka z naczynia I przyjęła fioletowe zabarwienie. W drugiej serii doświadczeń, po dodaniu świeżo strąconego wodorotlenku miedzi(II) do próbek pobranych z trzech naczyń (II, III i IV), próbka z naczynia II przyjęła fioletowe zabarwienie, a w pozostałych próbkach pojawiło się szafirowe zabarwienie. W trzeciej serii doświadczeń, po ogrzaniu szafirowych roztworów otrzymanych w serii drugiej, w roztworze powstałym z próbki z naczynia III pojawił się ceglasty osad.
Podaj nazwy związków, które zidentyfikowano w wyniku każdej z serii doświadczeń. Seria I (naczynie I): roztwór Seria II (naczynie II): roztwór Seria III (naczynie III): roztwór (naczynie IV): roztwór
Zapis nazwy reakcji chemicznej, której przebieg doprowadził do powstania fioletowego zabarwienia. Zadanie 38. Arkusz CKE chemia maj 2015 rozszerzony (1 punkt)
W czterech naczyniach (I–IV) znajdowały się wodne roztwory: glukozy, fenolu (benzenolu), glicerolu (propano-1,2,3-triolu) i glicyloalanyloglicyny. W celu ich identyfikacji przeprowadzono trzy serie doświadczeń. W pierwszej serii doświadczeń, po dodaniu wodnego roztworu chlorku żelaza(III) do próbek pobranych z czterech naczyń, próbka z naczynia I przyjęła fioletowe zabarwienie. W drugiej serii doświadczeń, po dodaniu świeżo strąconego wodorotlenku miedzi(II) do próbek pobranych z trzech naczyń (II, III i IV), próbka z naczynia II przyjęła fioletowe zabarwienie, a w pozostałych próbkach pojawiło się szafirowe zabarwienie. W trzeciej serii doświadczeń, po ogrzaniu szafirowych roztworów otrzymanych w serii drugiej, w roztworze powstałym z próbki z naczynia III pojawił się ceglasty osad.
Podaj nazwę reakcji chemicznej przeprowadzonej w drugiej serii doświadczeń, w wyniku której roztwór z naczynia II przyjął fioletowe zabarwienie.