Zapis liczby atomowej, symbolu pierwiastka oraz liczby masowej izotopu. Zadanie 1.1. Arkusz CKE chemia czerwiec 2024 rozszerzony (1 punkt)
Liczba atomowa pierwiastka X jest dwa razy większa od liczby atomowej rutenu (Ru). Liczba neutronów w jądrze pewnego izotopu pierwiastka X jest równa liczbie masowej izotopu baru, w którego jądrze znajduje się 81 neutronów. Z tego izotopu pierwiastka X w ciągu rozpadów α i β– powstaje nietrwały izotop ołowiu zawierający w jądrze 127 neutronów. Ten izotop ulega następnie przemianie w trwały izotop 209Bi.
Uzupełnij tabelę. Wpisz wartość liczby atomowej i symbol pierwiastka X oraz wartość liczby masowej opisanego izotopu pierwiastka X.
Wskazanie liczby przemian alfa oraz beta. Zadanie 1.2. Arkusz CKE chemia czerwiec 2024 rozszerzony (1 punkt)
Liczba atomowa pierwiastka X jest dwa razy większa od liczby atomowej rutenu (Ru). Liczba neutronów w jądrze pewnego izotopu pierwiastka X jest równa liczbie masowej izotopu baru, w którego jądrze znajduje się 81 neutronów. Z tego izotopu pierwiastka X w ciągu rozpadów α i β– powstaje nietrwały izotop ołowiu zawierający w jądrze 127 neutronów. Ten izotop ulega następnie przemianie w trwały izotop 209Bi.
Uzupełnij tabelę. Wpisz liczbę przemian α i β– zachodzących podczas powstawania izotopu ołowiu z opisanego izotopu pierwiastka X.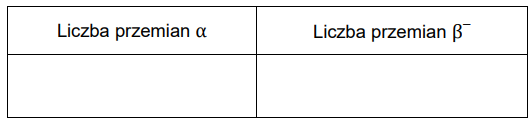
Zapis równania przemiany jądrowej. Zadanie 1.3. Arkusz CKE chemia czerwiec 2024 rozszerzony (1 punkt)
Liczba atomowa pierwiastka X jest dwa razy większa od liczby atomowej rutenu (Ru). Liczba neutronów w jądrze pewnego izotopu pierwiastka X jest równa liczbie masowej izotopu baru, w którego jądrze znajduje się 81 neutronów. Z tego izotopu pierwiastka X w ciągu rozpadów α i β– powstaje nietrwały izotop ołowiu zawierający w jądrze 127 neutronów. Ten izotop ulega następnie przemianie w trwały izotop 209Bi.
Napisz równanie – opisanej w informacji – przemiany izotopu ołowiu w izotop bizmutu. Uzupełnij wszystkie pola w poniższym schemacie.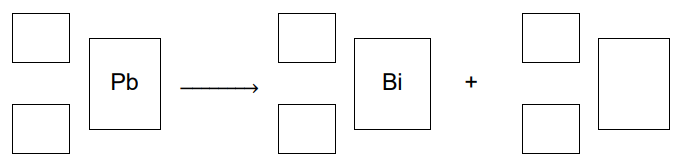
Zapis wzoru elektronowego monomeru chlorku galu(III). Zadanie 2.1. Arkusz CKE chemia czerwiec 2024 rozszerzony (1 punkt)
Gal tworzy trihalogenki, np. chlorek galu(III). W fazie stałej chlorek galu(III) występuje głównie w postaci dimerów, a w fazie gazowej – jako mieszanina dimerów i monomerów. Monomer chlorku galu(III) jest płaską cząsteczką, w której wszystkie atomy chloru są równocenne. Model dimeru przedstawiono na rysunku.
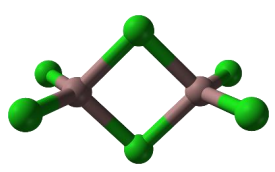
Na podstawie: CRC Handbook of Chemistry and Physics 97th Edition, CRC Press 2017.
Narysuj wzór elektronowy monomeru chlorku galu(III). Zaznacz kreskami wiążące i wolne pary elektronowe.
Określanie typu hybrydyzacji orbitali walencyjnych atomu galu. Zadanie 2.2. Arkusz CKE chemia czerwiec 2024 rozszerzony (1 punkt)
Gal tworzy trihalogenki, np. chlorek galu(III). W fazie stałej chlorek galu(III) występuje głównie w postaci dimerów, a w fazie gazowej – jako mieszanina dimerów i monomerów. Monomer chlorku galu(III) jest płaską cząsteczką, w której wszystkie atomy chloru są równocenne. Model dimeru przedstawiono na rysunku.

Na podstawie: CRC Handbook of Chemistry and Physics 97th Edition, CRC Press 2017.
Uzupełnij tabelę. Napisz, jaki typ hybrydyzacji (sp, sp2 albo sp3 ) przypisuje się orbitalom walencyjnym atomu galu w monomerze oraz w dimerze chlorku galu(III).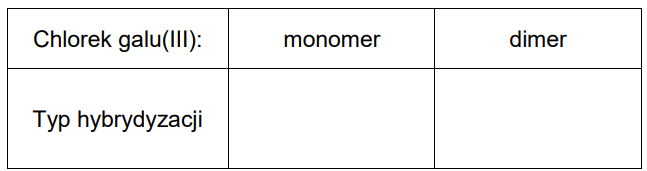
Wyjaśnienie przyczyny możliwości łączenia się monomerów chlorku galu(III) w dimery. Zadanie 2.3. Arkusz CKE chemia czerwiec 2024 rozszerzony (1 punkt)
Gal tworzy trihalogenki, np. chlorek galu(III). W fazie stałej chlorek galu(III) występuje głównie w postaci dimerów, a w fazie gazowej – jako mieszanina dimerów i monomerów. Monomer chlorku galu(III) jest płaską cząsteczką, w której wszystkie atomy chloru są równocenne. Model dimeru przedstawiono na rysunku.

Na podstawie: CRC Handbook of Chemistry and Physics 97th Edition, CRC Press 2017.
Wyjaśnij, dlaczego monomery chlorku galu(III) mają zdolność łączenia się w dimery. Uwzględnij sposób powstawania wiązań, dzięki którym z monomeru chlorku galu(III) powstaje dimer.
Uzupełnienie schematu klatkowego konfiguracji elektronowej kationu tytanu(II). Zadanie 3.1. Arkusz CKE chemia czerwiec 2024 rozszerzony (1 punkt)
Tytan jest lekkim metalem odpornym na korozję. W zależności od stopnia utlenienia tytanu chlorki tego pierwiastka odznaczają się różnymi właściwościami fizycznymi. Wartości temperatury topnienia i temperatury wrzenia dwóch związków tytanu z chlorem zestawiono w poniższej tabeli.

Reakcja tlenku tytanu(IV) – o wzorze TiO2 – z tetrachlorometanem w temperaturze 500 °C prowadzi do powstania chlorku tytanu(IV) oraz tlenku węgla(IV) (reakcja 1.). Z kolei chlorek tytanu(II) – jako jedyny produkt reakcji – można otrzymać w wyniku przepuszczania par chlorku tytanu(IV) w temperaturze 1040 °C nad metalicznym tytanem (reakcja 2.).
Na podstawie: L. Kolditz, Chemia nieorganiczna, Warszawa 1994.
Uzupełnij poniższy schemat, tak aby przedstawiał on graficzny (klatkowy) zapis konfiguracji elektronowej jonu Ti2+ w stanie podstawowym. W zapisie uwzględnij numer powłoki i symbol podpowłoki.
Wskazanie wartości głównej oraz pobocznej liczby kwantowej. Zadanie 3.2. Arkusz CKE chemia czerwiec 2024 rozszerzony (1 punkt)
Tytan jest lekkim metalem odpornym na korozję. W zależności od stopnia utlenienia tytanu chlorki tego pierwiastka odznaczają się różnymi właściwościami fizycznymi. Wartości temperatury topnienia i temperatury wrzenia dwóch związków tytanu z chlorem zestawiono w poniższej tabeli.

Reakcja tlenku tytanu(IV) – o wzorze TiO2 – z tetrachlorometanem w temperaturze 500 °C prowadzi do powstania chlorku tytanu(IV) oraz tlenku węgla(IV) (reakcja 1.). Z kolei chlorek tytanu(II) – jako jedyny produkt reakcji – można otrzymać w wyniku przepuszczania par chlorku tytanu(IV) w temperaturze 1040 °C nad metalicznym tytanem (reakcja 2.).
Na podstawie: L. Kolditz, Chemia nieorganiczna, Warszawa 1994.
Uzupełnij tabelę. Wpisz wartości dwóch liczb kwantowych: głównej i pobocznej, które opisują stan energetyczny jednego z niesparowanych elektronów atomu tytanu w stanie podstawowym.
Wybór właściwych wyrażeń dotyczących sieci krystalicznej tytanu oraz chlorku tytanu(II). Zadanie 3.3. Arkusz CKE chemia czerwiec 2024 rozszerzony (1 punkt)
Tytan jest lekkim metalem odpornym na korozję. W zależności od stopnia utlenienia tytanu chlorki tego pierwiastka odznaczają się różnymi właściwościami fizycznymi. Wartości temperatury topnienia i temperatury wrzenia dwóch związków tytanu z chlorem zestawiono w poniższej tabeli.

Reakcja tlenku tytanu(IV) – o wzorze TiO2 – z tetrachlorometanem w temperaturze 500 °C prowadzi do powstania chlorku tytanu(IV) oraz tlenku węgla(IV) (reakcja 1.). Z kolei chlorek tytanu(II) – jako jedyny produkt reakcji – można otrzymać w wyniku przepuszczania par chlorku tytanu(IV) w temperaturze 1040 °C nad metalicznym tytanem (reakcja 2.).
Na podstawie: L. Kolditz, Chemia nieorganiczna, Warszawa 1994.
Uzupełnij poniższe zdania. Wybierz i zaznacz jedno określenie spośród podanych w każdym nawiasie. Sieć krystaliczna metalicznego tytanu składa się z (atomów / kationów) otoczonych chmurą zdelokalizowanych elektronów. W sieci krystalicznej chlorku tytanu(II) obecne są (atomy / jony). Ze wzrostem stopnia utlenienia tytanu w chlorkach (maleje / rośnie) jonowy charakter wiązania.
Zapis równań reakcji otrzymywania chlorku tytanu(IV) oraz rozstrzygnięcie, czy są to reakcje redoks. Zadanie 3.4. Arkusz CKE chemia czerwiec 2024 rozszerzony (2 punkty)
Tytan jest lekkim metalem odpornym na korozję. W zależności od stopnia utlenienia tytanu chlorki tego pierwiastka odznaczają się różnymi właściwościami fizycznymi. Wartości temperatury topnienia i temperatury wrzenia dwóch związków tytanu z chlorem zestawiono w poniższej tabeli.

Reakcja tlenku tytanu(IV) – o wzorze TiO2 – z tetrachlorometanem w temperaturze 500 °C prowadzi do powstania chlorku tytanu(IV) oraz tlenku węgla(IV) (reakcja 1.). Z kolei chlorek tytanu(II) – jako jedyny produkt reakcji – można otrzymać w wyniku przepuszczania par chlorku tytanu(IV) w temperaturze 1040 °C nad metalicznym tytanem (reakcja 2.).
Na podstawie: L. Kolditz, Chemia nieorganiczna, Warszawa 1994.
Napisz w formie cząsteczkowej równania opisanych reakcji otrzymywania TiCl4 (reakcja 1.) i TiCl2 (reakcja 2.). Rozstrzygnij, czy dana przemiana jest reakcją utleniania-redukcji. Zaznacz TAK albo NIE. Równanie reakcji 1.: Rozstrzygnięcie: TAK NIE Równanie reakcji 2.: Rozstrzygnięcie: TAK NIE
Ocena poprawności zdań dotyczących kinetyki reakcji. Zadanie 4. Arkusz CKE chemia czerwiec 2024 rozszerzony (1 punkt)
Reakcja rozkładu tlenku azotu(V) przebiega według równania:
2N2O5 (g) → 4NO2 (g) + O2 (g)
Zależność szybkości tej reakcji od stężenia N2O5 przedstawia równanie kinetyczne: 𝑣 = 𝑘 ∙ CN2O5. W temperaturze 65 °C wartość stałej szybkości reakcji 𝑘 jest równa 5,2 · 10−3 s−1.
Na podstawie: L. Jones, P. Atkins, Chemia ogólna. Cząsteczki, materia, reakcje, Warszawa 2004.
Oceń prawdziwość poniższych zdań. Zaznacz P, jeżeli zdanie jest prawdziwe, albo F – jeśli jest fałszywe. 1. Stała szybkości 𝑘 opisanej reakcji prowadzonej w temperaturze T wyższej niż 65 °C będzie miała wartość mniejszą niż 5,2 · 10−3 s−1. 2. Początkowa szybkość reakcji rozkładu tlenku azotu(V) w temperaturze 65 °C wzrasta czterokrotnie po czterokrotnym wzroście stężenia N2O5.
Obliczenie chwilowej szybkości reakcji utleniania. Zadanie 5. Arkusz CKE chemia czerwiec 2024 rozszerzony (4 punkty) zadanie problemowe
Równanie kinetyczne wyznacza się doświadczalnie. W tym celu dokonuje się wielokrotnego pomiaru szybkości reakcji przy zmianie stężenia tylko jednego z reagentów. Takie postępowanie pozwala określić, jak zmiana stężenia wpływa na wartość szybkości reakcji. Przeprowadzono trzy doświadczenia, w których określono początkową szybkość reakcji przebiegającej w temperaturze T według równania:
S2O82− (aq) + 3I− (aq) → 2SO42− (aq) + I3− (aq)
Równanie kinetyczne przedstawionego procesu ma postać: 𝑣 = 𝑘 ∙ CS2O82−𝑚 ∙ CI–𝑛. Wartości stężenia jonów S2O82− i I− oraz uzyskane wartości początkowej szybkości zaniku jonów S2O82− podano w poniższej tabeli. Przedstawione dane pozwoliły określić współczynniki 𝑚 i 𝑛 w równaniu kinetycznym tej reakcji.
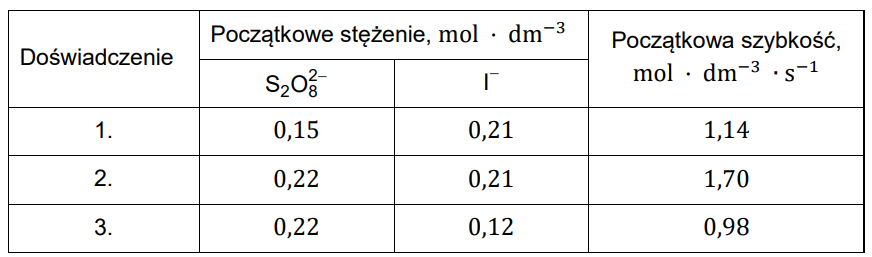
Na podstawie: L. Jones, P. Atkins, Chemia ogólna. Cząsteczki, materia, reakcje, Warszawa 2004.
Oblicz szybkość reakcji (wyrażoną w jednostce: mol · dm−3 · s−1) w doświadczeniu 1. w chwili, gdy w wyniku zachodzącej reakcji stężenie jonów S2O82− obniży się do wartości 0,10 mol · dm−3.
Dokończenie zdania dotyczącego kinetyki reakcji chemicznej. Zadanie 6. Arkusz CKE chemia czerwiec 2024 rozszerzony (1 punkt)
Badano szybkość reakcji opisanej równaniem
(CH3)3CCl (c) + H2O (c) → (CH3)3C(OH) (aq) + HCl (aq)
Dokończ zdanie. Wybierz odpowiedź A albo B i jej uzasadnienie 1., 2. albo 3. Pomiar pH roztworu, w którym zachodzi opisana reakcja,
Ocena poprawności zdań dotyczących syntezy chlorowodoru. Zadanie 7. Arkusz CKE chemia czerwiec 2024 rozszerzony (1 punkt)
Poniżej przedstawiono równanie syntezy chlorowodoru.
H2 (g) + Cl2 (g) ⇄ 2HCl (g)
Tę reakcję prowadzono w zamkniętym reaktorze i po pewnym czasie w układzie reakcyjnym ustaliła się równowaga.
Odczytaj w tablicy wartość standardowej molowej entalpii tworzenia HCl i oceń prawdziwość poniższych zdań. Zaznacz P, jeśli zdanie jest prawdziwe, albo F – jeśli jest fałszywe. 1. Podwyższenie temperatury (w warunkach izobarycznych) skutkuje wzrostem wydajności tworzenia chlorowodoru. 2. Zmiana ciśnienia (w warunkach izotermicznych) nie wpływa na wydajność tworzenia chlorowodoru.
Określenie rodzaju efektu energetycznego reakcji tlenku węgla(IV) z wodorem. Zadanie 8. Arkusz CKE chemia czerwiec 2024 rozszerzony (1 punkt)
Reakcja tlenku węgla(IV) z wodorem przebiega zgodnie z równaniem:
CO2 (g) + H2 (g) ⇄ CO (g) + H2O (g)
W tabeli przedstawiono wartości stężeniowej stałej równowagi Kc tej reakcji w wybranych temperaturach.

Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Rozstrzygnij, czy reakcja tlenku węgla(IV) z wodorem jest procesem endoenergetycznym. Odpowiedź uzasadnij. Rozstrzygnięcie: Uzasadnienie: