Wskazanie liczby powstałych monobromopochodnych oraz zapis nazwy jednej z nich. Zadanie 25.1. Arkusz CKE chemia czerwiec 2023 rozszerzony (1 punkt)
W reakcjach substytucji na świetle względna reaktywność atomów wodoru połączonych z atomami węgla o różnej rzędowości wskazuje, że najłatwiej ulega podstawieniu atom wodoru związany z atomem węgla o najwyższej rzędowości. Ilości poszczególnych produktów zależą od liczby atomów wodoru o określonej rzędowości oraz od ich reaktywności i są zwykle podawane w przeliczeniu na jeden atom wodoru jako tzw. współczynnik reaktywności. Względna ilość produktu reakcji substytucji jest iloczynem liczby atomów wodoru o określonej rzędowości i ich współczynnika reaktywności.
Dla reakcji monochlorowania w temperaturze pokojowej współczynniki reaktywności atomów wodoru wynoszą odpowiednio:
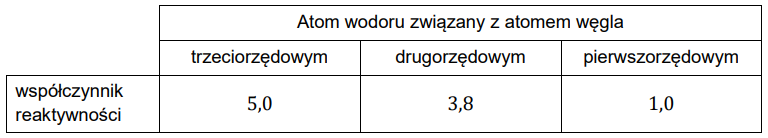
Podobny szereg reaktywności 3° > 2° > 1° dla monobromowania alkanów wyraża się stosunkiem znacznie większych liczb. Dla reakcji monobromowania w temperaturze 127 °C współczynniki reaktywności atomów wodoru wynoszą odpowiednio:
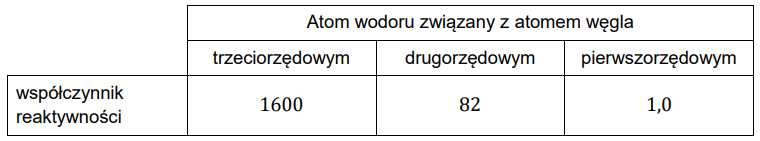
Na podstawie: R.T. Morrison, R.N. Boyd, Chemia organiczna, Warszawa 1996.
Napisz: Liczba monobromopochodnych: Nazwa systematyczna:
• liczbę różnych monobromopochodnych będących izomerami konstytucyjnymi, które można otrzymać w reakcji monobromowania 2-metylopentanu na świetle
• nazwę systematyczną tej monobromopochodnej, która powstaje z największą wydajnością.
Wyjaśnienie przyczyny występowania praktycznie jednego organicznego produktu w reakcji monobromowania. Zadanie 25.2. Arkusz CKE chemia czerwiec 2023 rozszerzony (1 punkt)
W reakcjach substytucji na świetle względna reaktywność atomów wodoru połączonych z atomami węgla o różnej rzędowości wskazuje, że najłatwiej ulega podstawieniu atom wodoru związany z atomem węgla o najwyższej rzędowości. Ilości poszczególnych produktów zależą od liczby atomów wodoru o określonej rzędowości oraz od ich reaktywności i są zwykle podawane w przeliczeniu na jeden atom wodoru jako tzw. współczynnik reaktywności. Względna ilość produktu reakcji substytucji jest iloczynem liczby atomów wodoru o określonej rzędowości i ich współczynnika reaktywności.
Dla reakcji monochlorowania w temperaturze pokojowej współczynniki reaktywności atomów wodoru wynoszą odpowiednio:

Podobny szereg reaktywności 3° > 2° > 1° dla monobromowania alkanów wyraża się stosunkiem znacznie większych liczb. Dla reakcji monobromowania w temperaturze 127 °C współczynniki reaktywności atomów wodoru wynoszą odpowiednio:

Na podstawie: R.T. Morrison, R.N. Boyd, Chemia organiczna, Warszawa 1996.
Wyjaśnij, dlaczego główny produkt reakcji monobromowania 2,3-dimetylobutanu w temperaturze 𝟏𝟐𝟕 °𝐂 jest praktycznie jedynym produktem tej reakcji.
Określanie wzoru grupowego związku. Zadanie 26. Arkusz CKE chemia czerwiec 2023 rozszerzony (4 punkty) zadanie problemowe
Próbkę pewnego związku organicznego A o masie 4,4 g spalono w tlenie i otrzymano wyłącznie 8,8 g tlenku węgla(IV) oraz 3,6 g wody. Stwierdzono, że:
• łańcuch węglowy cząsteczki tego związku jest nierozgałęziony
• ten związek w roztworze wodnym dysocjuje z odszczepieniem jonu wodorowego
• całkowite spalenie 0,05 mol tego związku wymaga użycia 0,25 mol tlenu.
Ustalono także, że związki umownie oznaczone literami X i Y są izomerami związku organicznego A. Związek X jest kwasem karboksylowym. Cząsteczki związku Y o nierozgałęzionym łańcuchu węglowym nie są chiralne, a wynik reakcji tego związku z odczynnikiem Trommera przedstawiono na zdjęciu. Związek Y może brać udział w reakcjach estryfikacji.

Napisz wzór półstrukturalny (grupowy) opisanego związku organicznego A oraz wzory półstrukturalne (grupowe) związków X i Y.
Określanie stopnia utlenienia atomu węgla, typu hybrydyzacji oraz liczby wiązań pi w cząsteczce witaminy A. Zadanie 27.1. Arkusz CKE chemia czerwiec 2023 rozszerzony (2 punkty)
Wzory szkieletowe związków organicznych odzwierciedlają kształt łańcucha węglowego. W tych wzorach pomija się symbole atomów węgla i połączonych z nimi atomów wodoru, a szkielet węglowy rysuje się jako linię łamaną i zaznacza – występujące w cząsteczce – wiązania wielokrotne. Zapisuje się symbole podstawników innych niż wodór oraz wzory grup funkcyjnych. Niekiedy, w celu jednoznacznej interpretacji wzoru, uwzględnia się w nich atom węgla.
Poniżej przedstawiono wzór witaminy A (retinolu):
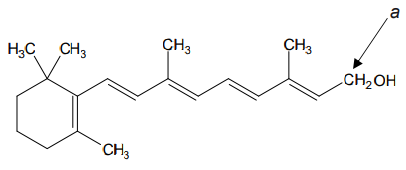
Na podstawie: P. Mastalerz, Chemia organiczna, Wrocław 2016.
Uzupełnij tabelę. Wpisz formalny stopień utlenienia oraz typ hybrydyzacji (sp, sp2 , sp3) orbitali walencyjnych atomu węgla oznaczonego literą a w cząsteczce witaminy A (retinolu) oraz liczbę wszystkich wiązań 𝝅 w tej cząsteczce.
Ocena poprawności zdań dotyczących ciągu przemian z udziałem retinolu. Zadanie 27.2. Arkusz CKE chemia czerwiec 2023 rozszerzony (1 punkt)
Wzory szkieletowe związków organicznych odzwierciedlają kształt łańcucha węglowego. W tych wzorach pomija się symbole atomów węgla i połączonych z nimi atomów wodoru, a szkielet węglowy rysuje się jako linię łamaną i zaznacza – występujące w cząsteczce – wiązania wielokrotne. Zapisuje się symbole podstawników innych niż wodór oraz wzory grup funkcyjnych. Niekiedy, w celu jednoznacznej interpretacji wzoru, uwzględnia się w nich atom węgla.
Poniżej przedstawiono wzór witaminy A (retinolu):

Na podstawie: P. Mastalerz, Chemia organiczna, Wrocław 2016.
Witamina A (retinol) to substancja niezbędna do prawidłowego funkcjonowania organizmu. Jej źródłem są m.in. estry – związki takie jak palmitynian czy octan retinylu. Z tych estrów powstaje retinol, który ulega kolejnym przemianom. Na schemacie przedstawiono wybrane etapy metabolizmu witaminy A w komórkach.
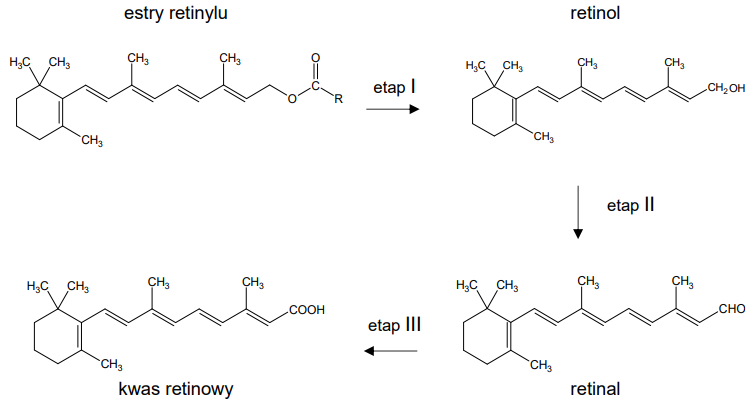
Na podstawie: M. Zasada, A. Adamczyk, Witamina A. Budowa i mechanizm działania, „Kosmetologia Estetyczna” 2018, nr 5, vol. 7.
Oceń prawdziwość poniższych zdań. Zaznacz P, jeśli zdanie jest prawdziwe, albo F – jeśli jest fałszywe. 1. Podczas etapu I, w którym powstaje retinol, zachodzi hydroliza estrów. 2. W etapie III 1 mol retinalu oddaje 2 mol elektronów.
Wybór odpowiednich wyrażeń w celu dokończenia zdania dotyczącego retinolu i retinalu. Zadanie 27.3. Arkusz CKE chemia czerwiec 2023 rozszerzony (1 punkt)
Wzory szkieletowe związków organicznych odzwierciedlają kształt łańcucha węglowego. W tych wzorach pomija się symbole atomów węgla i połączonych z nimi atomów wodoru, a szkielet węglowy rysuje się jako linię łamaną i zaznacza – występujące w cząsteczce – wiązania wielokrotne. Zapisuje się symbole podstawników innych niż wodór oraz wzory grup funkcyjnych. Niekiedy, w celu jednoznacznej interpretacji wzoru, uwzględnia się w nich atom węgla.
Poniżej przedstawiono wzór witaminy A (retinolu):

Na podstawie: P. Mastalerz, Chemia organiczna, Wrocław 2016.
Witamina A (retinol) to substancja niezbędna do prawidłowego funkcjonowania organizmu. Jej źródłem są m.in. estry – związki takie jak palmitynian czy octan retinylu. Z tych estrów powstaje retinol, który ulega kolejnym przemianom. Na schemacie przedstawiono wybrane etapy metabolizmu witaminy A w komórkach.

Na podstawie: M. Zasada, A. Adamczyk, Witamina A. Budowa i mechanizm działania, „Kosmetologia Estetyczna” 2018, nr 5, vol. 7.
Dokończ zdanie. Wybierz i zaznacz odpowiedź A albo B oraz uzasadnienie 1., 2. albo 3. Retinol i retinal
Zapis sumarycznego równania reakcji anionu octanowego z 1-chlorobutanem. Zadanie 28.1. Arkusz CKE chemia czerwiec 2023 rozszerzony (1 punkt)
Estry można otrzymać w reakcji alifatycznych chlorowcopochodnych z solami kwasów karboksylowych. Poniżej przedstawiono mechanizm reakcji – zachodzącej w obecności jodków – między pierwszorzędowym halogenkiem alkilowym a anionem karboksylanowym:
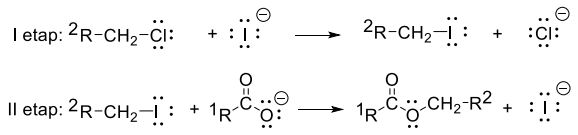
Na podstawie: J. McMurry, Chemia organiczna, Warszawa 2005.
Napisz sumaryczne równanie reakcji anionu octanowego z 1-chlorobutanem. Zastosuj wzory półstrukturalne (grupowe) związków organicznych.
Wybór właściwych wyrazów w nawiasach. Zadanie 28.2. Arkusz CKE chemia czerwiec 2023 rozszerzony (1 punkt)
Estry można otrzymać w reakcji alifatycznych chlorowcopochodnych z solami kwasów karboksylowych. Poniżej przedstawiono mechanizm reakcji – zachodzącej w obecności jodków – między pierwszorzędowym halogenkiem alkilowym a anionem karboksylanowym:

Na podstawie: J. McMurry, Chemia organiczna, Warszawa 2005.
Uzupełnij poniższe zdania. Wybierz i zaznacz jedną odpowiedź spośród podanych w każdym nawiasie. Opisane przemiany, w których udział biorą alifatyczne chlorowcopochodne i sole kwasów karboksylowych, są reakcjami (addycji / substytucji). Anion jodkowy pełni funkcję katalizatora i jego obecność skutkuje (obniżeniem / podwyższeniem) energii aktywacji oraz wzrostem (szybkości / wydajności) reakcji w porównaniu do reakcji prowadzonej bez jego udziału.
Rozstrzygnięcie czy kwas sorbowy może pełnić funkcję utleniacza. Zadanie 29. Arkusz CKE chemia czerwiec 2023 rozszerzony (1 punkt)
Przeciwutleniacze i konserwanty to ważne dodatki do żywności. Przeciwutleniacze zawierają w swoich cząsteczkach takie elementy budowy, które mogą ulegać utlenianiu, dzięki czemu zapobiegają utlenianiu innych substancji. Z kolei działanie konserwantów polega na dezaktywacji enzymów oraz na zahamowaniu rozwoju drobnoustrojów. Jako konserwantów można używać kwasu sorbowego oraz jego soli, sorbinianów: sodu, potasu, wapnia. Wzór kwasu sorbowego podano poniżej:
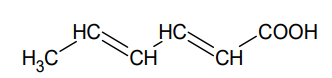
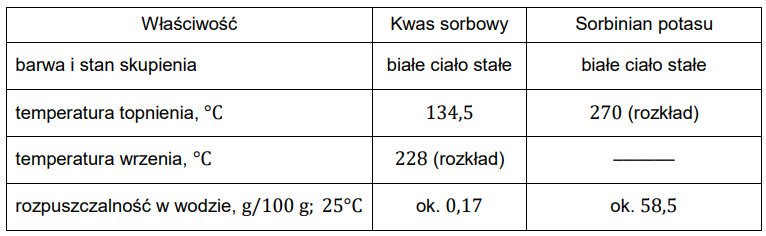
W tabeli zebrano wybrane właściwości fizykochemiczne kwasu sorbowego i sorbinianiu potasu.
Wartość 𝐾a dla kwasu sorbowego wynosi 1,7 ∙ 10–5.
Na podstawie: Z.E. Sikorski (red.), Chemia żywności, Warszawa 2007 oraz W. Grajek (red.), Przeciwutleniacze w żywności, Warszawa 2007.
Rozstrzygnij, czy kwas sorbowy może pełnić funkcję przeciwutleniacza. W uzasadnieniu odwołaj się do elementów budowy cząsteczki kwasu. Rozstrzygnięcie: Uzasadnienie:
Wybór właściwego odczynnika wraz z uzasadnieniem wyboru. Zadanie 31. Arkusz CKE chemia czerwiec 2023 rozszerzony (1 punkt)
Przeciwutleniacze i konserwanty to ważne dodatki do żywności. Przeciwutleniacze zawierają w swoich cząsteczkach takie elementy budowy, które mogą ulegać utlenianiu, dzięki czemu zapobiegają utlenianiu innych substancji. Z kolei działanie konserwantów polega na dezaktywacji enzymów oraz na zahamowaniu rozwoju drobnoustrojów. Jako konserwantów można używać kwasu sorbowego oraz jego soli, sorbinianów: sodu, potasu, wapnia. Wzór kwasu sorbowego podano poniżej:

W tabeli zebrano wybrane właściwości fizykochemiczne kwasu sorbowego i sorbinianiu potasu.

Wartość 𝐾a dla kwasu sorbowego wynosi 1,7 ∙ 10–5.
Na podstawie: Z.E. Sikorski (red.), Chemia żywności, Warszawa 2007 oraz W. Grajek (red.), Przeciwutleniacze w żywności, Warszawa 2007.
Wybierz i zaznacz nazwę odczynnika, który wprowadzony w postaci roztworu pozwoli odróżnić wodny roztwór kwasu sorbowego i wodny roztwór sorbinianu potasu o jednakowych stężeniach. Odpowiedź uzasadnij. brom fenoloftaleina Uzasadnienie:
Uzupełnienie schematu reakcji hydrolizy zasadowej kwasu pantotenowego. Zadanie 32. Arkusz CKE chemia czerwiec 2023 rozszerzony (1 punkt)
Kwas pantotenowy wchodzi w skład witaminy B5. Jego wzór chemiczny przedstawiono poniżej:
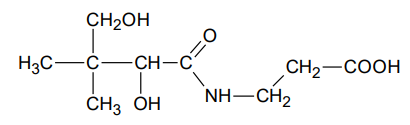
Kwas pantotenowy może ulegać hydrolizie zasadowej.
Uzupełnij poniższy schemat, tak aby przedstawiał w formie jonowej skróconej równanie hydrolizy zasadowej kwasu pantotenowego. Zastosuj wzory półstrukturalne (grupowe) lub uproszczone związków organicznych.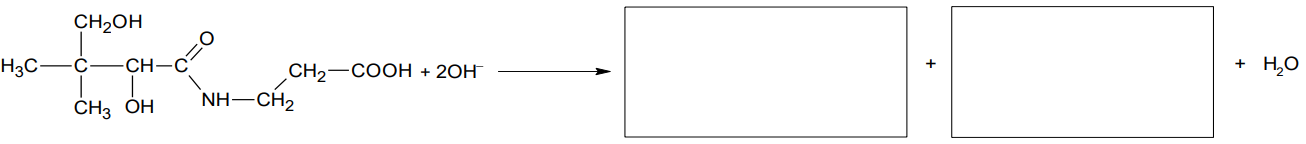
Rozstrzygnięcie czy cząsteczka kwasu pantotenowego jest chiralna. Zadanie 33. Arkusz CKE chemia czerwiec 2023 rozszerzony (1 punkt)
Kwas pantotenowy wchodzi w skład witaminy B5. Jego wzór chemiczny przedstawiono poniżej:

Kwas pantotenowy może ulegać hydrolizie zasadowej.
Rozstrzygnij, czy cząsteczka kwasu pantotenowego jest chiralna. Odpowiedź uzasadnij. Rozstrzygnięcie: Uzasadnienie:
Rysowanie wzorów dwóch monomerów Nomexu. Zadanie 34.1. Arkusz CKE chemia czerwiec 2023 rozszerzony (1 punkt)
Nomex to polimer stosowany do produkcji materiałów o wysokiej odporności mechanicznej i termicznej. Fragment jego łańcucha przedstawiono poniżej:
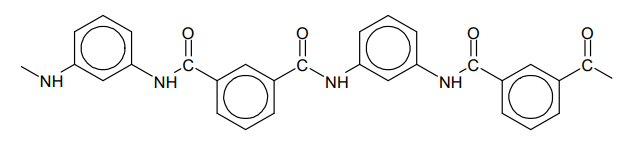
Monomery, z których można otrzymać nomex, różnią się charakterem kwasowo-zasadowym.
Uzupełnij tabelę. Narysuj wzory półstrukturalne (grupowe) lub uproszczone dwóch monomerów, z których można otrzymać ten polimer.
Wybór właściwych wyrazów w nawiasach. Zadanie 34.2. Arkusz CKE chemia czerwiec 2023 rozszerzony (1 punkt)
Nomex to polimer stosowany do produkcji materiałów o wysokiej odporności mechanicznej i termicznej. Fragment jego łańcucha przedstawiono poniżej:

Uzupełnij zdania. Wybierz i podkreśl jedno określenie spośród podanych w każdym nawiasie. Nomex otrzymuje się w wyniku polimeryzacji (łańcuchowej / kondensacyjnej). W tej przemianie (wydziela się / nie wydziela się) produkt uboczny.