Znaleziono 12 wyników wyszukiwania dla słowa: Iloczyn rozpuszcz
TEMAT VII. Wykład: Równowagi w roztworach wodnych, część 1 - prawo rozcieńczeń Ostwalda, pH, iloczyn rozpuszczalności, bufory
Podczas tego wykładu omówione zostały zagadnienia związane z procesami równowagowymi w roztworach wodnych.
Film podzielony jest na rozdziały. Możesz wybrać dowolny z nich, klikając na pasek postępu w odtwarzaczu.
0:00 Wstęp
0:24 Pojęcie elektrolitu, elektrolity mocne oraz słabe
1:54 Pojęcie stopnia dysocjacji elektrolitu
4:23 Kwasy i zasady w ujęciu teorii Arrheniusa
7:40 Kwasy i zasady w ujęciu teorii Lewisa (teoria elektronowa)
10:15 Kwasy i zasady w ujęciu teorii Brønsteda-Lowry’ego (teoria protonowa)
12:41 Drobiny amfiprotyczne
16:22 Pojęcie stałej równowagi dysocjacji elektrolitu
19:33 Prawo rozcieńczeń Ostwalda
22:42 Kiedy stosujemy wzór dokładny, a kiedy uproszczony prawa rozcieńczeń Ostwalda?
26:20 Która wielkość lepiej opisuje moc elektrolitu – stała, czy stopień dysocjacji?
32:58 Reakcje wypierania kwasów słabych przez inne kwasy słabe
35:55 Kolejność reakcji mieszaniny kwasów Brønsteda z zasadą Brønsteda
39:07 Kolejność reakcji mieszaniny zasad Brønsteda z kwasem Brønsteda
41:43 Autodysocjacja wody oraz innych związków chemicznych, iloczyn jonowy wody
45:33 Zależność iloczynu jonowego wody od temperatury
49:11 Skala pH, obliczanie wartości pH i pOH roztworu
51:41 Zależność pH od stężeń roztworów mocnych i słabych kwasów oraz zasad
55:38 Wpływ autodysocjacji wody na pH silnie rozcieńczonych roztworów mocnych kwasów i zasad
1:00:04 Relacja między stałą dysocjacji oraz stałą hydrolizy w roztworach soli
1:03:43 Dysocjacja czy hydroliza w roztworach wodorosoli
1:07:00 Pojęcie substancji trudno rozpuszczalnej w wodzie, reakcje strąceniowe
1:09:42 Iloczyn rozpuszczalności
1:12:46 Rozpuszczalność substancji a iloczyn rozpuszczalności
1:15:33 Rozpuszczalność molowa, określanie, który związek jest lepiej rozpuszczalny w wodzie
1:20:17 Rozpuszczalność substancji a efekt wspólnego jonu
1:22:41 Kolejność strącania osadów
1:25:48 Twardość wody
1:28:04 Roztwory buforowe, bufor amonowy
1:32:06 Roztwory buforowe, bufor octanowy
1:34:01 Roztwory buforowe, bufor fosforanowy
Po obejrzeniu tej lekcji należy zapoznać się z następującymi tutorialami oraz artykułami:
1. Prawo rozcieńczeń Ostwalda.
2. Zależność między stopniem dysocjacji i wartością wyrażenia Co/K.
6. Równowagi jonowe z udziałem wodorotlenku cynku.
Czas trwania wykładu: 1 godzina 37 minut 19 sekund. Forma wykładu: film – prezentacja multimedialna z lektorem (Rafał Szczypiński).
Obliczanie ilości wody, jaka pozwoliłaby na rozpuszczenie określonej porcji związku trudno rozpuszczalnego (iloczyn rozpuszczalności)
W temperaturze 25 ⁰C iloczyn rozpuszczalności wodorotlenku magnezu ma wartość 7,94∙10−12, a węglanu wapnia 3,31∙10–9.
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Oblicz minimalną objętość wody destylowanej, jaką należałoby dodać do 100 cm3 nasyconego w temperaturze 25 ⁰C roztworu wodorotlenku magnezu, aby możliwe było rozpuszczenie dodatkowej porcji tego związku chemicznego o masie 5,8 mg. Wynik podaj w centymetrach sześciennych, z dokładnością do cyfry jedności. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie rozpuszczalności wodorotlenku w roztworze o odczynie zasadowym (iloczyn rozpuszczalności)
W temperaturze 25 ⁰C iloczyn rozpuszczalności wodorotlenku magnezu ma wartość 7,94∙10−12, a węglanu wapnia 3,31∙10–9.
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Oblicz rozpuszczalność wodorotlenku magnezu w temperaturze 25 ⁰C, w roztworze o wartości pH równej 12. Wynik podaj w μg/dm3 (mikrogramach na decymetr sześcienny roztworu), z dokładnością do dwóch cyfr znaczących. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określanie, czy strąci się osad substancji trudno rozpuszczalnej (iloczyn rozpuszczalności)
Iloczyn rozpuszczalności jest wielkością opisującą równowagę dynamiczną, jaka ustala się między osadem substancji trudno rozpuszczalnej, a jej nasyconym roztworem. W tabeli zebrano dane na temat wartości iloczynów rozpuszczalności trzech soli baru w temperaturze 25 ⁰C.
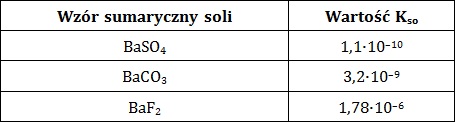
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Uzasadnij (wykonując stosowne obliczenia), czy strąci się osad węglanu baru, jeśli w temperaturze 25 ⁰C zmieszamy ze sobą 10 cm3 0,001-molowego roztworu chlorku baru z 15 cm3 0,002-molowego roztworu węglanu potasu? Rozwiązanie tego zadania dostępne jest nieodpłatnie pod poniższym linkiem: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie masy związku chemicznego, jaką można rozpuścić w roztworze zawierającym wspólny jon (iloczyn rozpuszczalności)
Iloczyn rozpuszczalności jest wielkością opisującą równowagę dynamiczną, jaka ustala się między osadem substancji trudno rozpuszczalnej, a jej nasyconym roztworem. W tabeli zebrano dane na temat wartości iloczynów rozpuszczalności trzech soli baru w temperaturze 25 ⁰C.

Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Oblicz masę fluorku baru, jaką można rozpuścić w 100 cm3 roztworu azotanu(V) baru o stężeniu równym 0,005 mol∙dm–3 w temperaturze 25 ⁰C. Wynik podaj w miligramach, z dokładnością do cyfry jedności. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie liczby jonów w nasyconym roztworze trudno rozpuszczalnego związku chemicznego (iloczyn rozpuszczalności)
Iloczyn rozpuszczalności jest wielkością opisującą równowagę dynamiczną, jaka ustala się między osadem substancji trudno rozpuszczalnej, a jej nasyconym roztworem. W tabeli zebrano dane na temat wartości iloczynów rozpuszczalności trzech soli baru w temperaturze 25 ⁰C.

Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Oblicz liczbę jonów pochodzących z dysocjacji siarczanu(VI) baru, jakie znajdują się w 500 cm3 nasyconego w temperaturze 25 ⁰C wodnego roztworu tej soli. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określanie objętości roztworu, jaką należy dodać do nasyconego roztworu zawierającego wspólny jon, aby doszło do zmniejszenia się rozpuszczalności (iloczyn rozpuszczalności)
W temperaturze 25 ⁰C iloczyn rozpuszczalności wodorotlenku magnezu ma wartość 7,94∙10−12, a węglanu wapnia 3,31∙10–9.
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Oblicz, jaką objętość 0,05-molowego roztworu wodorotlenku potasu należy dodać do 220 cm3 nasyconego w 25 ⁰C roztworu wodorotlenku magnezu, aby rozpuszczalność Mg(OH)2 zmalała 20-krotnie? Wynik podaj w centymetrach sześciennych, z dokładnością do cyfry jedności. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wybór poprawnych określeń dotyczących układu zawierającego trudno rozpuszczalny siarczan(VI) wapnia (iloczyn rozpuszczalności)
W temperaturze 25 ⁰C do zlewki zawierającej 250 cm3 wody destylowanej wprowadzono 30 g siarczanu(VI) wapnia, którego iloczyn rozpuszczalności (Kso) w opisanych warunkach ma wartość 3,16∙10–5. Zawartość naczynia zamieszano bagietką i odstawiono na kilka godzin utrzymując podaną wyżej temperaturę. W ten sposób uzyskano układ, którego schemat ilustruje rysunek poniżej. Literami A i B oznaczono pewne jego składniki.
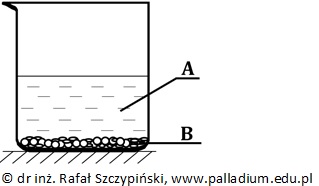
Zakładając, że ubytek wody powstały na skutek jej parowania został uzupełniony do ilości wyjściowej, podkreśl wyrażenia w nawiasach tak, by powstały zdania prawdziwe. W opisanym układzie klarowny roztwór znajdujący się nad osadem siarczanu(VI) wapnia jest roztworem (nienasyconym/nasyconym). Literą A oznaczono substancję (prostą/złożoną), która jest mieszaniną (jednorodną/niejednorodną), natomiast literą B substancję (prostą/złożoną), którą jest związek chemiczny tworzący kryształy (molekularne/jonowe). © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Opis obserwacji towarzyszących przeprowadzonemu doświadczeniu z udziałem wodnej zawiesiny siarczanu(VI) wapnia wraz z uzasadnieniem (iloczyn rozpuszczalności)
W temperaturze 25 ⁰C do zlewki zawierającej 250 cm3 wody destylowanej wprowadzono 30 g siarczanu(VI) wapnia, którego iloczyn rozpuszczalności (Kso) w opisanych warunkach ma wartość 3,16∙10–5. Zawartość naczynia zamieszano bagietką i odstawiono na kilka godzin utrzymując podaną wyżej temperaturę. W ten sposób uzyskano układ, którego schemat ilustruje rysunek poniżej. Literami A i B oznaczono pewne jego składniki.

Opisaną w informacji wprowadzającej zawartość zlewki przesączono. Do przesączu dodano pewną ilość wodnego roztworu chlorku wapnia i zaobserwowano objaw świadczący o przebiegu reakcji chemicznej. Napisz, co zaobserwowano w wyniku przeprowadzonego w temperaturze 25 ⁰C doświadczenia? Odpowiedź uzasadnij równaniem reakcji chemicznej, zapisanym w formie jonowej skróconej. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie minimalnej wartości pH roztworu sprzyjającej strąceniu osadu wodorotlenku wapnia (iloczyn rozpuszczalności)
W pewnej temperaturze rozpuszczalność wodorotlenku wapnia wynosi około 90 mg na 100 g wody.
Oblicz, przy jakiej minimalnej wartości pH w opisanych warunkach strąca się osad tego wodorotlenku? Wynik podaj z dokładnością do trzech cyfr znaczących. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone