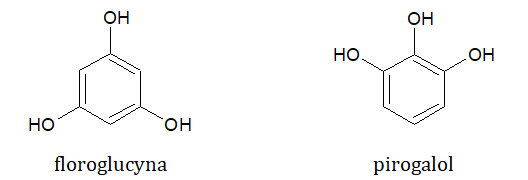Wyjaśnienie przyczyny najniższej temperatury wrzenia określonej aminy
W tabeli zebrano informacje na temat wartości temperatur wrzenia (1013 hPa) trzech wybranych amin alifatycznych: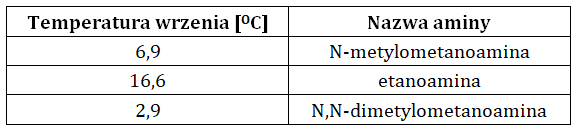
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Wyjaśnij, dlaczego wśród wymienionych amin temperatura wrzenia N,N-dimetylometanoaminy jest najniższa, pomimo największej masy cząsteczkowej tego związku chemicznego? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Zapis równania reakcji z udziałem roztworu fenolanu potasu oraz tlenku węgla(IV)
Podczas przepuszczania gazowego tlenku węgla(IV) przez wodny roztwór fenolanu potasu obserwuje się mętnienie zawartości naczynia reakcyjnego. Przyczyną takiego zjawiska jest powstający fenol, który w warunkach prowadzonego doświadczenia niezbyt dobrze rozpuszcza się w wodzie. Drugim produktem reakcji jest słabszy od fenolu anionowy kwas Brønsteda.
Stosując grupowe lub uproszczone wzory związków organicznych napisz w formie jonowej skróconej równanie opisanej przemiany chemicznej. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określanie mocy fenoli jako kwasów na podstawie wartości stałych dysocjacji
W poniższej tabeli zebrano dane na temat stałych dysocjacji trzech związków chemicznych A÷C o nazwach: 2-metylofenol (o-metylofenol), 4-nitrofenol (p-nitrofenol) oraz fenol.
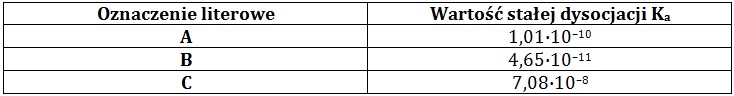
Moc fenoli jako kwasów Brønsteda maleje, gdy w ich cząsteczkach pojawia się ugrupowanie alkilowe.
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Przyporządkuj literom A, B i C nazwy podanych związków chemicznych. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określanie odczynu roztworów fenolanów oraz uszeregowanie ich według wzrastającej wartości pH
W poniższej tabeli zebrano dane na temat stałych dysocjacji trzech związków chemicznych A÷C o nazwach: 2-metylofenol (o-metylofenol), 4-nitrofenol (p-nitrofenol) oraz fenol.

Moc fenoli jako kwasów Brønsteda maleje, gdy w ich cząsteczkach pojawia się ugrupowanie alkilowe.
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Określ odczyn 0,1-molowych wodnych roztworów soli potasowych wymienionych związków chemicznych, a następnie uszereguj je zgodnie z rosnącą wartością pH. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Rysowanie wzoru półstrukturalnego cząsteczki imidu oraz określanie liczby wiązań sigma i pi
Przykładem pochodnych kwasów karboksylowych są imidy, w cząsteczkach których atom azotu połączony jest z atomami węgla obu grup karbonylowych.
Narysuj wzór półstrukturalny cząsteczki imidu kwasu benzeno-1,2-dikarboksylowego i określ liczbę znajdujących się w niej wiązań σ oraz wiązań π. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie rozpuszczalności hydratu chlorku żelaza(II) na podstawie stężenia procentowego nasyconego roztworu (rozpuszczalność substancji)
Nasycony w temperaturze 20 oC wodny roztwór chlorku żelaza(II) ma stężenie równe 38,5%.
Oblicz (wyrażoną w g/100 g wody) rozpuszczalność hydratu o wzorze sumarycznym FeCl2∙4H2O użytego do sporządzenia opisanego nasyconego roztworu chlorku żelaza(II). Wynik podaj z dokładnością do całkowitej liczby gramów. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określenie przyczyny bardzo dobrej rozpuszczalności sorbitolu w wodzie
Sorbitol jest wielohydroksylowym, bardzo dobrze rozpuszczalnym w wodzie alkoholem. Zamieszczony rysunek przedstawia wzór cząsteczki tego związku chemicznego, narysowany w projekcji Fischera. Zmieniając pojedynczo konfigurację na przeciwną tylko dwóch jego centrów chiralności (w jednym z nich zmieniamy, a przy drugim wówczas już nie – i na odwrót), uzyskuje się dwa nieczynne optycznie izomeryczne alkohole A i B.
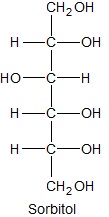
Wyjaśnij, dlaczego sorbitol jest związkiem chemicznym bardzo dobrze rozpuszczalnym w wodzie? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie rozpuszczalności siarczanu(VI) magnezu na podstawie rozpuszczalności jego hydratu (rozpuszczalność substancji)
W temperaturze 20 oC rozpuszczalność siarczanu(VI) magnezu-woda (1/7) ma wartość równą 105,5 g/100 g wody.
Na podstawie: W. Mizerski, Tablice chemiczne, Warszawa 2013.
Rozpuszczając w wodzie w danych warunkach określoną masę hydratu można uzyskać nasycony roztwór soli bezwodnej.
Oblicz rozpuszczalność bezwodnego siarczanu(VI) magnezu w temperaturze 20 oC. Wynik podaj w g/ 100 g wody, z dokładnością do trzech cyfr znaczących. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone