Określanie symboli pierwiastków chemicznych oraz ich położenia w układzie okresowym. Zadanie 1.1. Informator CKE chemia 2023 rozszerzony (2 punkty)
O dwóch pierwiastkach umownie oznaczonych literami X i Z wiadomo, że:
● konfigurację elektronową atomu pierwiastka X w jednym ze stanów wzbudzonych przedstawia zapis:
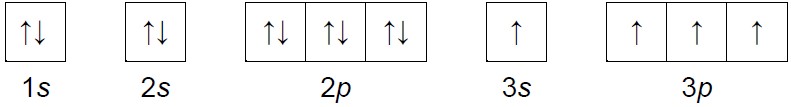
● łączna liczba elektronów na ostatniej powłoce i na podpowłoce 3d atomu w stanie podstawowym pierwiastka Z jest dwa razy większa od liczby elektronów walencyjnych atomu pierwiastka X.
Uzupełnij poniższą tabelę. Wpisz symbole pierwiastków X i Z, numer grupy układu okresowego oraz symbol bloku konfiguracyjnego, do którego należy każdy z pierwiastków.
Przypisywanie wartości liczb kwantowych dla elektronu. Zadanie 1.2. Informator CKE chemia 2023 rozszerzony (1 punkt)
O dwóch pierwiastkach umownie oznaczonych literami X i Z wiadomo, że:
● konfigurację elektronową atomu pierwiastka X w jednym ze stanów wzbudzonych przedstawia zapis:

● łączna liczba elektronów na ostatniej powłoce i na podpowłoce 3d atomu w stanie podstawowym pierwiastka Z jest dwa razy większa od liczby elektronów walencyjnych atomu pierwiastka X.
Wpisz do tabeli wartości dwóch liczb kwantowych: głównej i pobocznej, opisujące stan kwantowo-mechaniczny jednego z niesparowanych elektronów o najwyższej energii atomu pierwiastka X w przedstawionym stanie wzbudzonym.
Zapis konfiguracji elektronowej dwudodatniego jonu. Zadanie 1.3. Informator CKE chemia 2023 rozszerzony (1 punkt)
O dwóch pierwiastkach umownie oznaczonych literami X i Z wiadomo, że:
● konfigurację elektronową atomu pierwiastka X w jednym ze stanów wzbudzonych przedstawia zapis:

● łączna liczba elektronów na ostatniej powłoce i na podpowłoce 3d atomu w stanie podstawowym pierwiastka Z jest dwa razy większa od liczby elektronów walencyjnych atomu pierwiastka X.
Przedstaw pełną konfigurację elektronową jonu Z2+ w stanie podstawowym. Zastosuj zapis konfiguracji elektronowej z uwzględnieniem podpowłok.
Wybór pierwiastków o różnych liczbach niesparowanych elektronów. Zadanie 2. Informator CKE chemia 2023 rozszerzony (1 punkt)
Wybierz parę pierwiastków, których atomy w stanie podstawowym mają różne liczby niesparowanych elektronów. Zaznacz poprawną odpowiedź. A. krzem i tytan
B. siarka i tytan
C. krzem i żelazo
D. siarka i nikiel