Znaleziono 20 wyników wyszukiwania dla słowa: izomeria optyczna
Rysowanie wzoru stereochemicznego określonego alkoholu (izomeria optyczna)
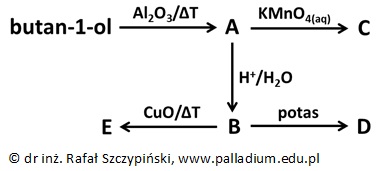
Pewne nasycone, izomeryczne alkohole łańcuchowe reagują z wapniem w stosunku wagowym równym (odpowiednio) 3:1, natomiast z sodem w stosunku molowym 1:1.
Istnieją pewne diole, których szkielety węglowe są takie same, jak opisanych izomerów reagujących z wapniem. Jeden z opisanych dioli wykazuje czynność optyczną.
Uzupełnij poniższy schemat tak, aby przedstawiał parę enancjomerów tego diolu. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określanie wzoru półstrukturalnego oraz nazwy związku organicznego (izomeria optyczna)
Pewien występujący w postaci enancjomerów nasycony, alifatyczny keton łańcuchowy A poddano redukcji wodorem. Produkt B tej reakcji odwodniono w obecności tlenku glinu i uzyskano równomolową mieszaninę alkenów C i D. Związek C występuje jako para izomerów geometrycznych, natomiast związek D – enancjomerów. Centrum chiralności związku D jest ten sam atom węgla, co w wyjściowym ketonie A. Głównymi produktami addycji wody do związków chemicznych C i D są alkohole o najwyższej rzędowości.
Wiedząc, że produktem addycji wodoru do alkenów jest 2,4-dimetyloheksan, podaj wzór półstrukturalny oraz nazwę systematyczną związku chemicznego A. Zapisz numer lokantu, którym opisany jest asymetryczny atom węgla w jego cząsteczce. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wskazanie czynnego optycznie produktu reakcji chemicznej oraz uzasadnienie, czy jest to produkt główny, czy uboczny (izomeria optyczna)
Trwałość izomerów geometrycznych zależy od tzw. oddziaływania przestrzennego (sterycznego) między dwoma objętościowymi podstawnikami po tej samej stronie wiązania podwójnego. Im oddziaływanie to jest silniejsze (podstawniki zajmują więcej miejsca w przestrzeni), tym izomer wykazuje mniejszą trwałość.
Na podstawie: J. McMurry, Chemia organiczna, Warszawa 2012.
Przykładem węglowodoru, który występuje w postaci izomerów geometrycznych jest związek chemiczny o nazwie 3-metylopent-2-en.
Jeden z izomerów opisanego węglowodoru o takim samym szkielecie węglowym poddano działaniu bromowodoru. Uzyskano mieszaninę czynnych optycznie związków chemicznych.
Podaj nazwę systematyczną tego produktu, który występuje w postaci diastereoizomerów. Określ, czy jest to główny, czy uboczny produkt przebiegającej reakcji chemicznej. Uzasadnij swoje stanowisko. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Rysowanie odpowiednich stereoizomerów będących alkenami (izomeria optyczna, izomeria geometryczna)
Pewien alken A oraz jego izomer konstytucyjny B tworzą różnego typu stereoizomery. Pierwszy z nich występuje wyłącznie w postaci pary enancjomerów, natomiast drugi jako para izomerów geometrycznych. Addycja wodoru w obecności katalizatora niklowego do związków A i B daje ten sam nieczynny optycznie produkt C. Związki chemiczne A i B są najlżejszymi alkenami spełniającymi opisane warunki.
Narysuj stereoizomery związków chemicznych A i B, aby w sposób jednoznaczny wskazywały na rodzaj występującej w ich cząsteczkach izomerii przestrzennej. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określanie wzoru półstrukturalnego związku chemicznego będącego wspólnym produktem reakcji (izomeria optyczna, izomeria geometryczna)
Pewien alken A oraz jego izomer konstytucyjny B tworzą różnego typu stereoizomery. Pierwszy z nich występuje wyłącznie w postaci pary enancjomerów, natomiast drugi jako para izomerów geometrycznych. Addycja wodoru w obecności katalizatora niklowego do związków A i B daje ten sam nieczynny optycznie produkt C. Związki chemiczne A i B są najlżejszymi alkenami spełniającymi opisane warunki.
Narysuj wzór półstrukturalny i podaj nazwę systematyczną związku chemicznego C. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Ocena poprawności stwierdzeń dotyczących struktury cząsteczek progesteronu oraz dydrogesteronu i reaktywności (izomeria optyczna)
Progesteron jest żeńskim hormonem płciowym, który umożliwia implantację zarodka w błonie śluzowej macicy. W celu podtrzymania ciąży (w przypadku niedoboru progesteronu) stosuje się lek o nazwie handlowej Duphaston, zawierający dydrogesteron, który jest pochodną progesteronu. Wzory chemiczne cząsteczek obu tych związków chemicznych przedstawiono na rysunkach poniżej.
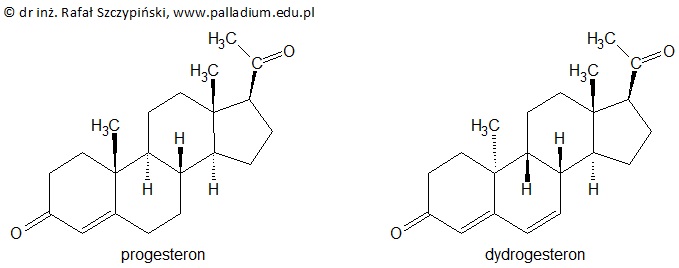
Dokonaj analizy wzorów cząsteczek progesteronu oraz dydrogesteronu, a następnie oceń poprawność poniższych zdań wpisując literę „P” (prawda) lub literę „F” (fałsz). 1. W cząsteczce progesteronu znajdują się trzy wiązania π, natomiast dydrogesteron ma cztery takie wiązania. 2. Każda z przedstawionych cząsteczek ma sześć asymetrycznych atomów węgla. 3. Progesteron oraz dydrogesteron są względem siebie diastereoizomerami. 4. W odpowiednich warunkach dydrogesteron może ulegać próbie jodoformowej. 5. W wyniku całkowitej hydrogenacji każdego z przedstawionych związków chemicznych otrzymuje się alkohole I-rzędowe. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Rysowanie projekcji Fischera enancjomeru cząsteczki kwasu D-glukonowego (izomeria optyczna)
Schemat biochemicznego procesu, w wyniku którego β-D-glukopiranoza przekształcona zostaje w kwas D-glukonowy ilustruje rysunek poniżej:
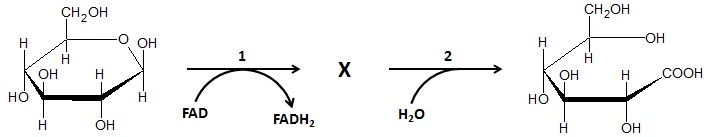
Na podstawie: J. Kączkowski, Podstawy biochemii, Warszawa 1976.
Narysuj wzór cząsteczki będącej enancjomerem kwasu D-glukonowego. W tym celu uzupełnij poniższy szablon projekcji Fischera. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone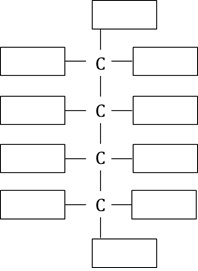
Rysowanie stereochemicznych wzorów enancjomerów tłuszczu o określonej liczbie jodowej (izomeria optyczna)
Liczba jodowa (Lj) określa masę jodu, jaka przyłącza się do 100 g tłuszczu. Dla pewnego trójglicerydu o masie cząsteczkowej równej 888 u liczba jodowa wynosi 28,6 g.
Wiedząc, że jedna z reszt kwasowych tego związku chemicznego jest pochodną drugiej z nich, a stosunek wagowy uzyskanych w wyniku jego zmydlenia soli sodowych równy jest 2:1, narysuj wzory stereochemiczne cząsteczek obu enancjomerów opisanego trójglicerydu. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Rysowanie wzoru stereochemicznego określonego stereoizomeru (izomeria optyczna)
Wzór cząsteczki peptydu o sekwencji aminokwasów Asp-Ser-Ser-Gly można przedstawić rysunkiem:
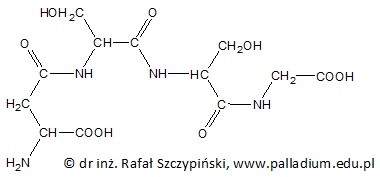
W cząsteczce narysowanego związku chemicznego reszta jednego z aminokwasów połączona jest wiązaniem peptydowym z resztą innego aminokwasu w sposób odmienny niż ten, jaki obserwuje się w łańcuchach peptydowych białek pochodzenia naturalnego.
Uzupełnij poniższy szablon tak, aby przedstawiał cząsteczkę niebiogennego aminokwasu, o którego reszcie mowa jest w powyższym tekście. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone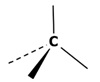
Rysowanie projekcji Fischera D-penicylaminy oraz wzoru stereochemicznego jej enancjomeru i określanie stopnia utlenienia centrum stereogenicznego cząsteczki (izomeria optyczna)
Penicylamina to zwyczajowa nazwa kwasu 2-amino-3-merkapto-3-metylobutanowego. Dzięki obecności grupy –SH (merkaptanowej), cząsteczki tego związku chemicznego mają zdolność do tworzenia trwałych kompleksów z dwu- oraz trójdodatnimi jonami tzw. metali ciężkich. Kompleksy takie stosunkowo łatwo usuwane są z organizmu. Fakt ten stanowił podstawę pierwotnego zastosowania D-penicylaminy, jakim była detoksykacja organizmu po zatruciu metalami ciężkimi.
Na podstawie: D. Steinhilber i inni, Chemia medyczna. Cele leków, substancje czynne, biologia chemiczna, Wrocław 2012.
Narysuj projekcję Fischera D-penicylaminy oraz wzór przestrzenny (stereochemiczny) jej enancjomeru, a następnie określ wartość stopnia utlenienia atomu węgla stanowiącego centrum stereogeniczne cząsteczki D-penicylaminy © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Rysowanie projekcji Fischera cząsteczek alkoholi, które nie wykazują czynności optycznej (izomeria optyczna)
Sorbitol jest wielohydroksylowym, bardzo dobrze rozpuszczalnym w wodzie alkoholem. Zamieszczony rysunek przedstawia wzór cząsteczki tego związku chemicznego, narysowany w projekcji Fischera. Zmieniając pojedynczo konfigurację na przeciwną tylko dwóch jego centrów chiralności (w jednym z nich zmieniamy, a przy drugim wówczas już nie – i na odwrót), uzyskuje się dwa nieczynne optycznie izomeryczne alkohole A i B.
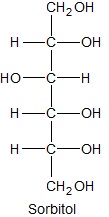
Narysuj projekcje Fischera alkoholi A i B, a następnie wyjaśnij dlaczego związki te nie wykazują czynności optycznej? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Określanie nazwy systematycznej sorbitolu oraz liczby asymetrycznych atomów węgla w cząsteczce (izomeria optyczna)
Sorbitol jest wielohydroksylowym, bardzo dobrze rozpuszczalnym w wodzie alkoholem. Zamieszczony rysunek przedstawia wzór cząsteczki tego związku chemicznego, narysowany w projekcji Fischera. Zmieniając pojedynczo konfigurację na przeciwną tylko dwóch jego centrów chiralności (w jednym z nich zmieniamy, a przy drugim wówczas już nie – i na odwrót), uzyskuje się dwa nieczynne optycznie izomeryczne alkohole A i B.

Podaj nazwę systematyczną sorbitolu, a następnie podkreśl wyrażenia w nawiasach tak, aby powstały zdania prawdziwe. Nazwa systematyczna sorbitolu: …………………………………………………………….…………………… Alkohole A i B są względem siebie (enancjomerami/diastereoizomerami), a liczba asymetrycznych atomów węgla w ich cząsteczkach jest (różna/taka sama). © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Ocena poprawności zdań dotyczących aminokwasu oraz hydroksyaldehydu (izomeria optyczna)
Rysunek poniżej przedstawia wzory chemiczne cząsteczek pewnych związków chemicznych.
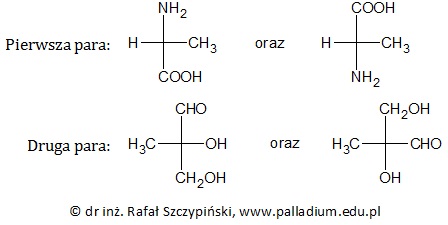
Oceń poprawność poniższych zdań dotyczących związków chemicznych, których wzory przedstawiono w informacji wprowadzającej. Wpisz literę „P” (prawda) lub literę „F” (fałsz). 1. Każda z narysowanych cząsteczek wykazuje czynność optyczną. 2. Pierwsza para stanowi związki chemiczne, których wodne roztwory mają odczyn obojętny. 3. Pierwszą parę związków chemicznych od drugiej pary można odróżnić stosując jako odczynnik wodny roztwór wodorowęglanu sodu. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wybór pary wzorów stanowiących tę samą cząsteczkę, ale inaczej narysowaną (izomeria optyczna)
Rysunek poniżej przedstawia wzory chemiczne cząsteczek pewnych związków chemicznych.

Spośród narysowanych wzorów związków organicznych wybierz parę przedstawiającą tę samą cząsteczkę, ale inaczej narysowaną, a następnie uwzględniając właściwy szereg konfiguracyjny (L lub D) podaj jej nazwę systematyczną. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone