Znaleziono 7 wyników wyszukiwania dla słowa: przerwan
Obliczanie procentu wagowego tlenku wapnia w mieszaninie poreakcyjnej uzyskanej po przerwaniu prażenia. Zadanie 16. Arkusz CKE chemia maj 2020 rozszerzony (2 punkty)
W laboratorium tlenek wapnia można otrzymać ze szczawianu wapnia o wzorze CaC2O4. Szczawian wapnia ulega termicznemu rozkładowi, który przebiega zgodnie z poniższym równaniem:
CaC2O4 → CaCO3 + CO
Dalsze ogrzewanie, w wyższej temperaturze, prowadzi do rozkładu węglanu wapnia:
CaCO3 → CaO + CO2
Próbkę szczawianu wapnia o masie 12,8 g umieszczono w tyglu pod wyciągiem i poddano prażeniu. Po pewnym czasie proces przerwano, a następnie ostudzono tygiel, zważono jego zawartość i zbadano skład mieszaniny poreakcyjnej. Stwierdzono, że masa zawartości tygla zmalała o 6,32 g i że otrzymana mieszanina nie zawierała szczawianu wapnia.
Oblicz w procentach masowych zawartość tlenku wapnia w mieszaninie otrzymanej po przerwaniu prażenia. Rozwiązanie tego zadania dostępne jest nieodpłatnie pod poniższym linkiem:
Obliczanie objętości powstałego azotu w przerwanej reakcji rozkładu dwuchromianu(VI) amonu
Reakcję termicznego rozkładu dwuchromianu(VI) amonu przedstawia równanie stechiometryczne:
(NH4)2Cr2O7 ⟶ Cr2O3 + N2 + 4H2O
Rozkładowi poddano 3,15 g substratu.
Oblicz objętość azotu (800 K, 1010 hPa) jaka powstała w tym doświadczeniu, jeśli w poreakcyjnej mieszaninie substancji stałych tlenek chromu(III) stanowił 70,7% masy. Wynik podaj w centymetrach sześciennych z przybliżeniem do cyfry jedności. Przyjmij, że uniwersalna stała gazowa ma wartość równą 83,1 hPa∙dm3∙mol–1∙K–1. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie, jaki procent początkowej ilości substratu uległ rozkładowi, gdy przerwano reakcję chemiczną
Na skalę laboratoryjną tlenek chromu(III) otrzymuje się podczas termicznego rozkładu dwuchromianu(VI) amonu:
(NH4)2Cr2O7 ⟶ Cr2O3 + N2 + 4H2O
Przez 10 sekund w tyglu porcelanowym prażono 12,6 g dwuchromianu(VI) amonu. Po tym czasie reakcję wstrzymano przez gwałtowne schłodzenie zawartości naczynia, a następnie ostrożnie odparowano powstałą wodę. Masa stałej pozostałości wynosiła 9,27 g.
Oblicz, jaki procent masy dwuchromianu(VI) amonu uległ rozkładowi? Wynik podaj z dokładnością do trzech cyfr znaczących. Rozwiązanie tego zadania dostępne jest nieodpłatnie pod poniższym linkiem: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Stosunek molowy stałych składników w mieszaninie poreakcyjnej po przerwaniu reakcji rozkładu dwuchromianu(VI) amonu
Na skalę laboratoryjną tlenek chromu(III) otrzymuje się podczas termicznego rozkładu dwuchromianu(VI) amonu:
(NH4)2Cr2O7 ⟶ Cr2O3 + N2 + 4H2O
Przez 10 sekund w tyglu porcelanowym prażono 12,6 g dwuchromianu(VI) amonu. Po tym czasie reakcję wstrzymano przez gwałtowne schłodzenie zawartości naczynia, a następnie ostrożnie odparowano powstałą wodę. Masa stałej pozostałości wynosiła 9,27 g.
Oblicz, w jakim stosunku molowym pozostawały względem siebie stałe składniki w uzyskanej mieszaninie poreakcyjnej? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie zawartości procentowej tlenku manganu(IV) w mieszaninie uzyskanej po przerwaniu reakcji rozkładu manganianu(VII) potasu
Przeprowadzono doświadczenie chemiczne, którego schemat ilustruje rysunek poniżej.
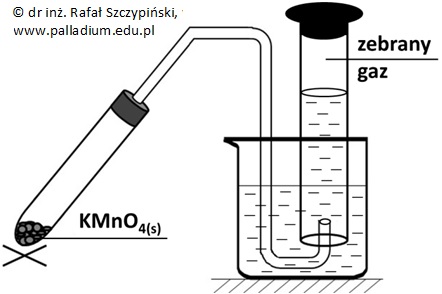
Rozkładowi termicznemu poddano próbkę manganianu(VII) potasu o masie 7,11 g. Wydzielający się gaz zbierano w cylindrze miarowym o pojemności 1 dm3, przy czym reakcję przerwano w momencie, gdy gaz stanowił 49,8% pojemności naczynia (80 oC, 1031 hPa). Opisana reakcja rozkładu przebiegła zgodnie z równaniem stechiometrycznym:
2KMnO4 ⟶ K2MnO4 + MnO2 + O2↑
Oblicz procent wagowy tlenku manganu(IV) w mieszaninie ciał stałych, jaka znajdowała się w probówce po przerwaniu ogrzewania jej zawartości. Wynik podaj z dokładnością do jednego miejsca po przecinku. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Przerwana reakcja rozkładu manganianu(VII) potasu
Odważono 3,95 g manganianu(VII) potasu i poddano termicznemu rozkładowi zgodnie z równaniem:
2KMnO4 ⟶ K2MnO4 + MnO2 + O2
Po zakończeniu doświadczenia stwierdzono, że w mieszaninie poreakcyjnej substancji stałych związek ten stanowił 21,8% masy.
Ile cm³ (warunki normalne) tlenu powstało? Wynik obliczeń podaj z dokładnością do cyfry jedności. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie stężenia procentowego sacharozy po przerwaniu reakcji hydrolizy. Zadanie 8. Arkusz CKE chemia maj 2011 rozszerzony (2 punkty)
Sporządzono 200 g roztworu zawierającego 100 g sacharozy. Sacharozę poddano reakcji hydrolizy:
![]()
Reakcję przerwano w momencie, gdy całkowite stężenie cukrów redukujących w roztworze było równe 40% masowych.
Oblicz stężenie sacharozy, wyrażone w procentach masowych, w roztworze po przerwaniu reakcji. W obliczeniach przyjmij przybliżone wartości mas molowych:![]()