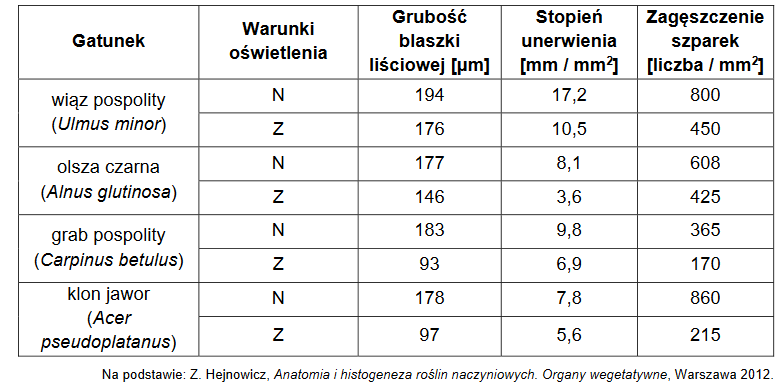
Znaleziono 26 wyników wyszukiwania dla słowa: blaszki
obserwacja przekrojów przez blaszki liściowe klonu cukrowego
Na poniższych rysunkach przedstawiono, z zachowaniem wspólnej skali, przekroje poprzeczne przez blaszki liści klonu cukrowego:
A. rosnących od południowej, w pełni oświetlonej strony korony drzewa,
B. znajdujących się w środkowej, zacienionej części korony drzewa.
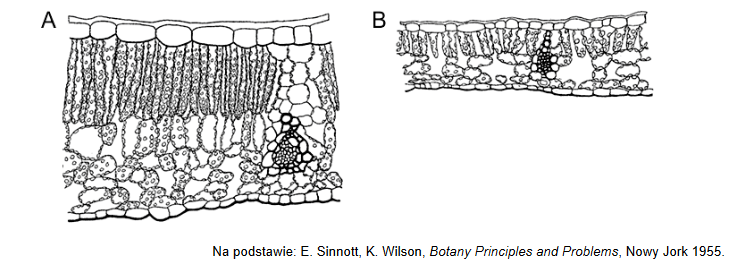
1. Sformułuj problem badawczy obserwacji przekrojów przez blaszki liściowe klonu cukrowego.
2. Na podstawie analizy rysunków podaj jedną różnicę w budowie miękiszu asymilacyjnego liści klonu cukrowego rosnących w różnych warunkach oświetlenia.
Wybór odpowiedniej blaszki oraz roztworu w celu przeprowadzenia reakcji chemicznej. Zadanie 17.1. Arkusz CKE chemia maj 2020 rozszerzony (1 punkt)
W celu porównania reaktywności różnych metali wykonano doświadczenie, w którym płytkę z metalu M zważono i umieszczono w naczyniu zawierającym wodny roztwór pewnej soli. W wyniku zachodzącej reakcji roztwór się odbarwił. Płytkę wyjęto, opłukano wodą destylowaną, wysuszono i zważono ponownie. Ustalono, że w wyniku reakcji masa płytki zmalała.

Wybierz i podkreśl jeden symbol metalu w zestawie I i jeden wzór odczynnika w zestawie II, tak aby otrzymać schemat przeprowadzonego doświadczenia.
Zapis równania reakcji chemicznej przebiegającej po wprowadzeniu blaszki do roztworu. Zadanie 17.2. Arkusz CKE chemia maj 2020 rozszerzony (1 punkt)
W celu porównania reaktywności różnych metali wykonano doświadczenie, w którym płytkę z metalu M zważono i umieszczono w naczyniu zawierającym wodny roztwór pewnej soli. W wyniku zachodzącej reakcji roztwór się odbarwił. Płytkę wyjęto, opłukano wodą destylowaną, wysuszono i zważono ponownie. Ustalono, że w wyniku reakcji masa płytki zmalała.

Napisz w formie jonowej skróconej równanie reakcji, która zaszła podczas doświadczenia.
Tutorial: jak zmieniła się masa blaszki?
Na filmie omówiono jak można określić, czy masa blaszki zmieniła się oraz czy był to wzrost, czy spadek jej masy.
Przygotowanie roztworu zawierającego jony Zn2+ o określonym stężeniu molowym (blaszki). Podręcznik 8.2 zad. 5
Cynk jest metalem aktywniejszym od miedzi.
Wykonując stosowne obliczenia oraz dysponując wodą destylowaną, niezbędnym szkłem laboratoryjnym, blaszką cynkową o masie 5 g oraz 80 cm³ wodnego roztworu siarczanu(VI) miedzi(II) o stężeniu 0,25 mol∙dm–3, zaprojektuj doświadczenie, którego celem będzie uzyskanie roztworu o stężeniu jonów Zn2+ równym 0,2 mol∙dm–3. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Odróżnianie wodnych roztworów azotanu(V) srebra różniących się stężeniem molowym (blaszki). Podręcznik 8.2 zad. 6
W dwóch nieopisanych kolbach miarowych o pojemności 250 cm3 każda, znajdowały się jednakowe objętości wodnych roztworów azotanu(V) srebra o stężeniach 0,1 mol∙dm–3 oraz 0,5 mol∙dm–3.
Zaproponuj doświadczenie, którego celem będzie odróżnienie zawartości wymienionych naczyń, jeśli dysponujesz identycznymi blaszkami cynkowymi, wagą laboratoryjną, cylindrem miarowym oraz dwiema zlewkami. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie zmiany masy blaszki do momentu 5-krotnego zmniejszenia się stężenia jonów srebra
W kolbie umieszczono 200 cm3 roztworu azotanu(V) srebra zawierającego 1,7 g substancji rozpuszczonej. W roztworze tym zanurzono blaszkę wykonaną z ołowiu.
Na podstawie niezbędnych obliczeń ustal, o ile miligramów zmieniła się masa blaszki do momentu, w którym stężenie jonów Ag+ zmalało 5-krotnie? Rozwiązanie tego zadania dostępne jest nieodpłatnie pod poniższym linkiem: © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Ocena, czy masa manganowej blaszki uległa zwiększeniu, czy zmniejszeniu (blaszki)
W wodnym roztworze chlorku kobaltu(II) zanurzono blaszkę wykonaną z manganu. Po zakończeniu reakcji chemicznej stwierdzono, że jej masa uległa zmianie.
Oceń, czy masa blaszki uległa zwiększeniu, czy zmniejszeniu? Odpowiedź uzasadnij odpowiednimi obliczeniami. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wskazanie probówek, w których masa blaszki uległa zwiększeniu po wprowadzeniu do roztworu soli niklu (blaszki)
Do czterech probówek zawierających kolejno blaszki: kadmową, miedzianą, cynkową oraz srebrną dodano wodnego roztworu NiSO4, który ma barwę zieloną.
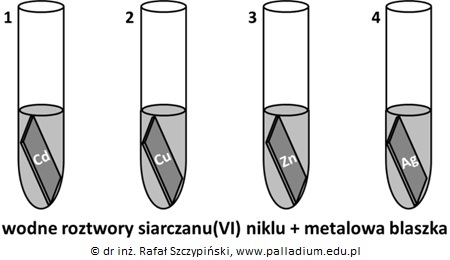
Po zakończeniu doświadczenia stwierdzono, że masy niektórych blaszek uległy zmianie.
Podaj numery tych probówek, w których masa blaszek uległa zwiększeniu. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wskazanie probówek, w których nie zaobserwowano objawów reakcji po wprowadzeniu blaszki do roztworu soli niklu (blaszki)
Do czterech probówek zawierających kolejno blaszki: kadmową, miedzianą, cynkową oraz srebrną dodano wodnego roztworu NiSO4, który ma barwę zieloną.

Wymień numery tych probówek, w których nie zaobserwowano objawów świadczących o przebiegu reakcji chemicznej oraz napisz, co zaobserwowano w probówkach, w których reakcja przebiegła? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wypieranie metalu z roztworu soli za pomocą innego metalu, skład procentowy blaszki
W roztworze azotanu(V) bizmutu(III) o objętości równej 200 cm3 zanurzono płytkę niklową o masie 29,5 g. Po całkowitym usunięciu jonów Bi3+ z roztworu stwierdzono, że masa płytki wynosi 32 g.
Określ w procentach masowych skład płytki po zakończeniu reakcji. Wyniki obliczeń podaj z dokładnością do pierwszego miejsca po przecinku. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie liczby atomów kobaltu osadzonych na blaszce (blaszki)
W wodnym roztworze chlorku kobaltu(II) zanurzono blaszkę wykonaną z manganu. Po zakończeniu reakcji chemicznej stwierdzono, że jej masa zmieniła się o 20 mg.
Oblicz, ile miligramów jonów manganu(II) pojawiło się w roztworze oraz ile atomów kobaltu osadziło się na blaszce? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie, jaki procent jonów został usunięty z roztworu (blaszki)
W 100 cm3 roztworu siarczanu(VI) miedzi(II) o stężeniu 0,5 mol∙dm–3 zanurzono płytkę niklową o masie równej 5 g. W układzie przebiegła reakcja chemiczna opisana równaniem:
Ni + Cu2+ → Ni2+ + Cu
Po jej zakończeniu płytkę przemyto wodą dejonizowaną, wysuszono i zważono. Stwierdzono, że jej masa wynosi 5,125 g.
Oblicz, jaki procent jonów miedzi(II) został usunięty z roztworu? Przyjmij, że masa mola atomów niklu wynosi 59 g, a miedzi 64 g. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie o ile procent zmienia się masa blaszki po usunięciu wszystkich jonów z roztworu (blaszki)
W 100 cm3 roztworu siarczanu(VI) miedzi(II) o stężeniu 0,5 mol∙dm–3 zanurzono płytkę niklową o masie równej 5 g. W układzie przebiegła reakcja chemiczna opisana równaniem:
Ni + Cu2+ → Ni2+ + Cu
Po jej zakończeniu płytkę przemyto wodą dejonizowaną, wysuszono i zważono. Stwierdzono, że jej masa wynosi 5,125 g.
Oblicz, o ile procent zwiększyłaby się masa wyjściowej blaszki, gdyby z roztworu usunięte zostały wszystkie jony Cu2+? Przyjmij, że masa mola atomów niklu wynosi 59 g, a miedzi 64 g. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wypieranie metalu z roztworu soli za pomocą innego metalu (blaszki), obliczanie stężenia molowego
W zlewce umieszczono 50 cm3 roztworu azotanu(V) srebra i zanurzono w nim blaszkę cynkową. Po 24 godzinach blaszkę wyjęto, przemyto i wysuszono. Po jej zważeniu stwierdzono przyrost masy równy 3,02 g.
Wiedząc, że całe srebro zostało usunięte z roztworu oblicz stężenie molowe jonów azotanowych(V). Wynik podaj z dokładnością do jednego miejsca po przecinku. Przyjmij, że objętość roztworu przed i po zakończeniu doświadczenia była taka sama. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wypieranie metalu z roztworu soli za pomocą innego metalu (blaszki), obliczanie stężenia molowego
W roztworze azotanu(V) bizmutu(III) o objętości równej 200 cm3 zanurzono płytkę niklową o masie 29,5 g. Po całkowitym usunięciu jonów Bi3+ z roztworu stwierdzono, że masa płytki wynosi 32 g.
Oblicz, jakie było stężenie jonów bizmutu(III) przed reakcją oraz jakie było stężenie jonów niklu(II) po jej zakończeniu? Wyniki obliczeń podaj z dokładnością do trzeciego miejsca po przecinku. Przyjmij, że objętość roztworu przed i po zakończeniu doświadczenia była taka sama. © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Obliczanie stężenia molowego roztworu azotanu(V) srebra użytego do posrebrzenia przedmiotu (blaszki)
W celu poprawienia estetyki, przedmioty wykonane z żelaza pokrywa się cienką warstwą metalicznego srebra, czemu towarzyszy przebieg reakcji chemicznej opisanej równaniem:
Fe + 3Ag+ → Fe3+ + 3Ag
W wodnym roztworze azotanu(V) srebra o objętości równej 485 cm3 całkowicie zanurzono żelazny przedmiot o masie 20 g.
Oblicz, jakie powinno być stężenie molowe opisanego roztworu azotanu(V) srebra, aby osadzone srebro stanowiło dokładnie 5% masy posrebrzonego nim przedmiotu? © dr inż. Rafał Szczypiński, wszelkie prawa zastrzeżone
Wskazanie właściwej blaszki oraz zapis równania reakcji chemicznej. Zadanie 22. Arkusz CKE chemia maj 2016 rozszerzony (1 punkt)
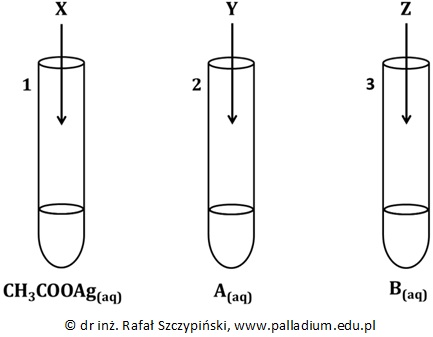
Przeprowadzono doświadczenie zilustrowane poniższym schematem.
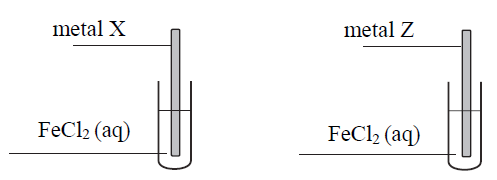
Celem doświadczenia było odróżnienie dwóch, oznaczonych umownie literami X i Z, metali,z których wykonano płytki. Wiadomo, że jednym metalem był cynk, a drugim – nikiel. Po pewnym czasie obie płytki wyjęto z roztworów, osuszono i zważono. Stwierdzono, że zmieniła się tylko masa płytki wykonanej z metalu X.
Uzupełnij poniższe zdania. Wybierz i zaznacz właściwe określenie spośród podanych w każdym nawiasie oraz napisz w formie jonowej skróconej równanie zachodzącej reakcji. Masa płytki wykonanej z metalu X się (zmniejszyła / zwiększyła). Podczas przeprowadzonego doświadczenia przebiegła reakcja zilustrowana równaniem: Metalem Z był (cynk / nikiel).